Calcein
Calcein, auch bekannt unter dem Namen Fluorexon, ist ein Fluorescein-Derivat und ein Fluoreszenzfarbstoff mit einem Anregungsmaximum bei 494 nm (Excitation) und einem Abstrahlungsmaximum (Emissionsmaximum) von 517 nm (bei einem pH-Wert von 9,0).[5] Eine Konzentration oberhalb von 0,1 mol/l führt zur Fluoreszenzlöschung.
| Strukturformel | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
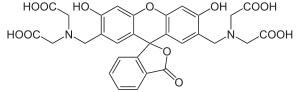 | ||||||||||||||||||||||
| Allgemeines | ||||||||||||||||||||||
| Name | Calcein | |||||||||||||||||||||
| Andere Namen |
| |||||||||||||||||||||
| Summenformel | C30H26N2O13 | |||||||||||||||||||||
| Kurzbeschreibung |
orangefarbenes Pulver[1] | |||||||||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Eigenschaften | ||||||||||||||||||||||
| Molare Masse | 622,51 g·mol−1 | |||||||||||||||||||||
| Aggregatzustand |
fest | |||||||||||||||||||||
| Löslichkeit |
| |||||||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||||||||
Struktur
Bei Calcein handelt es sich um eine nicht planare aromatische Verbindung. Als Anion sind die verschiedenen Carboxygruppen deprotoniert, so dass Calcein unter jenen Bedingungen hydrophil ist. Kommerziell ist es als freie Säure und 4',5'-Isomer verfügbar. Im Handel wurden aber im Laufe der Zeit bereits verschiedene andere Isomere bereitgestellt.
Anwendungen
Komplexometrie
Calcein wird in der Komplexometrie aufgrund seiner zahlreichen Carboxylatgruppen als Indikator bei Titrationen von Calciumionen mit EDTA und für fluorometrische Bestimmungen von Calcium und Magnesium verwendet. Darüber hinaus komplexiert es auch andere Ionen wie Cu2+, Fe2+, Fe3+ und Ni2+.
Zellbiologie
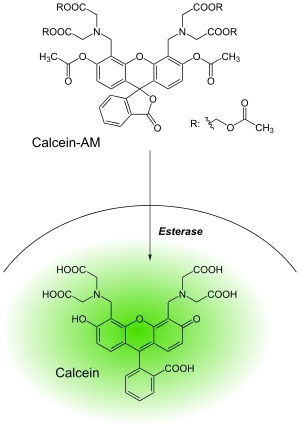
Als Acetoxymethylester von Calcein wird Calcein-AM (AM = Acetoxymethylester) bezeichnet. Hierbei sind vier Carboxygruppen verestert, es liegt zudem als Lacton vor. Die beiden restlichen Hydroxygruppen sind mit Essigsäure verestert. Calcein-AM wird in der Zellbiologie verwendet. Es wird zum Test der Zellviabilität (Zelladhäsion, Chemotaxis) und für die kurzzeitige Markierung lebender Zellen verwendet. Alternativ können Fura-2, Furaptra, Indo-1 und Aequorin verwendet werden.
Calcein-AM kann durch die Zellmembran hindurch in lebende Zellen transportiert werden. Die Acetoxymethyl-Gruppe maskiert den Molekülteil, der in der Lage ist, Calcium zu chelatisieren. Nach dem Transport in die Zelle werden die Acetoxymethyl- und die Acetatgruppen enzymatisch durch Esterasen abgespalten und in Calcein umgewandelt. Dieses ist dann in der Lage, Calciumionen innerhalb der Zelle zu binden (zu komplexieren), was in einer starken, grünen Fluoreszenz resultiert. Calcein ist kaum cytotoxisch, da es vitale Zellprozesse wie beispielsweise die Zellteilung nicht beeinflusst. Der Komplex verbleibt dabei in der Zelle, da er die Zellmembran nicht selbst passieren kann. Jedoch verfügen viele Zellen über einen ABC-Transporter, der aktiv Calcein aus der Zelle ausschleust. Diese Zellen leuchten dann ebenfalls nicht. Die Ausbildung dieser Transporter ist ein wichtiger Faktor bei der Ausbildung von Resistenzen gegen Arzneistoffe, beispielsweise Zytostatika und Antibiotika.
Da abgestorbene Zellen über keine aktiven Esterasen verfügen und deshalb kein Calcium-bindendes Calcein erzeugen können, werden lediglich lebende Zellen markiert. Diese fluoreszieren grün. Häufig wird zusätzlich ein zweiter Fluoreszenzfarbstoff eingesetzt, z. B. das Ethidium-Homodimer-1, welches durch beschädigte Zellmembranen in die Zelle eindringen und dort an Nukleinsäuren binden kann. So werden abgestorbene Zellen rot gefärbt und können deutlich von lebenden Zellen unterschieden werden. In einer weiteren Anwendung dient es als Zellmarker für Apoptose. Calcein kann aber auch direkt in die Zellen injiziert werden.
Außerhalb der Zelle wird Calcein zum Markieren von frisch geschlüpften Fischen[6] oder als Testsubstanz in der Dermatologie verwendet. Die Anzahl von Zellen auf Mikrotiterplatten kann ebenfalls mit Calcein getestet werden.
Literatur
- Horobin, RW. und Kiernan, JA. (2002): Conn's Biological Stains: A Handbook of Dyes, Stains and Fluorochromes for Use in Biology and Medicine. BIOS Scientific Publ., 10. Auflage; ISBN 1-85996-099-5; S. 249ff.
Einzelnachweise
- Eintrag zu Calcein. In: Römpp Online. Georg Thieme Verlag, abgerufen am 17. November 2014.
- Datenblatt Calcein bei Panreac.com, abgerufen am 29. November 2012.
- interchim.fr: Produktinformation Calceins, abgerufen am 17. November 2014.
- Datenblatt Calcein bei Sigma-Aldrich, abgerufen am 25. Mai 2011 (PDF).
- Horobin, RW. und Kiernan, JA. (2002): Conn's Biological Stains: A Handbook of Dyes, Stains and Fluorochromes for Use in Biology and Medicine. BIOS Scientific Publ., 10. Auflage; ISBN 1-85996-099-5; S. 249.
- Marking fry using calcein.