Arsensäure
Arsensäure (auch Arsen(V)-säure genannt) ist die von Diarsenpentaoxid abgeleitete Säure mit der Summenformel H3AsO4. Es ist eine dreiprotonige, mittelstarke Säure und etwa so stark wie Phosphorsäure. Die Salze der Arsensäure heißen Arsenate.
| Strukturformel | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
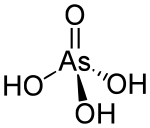 | ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | Arsensäure | |||||||||||||||
| Andere Namen |
Arsen(V)-säure | |||||||||||||||
| Summenformel | H3AsO4 | |||||||||||||||
| Kurzbeschreibung |
durchsichtig bis weißer, geruchloser Feststoff[1] | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 141,94 g·mol−1 | |||||||||||||||
| Aggregatzustand |
fest[1] | |||||||||||||||
| Dichte |
2,50 g·cm−3[1] | |||||||||||||||
| Schmelzpunkt | ||||||||||||||||
| Siedepunkt |
120 °C[1] | |||||||||||||||
| Dampfdruck | ||||||||||||||||
| pKS-Wert | ||||||||||||||||
| Löslichkeit |
leicht löslich in Wasser[1] | |||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Zulassungsverfahren unter REACH |
besonders besorgniserregend: krebserzeugend (CMR)[4]; zulassungspflichtig[5] | |||||||||||||||
| MAK |
| |||||||||||||||
| Toxikologische Daten | ||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||
Gewinnung und Darstellung
Arsensäure bildet sich durch Lösen von Arsenpentaoxid in Wasser:
Das Gleichgewicht dieser chemischen Reaktion kann zur linken Seite verschoben werden. Durch Entzug von Wasser beispielsweise mit Phosphorpentoxid bildet sich aus Arsensäure wieder Arsenpentaoxid.
Eine weitere Reaktion zur Darstellung von Arsensäure ist die Oxidation von Arsen oder Arsen(III)-oxid mit Hilfe konzentrierter Salpetersäure. Dabei bildet sich das Hemihydrat:
Das Dihydrat (H3AsO4 · 2H2O) ist nur über die Kristallisation während mehrerer Tage bei −30 °C zugänglich.[7]
Eigenschaften
Feste Arsensäure entzieht der Luft sehr schnell Wasser und bildet Hydrate: H3AsO4 · ½H2O beziehungsweise H3AsO4 · 2H2O bei −30 °C. Beim Erhitzen auf 100 °C entsteht As2O5 · 1,66H2O, über 300 °C wird alles Wasser freigesetzt.
Eine gesättigte wässrige Lösung ist ungefähr 80%ig.
Sicherheitshinweise und gesetzliche Regelungen
Arsensäure wurde im Dezember 2011 aufgrund seiner Einstufung als krebserzeugend (Carc. 1A) in die Kandidatenliste der besonders besorgniserregenden Stoffe (Substance of very high concern, SVHC) aufgenommen.[4] Im August 2014 wurde Arsensäure danach in das Verzeichnis der zulassungspflichtigen Stoffe mit dem Ablauftermin für die Verwendung in der EU zum 22. August 2017 aufgenommen.[8] Als Arsenverbindung unterliegt Arsensäure außerdem den Beschränkungen im Anhang XVII, Nummer 19 der REACH-Verordnung.[9]
Einzelnachweise
- Eintrag zu Arsensäure in der GESTIS-Stoffdatenbank des IFA, abgerufen am 20. Januar 2022. (JavaScript erforderlich)
- David R. Lide (Hrsg.): CRC Handbook of Chemistry and Physics. 90. Auflage. (Internet-Version: 2010), CRC Press/Taylor and Francis, Boca Raton, FL, Dissociation Constants of Inorganic Acids and Bases, S. 8-40.
- Nicht explizit in Verordnung (EG) Nr. 1272/2008 (CLP) gelistet, fällt aber mit der angegebenen Kennzeichnung unter den Gruppeneintrag Arsensäure und seine Salze, soweit in diesem Anhang nicht gesondert aufgeführt im Classification and Labelling Inventory der Europäischen Chemikalienagentur (ECHA), abgerufen am 9. Januar 2017. Hersteller bzw. Inverkehrbringer können die harmonisierte Einstufung und Kennzeichnung erweitern.
- Eintrag in der SVHC-Liste der Europäischen Chemikalienagentur, abgerufen am 17. Juli 2014.
- Eintrag im Verzeichnis der zulassungspflichtigen Stoffe der Europäischen Chemikalienagentur, abgerufen am 17. Juli 2014.
- Schweizerische Unfallversicherungsanstalt (Suva): Grenzwerte – Aktuelle MAK- und BAT-Werte (Suche nach 7778-39-4 bzw. Arsensäure), abgerufen am 24. Oktober 2016.
- G. Brauer (Hrsg.), Handbook of Preparative Inorganic Chemistry 2nd ed., vol. 1, Academic Press 1963, S. 601.
- Verordnung (EU) Nr. 895/2014
- ECHA: Liste der beschränkten Stoffe – Anhang XVII der REACH-Verordnung, abgerufen am 5. September 2020.



