Anatoxin A
Anatoxin A, auch bekannt als Very Fast Death Factor (VFDF), ist ein neurotoxisches Alkaloid, das von einer Vielzahl von Cyanobakterien produziert wird. Das Toxin als Reinsubstanz, bei Raumtemperatur eine ölige Flüssigkeit, wurde 1977 von John P. Devlin aus einer Kolonie der Cyanobacterien Anabaena flos-aquae, NRC-44h, extrahiert.[2] Anatoxin A ist außerordentlich toxisch. Der LD50-Wert für Mäuse liegt bei intraperitonealer Verabreichung bei etwa 0,25 mg/kg KG.[5][6][7] Bei oraler Aufnahme tötet es innerhalb von wenigen Minuten. In sehr kleinen Mengen wird Anatoxin A für die Grundlagenforschung produziert.
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
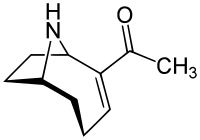 | |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Anatoxin A | ||||||||||||||||||
| Andere Namen | |||||||||||||||||||
| Summenformel | C10H15NO | ||||||||||||||||||
| Kurzbeschreibung |
ölige Flüssigkeit[2] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 165,232 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
flüssig, als Hydrochlorid weißes Pulver,[2] als Fumarat leicht braunes Pulver[3] | ||||||||||||||||||
| Löslichkeit |
wenig in Wasser (15 mg·ml−1, Fumarat)[4] | ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Toxikologische Daten | |||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||||||||||||
Wirkmechanismus
Anatoxin A ist ein Agonist nikotinerger Acetylcholinrezeptoren. Es bindet an neurale α4β2-, α4- und muskuläre α12βγδ-Rezeptoren.[8] Im gesunden Körper bindet Acetylcholin an postsynaptische Rezeptoren und verursacht eine Konformationsänderung, die den Ionenkanal öffnet. Positive Ionen fließen in Folge in die Zelle, depolarisieren sie und können so ein Aktionspotential (oder eine Muskelkontraktion) auslösen. Anatoxin A bindet an die gleichen Rezeptoren und verursacht eine irreversible Konformationsänderung, die den Kanal dauerhaft öffnet. Nach einer Weile wird der Ionenkanal desensitiv und kann nicht länger Kationen passieren lassen, was letztendlich zu einer Blockade der Signalweiterleitung führt. Anatoxin A ähnelt in seiner Wirkung anderen Acetylcholinrezeptoragonisten wie beispielsweise Nicotin des Tabaks, Cytisin des Goldregens, Epibatidin der Baumsteigerfrösche und Arecolin der Betelnüsse.
Analytik
Für die unterschiedlichen Untersuchungsmaterialien wie Wasser,[9] Umweltproben[10] oder Mageninhalt von Hunden[11] stehen Verfahren zur zuverlässigen Bestimmung von Anatoxin unter Anwendung der HPLC in Kopplung mit der Massenspektrometrie zur Verfügung. Eine adäquate Probenvorbereitung ist unabdingbar.
Symptome
Symptome einer Anatoxin-A-Vergiftung sind ein Verlust der Koordinationsfähigkeit, Krämpfe und schließlich der Tod durch Atemstillstand. Diese Symptome treten bemerkenswert schnell auf, was den englischen Namen very fast death factor (dt.: ‚sehr schneller Todesfaktor‘) bedingt. Innerhalb weniger Minuten können Cyanobakterien der Art Anabaena flos-aquae muskuläre Faszikulationen und Verlust der Koordinationsfähigkeit verursachen, wenn sie z. B. in den Magen von Rindern gelangen (wie experimentell an zwei Bullen gezeigt wurde). Der Tod der Rinder durch Atemstillstand tritt in einem Zeitraum von wenigen Minuten bis zu einer Stunde ein.[12] Wird das Toxin intraperitoneal injiziert, wirkt es auf Mäuse innerhalb von zwei bis fünf Minuten tödlich. Die Symptome sind auch hier Zuckungen, Muskelkrämpfe, Lähmung und schließlich Atemstillstand.
Bedrohung für Fauna

Seit seiner Entdeckung sind zahlreiche Fälle von Vergiftungen durch Anatoxin A bekannt geworden. Diese Fälle betreffen sowohl Wild- als auch Nutztiere, die mit Anatoxin A kontaminiertes Wasser zu sich nehmen. Der Tod zahlreicher Haushunde in den letzten 20 Jahren in Neuseeland, Frankreich, den Vereinigten Staaten und Schottland wurde durch Analyse des Mageninhalts auf Anatoxin A zurückgeführt.[13][14][15] In allen Fällen zeigten die Hunde innerhalb von wenigen Minuten typische Symptome, wie Muskelkrämpfe und erlagen der Vergiftung in wenigen Stunden. Außerdem berichten Rinderfarmen in den Vereinigten Staaten, Kanada und Finnland in den letzten 30 Jahren von Todesfällen bei Nutzvieh durch Anatoxin-A-verseuchtes Trinkwasser.[16]
Im Herbst 1999 fielen im Bogoriasee in Kenia etwa 30.000 Flamingos Anatoxin A zum Opfer. Auch hier wurde das Toxin im Mageninhalt verendeter Tiere und in deren Exkrementen gefunden. Bis heute sorgen die dort vorkommenden Anatoxin-A-produzierenden Cyanobakterien für ein alljährliches Massensterben unter den Flamingos, die sich von nichttoxischen Cyanobakterien, meist Spirulina ernähren. Die verursachenden Organismen treten natürlicherweise im Wasser des Sees und insbesondere in Mikrobenmatten in geringem Maß auf, die um die warmen Quellen im Seebett wachsen.[17]
Geschichte
Nach dem Verenden einiger Kühe, die Wasser aus dem unter Algenblüte stehenden kanadischen Burton Lake, 120 km östlich von Saskatoon, Saskatchewan getrunken hatten, wurden im Juni 1961 Proben aus dem See entnommen[2] und systematisch untersucht. Das von diesen Organismen produzierte Toxin, das Mäuse in zwei bis fünf Minuten zu töten vermag, wurde wegen seiner raschen Wirkung von Paul Gorham Very Fast Death Factor genannt.[18] Anatoxin A als Reinstoff wurde 1977 beschrieben. Die „verlässlichste und effizienteste“ Methode,[2] Anatoxin A zu produzieren, gelingt aus einer leicht sauren Suspension der Cyanobakterien. Diese Lösung wird gefriergetrocknet, mit HCl in Methanol ausgewaschen und der Extrakt eingedampft. Der Rückstand wird zunächst mit Benzol ausgewaschen, um neutrale Komponenten zu entfernen. Der Rückstand wird dann in Ethanol gelöst und die Lösung mit Chloroform versetzt. Ungewünschte Stoffe fallen aus, während das Toxin im Chloroform gelöst bleibt. Dies lässt einen Feststoff zurück, der reich an Anatoxin-A-Hydrochlorid ist.[2] Die Totalsynthese von Anatoxin A gelang 1977 aus Kokain. Damit wurden sowohl Struktur als auch Stereochemie geklärt.[19] Eine Reihe von Cyanobakterien, die Anatoxin A produzieren können, sind bekannt, zum Beispiel Aphanizomenon issatschenkoi.[20]
Grundlagenforschung
Anatoxin A wird in der Grundlagenforschung modellweise eingesetzt, um Krankheiten zu simulieren, die sich durch niedrige Acetylcholinwerte auszeichnen. Das betrifft beispielsweise Muskeldystrophie, Myasthenia gravis, die Alzheimer-Krankheit und die Parkinson-Krankheit.
Anatoxin A(S)
Anatoxin A(S) ("S" für "salivary", engl. Speichelfluss), ebenfalls von Cyanobakterien produziert, verursacht ähnliche Symptome wie Anatoxin A, ist aber eine völlig andere chemische Verbindung (Organophosphat) mit einem anderen Wirkmechanismus (Hemmung der Acetylcholinesterase). Aufgrund der ähnlichen Symptomatik wurden beide Verbindungen zunächst für Varianten desselben Toxins gehalten. Ein Unterscheidungskriterium ist, dass Anatoxin A(S) im Gegensatz zu Anatoxin A den Parasympathikus stark anregt, was u. a. zum genannten Speichelfluss führt.[21]
Siehe auch
- Aplysiatoxin und Microcystine (Giftstoffe, die ebenfalls von Cyanobakterien produziert werden.)
Literatur
- S. J. Roe, R. A. Stockman: A two-directional approach to the anatoxin alkaloids: second synthesis of homoanatoxin and efficient synthesis of anatoxin-a. In: Chemical Communications. Nummer 29, August 2008, S. 3432–3434, doi:10.1039/b804304c. PMID 18633513.
- Rick L. Danheiser, John M. Morin, Edward J. Salaski: Efficient total synthesis of (±)-anatoxin a. In: Journal of the American Chemical Society. 107, 1985, S. 8066–8073, doi:10.1021/ja00312a045.
- S. Vlad, W. B. Anderson u. a.: Removal of the cyanotoxin anatoxin-a by drinking water treatment processes: a review. In: Journal of water and health. Band 12, Nummer 4, Dezember 2014, S. 601–617, doi:10.2166/wh.2014.018. PMID 25473970 (Review).
- J. Osswald, S. Rellán u. a.: Toxicology and detection methods of the alkaloid neurotoxin produced by cyanobacteria, anatoxin-a. In: Environment international. Band 33, Nummer 8, November 2007, S. 1070–1089, doi:10.1016/j.envint.2007.06.003. PMID 17673293 (Review).
- B. Puschner, B. Hoff, E. R. Tor: Diagnosis of anatoxin-a poisoning in dogs from North America. In: Journal of veterinary diagnostic investigation : official publication of the American Association of Veterinary Laboratory Diagnosticians, Inc. Band 20, Nummer 1, Januar 2008, S. 89–92. PMID 18182518.
- E. Devic, D. Li u. a.: Detection of anatoxin-a(s) in environmental samples of cyanobacteria by using a biosensor with engineered acetylcholinesterases. In: Applied and environmental microbiology. Band 68, Nummer 8, August 2002, S. 4102–4106. PMID 12147513, PMC 123992 (freier Volltext).
Einzelnachweise
- Eberhard Breitmaier: Alkaloide. Springer-Verlag, 2008, ISBN 978-3-8348-0531-7, S. 35 (eingeschränkte Vorschau in der Google-Buchsuche).
- J. P. Devlin, O. E. Edwards, P. R. Gorham, N. R. Hunter, R. K. Pike, B. Stavric: Anatoxin-a, a toxic alkaloid from NRC-44h. In: Canadian Journal of Chemistry. 55, 1977, S. 1367–1371, doi:10.1139/v77-189.
- Datenblatt (±)-Anatoxin A fumarate bei Tocris, abgerufen am 22. September 2018.
- Datenblatt (+)-Anatoxin-A fumarate bei Sigma-Aldrich, abgerufen am 28. April 2015 (PDF).
- W. T. Shier: Handbook of Toxinology. CRC Press, 1990, ISBN 0-8247-8374-3, S. 560 (eingeschränkte Vorschau in der Google-Buchsuche).
- Nobuhiro Fusetani: Marine Toxins as Research Tools. Springer Science & Business Media, 2009, ISBN 978-3-540-87895-7, S. 5 (eingeschränkte Vorschau in der Google-Buchsuche).
- Antonia Herrero: The Cyanobacteria. Horizon Scientific Press, 2008, ISBN 978-1-904455-15-8, S. 162 (eingeschränkte Vorschau in der Google-Buchsuche).
- R. Aráoz, J. Molgó, N. Tandeau de Marsac: Neurotoxic cyanobacterial toxins. In: Toxicon. Band 56, Nummer 5, Oktober 2010, S. 813–828, doi:10.1016/j.toxicon.2009.07.036. PMID 19660486 (Review).
- H. K. Yen, T. F. Lin, P. C. Liao: Simultaneous detection of nine cyanotoxins in drinking water using dual solid-phase extraction and liquid chromatography-mass spectrometry. In: Toxicon. 58(2), Aug 2011, S. 209–218. PMID 21699910
- C. Rivetti, C. Gómez-Canela, S. Lacorte, C. Barata: Liquid chromatography coupled with tandem mass spectrometry to characterise trace levels of cyanobacteria and dinoflagellate toxins in suspended solids and sediments. In: Anal Bioanal Chem. 407(5), Feb 2015, S. 1451–1462. PMID 25619981
- B. Puschner, B. Hoff, E. R. Tor: Diagnosis of anatoxin-a poisoning in dogs from North America. In: J Vet Diagn Invest. 20(1), Jan 2008, S. 89–92. PMID 18182518
- W. W. Carmichael, P. R. Gorham, D. F. Biggs: Two laboratory case studies on the oral toxicity to calves of the freshwater cyanophyte (blue-green alga) Anabaena flos-aquae NRC-44-1. In: The Canadian veterinary journal. Band 18, Nummer 3, März 1977, S. 71–75. PMID 404019, PMC 1697489 (freier Volltext).
- S. A. Wood, A. I. Selwood, A. Rueckert, P. T. Holland, J. R. Milne, K. F. Smith, B. Smits, L. F. Watts, C. S. Cary: First report of homoanatoxin-a and associated dog neurotoxicosis in New Zealand. In: Toxicon. Band 50, Nummer 2, August 2007, S. 292–301, doi:10.1016/j.toxicon.2007.03.025. PMID 17517427.
- M. Gugger, S. Lenoir, C. Berger, A. Ledreux, J. C. Druart, J. F. Humbert, C. Guette, C. Bernard: First report in a river in France of the benthic cyanobacterium Phormidium favosum producing anatoxin-a associated with dog neurotoxicosis. In: Toxicon. Band 45, Nummer 7, Juni 2005, S. 919–928, doi:10.1016/j.toxicon.2005.02.031. PMID 15904687.
- B. Puschner, B. Hoff, E. R. Tor: Diagnosis of anatoxin-a poisoning in dogs from North America. In: Journal of veterinary diagnostic investigation. Band 20, Nummer 1, Januar 2008, S. 89–92. PMID 18182518.
- EPA Report on Anatoxin-a (Memento vom 4. Juli 2015 im Internet Archive), abgerufen am 28. April 2015.
- L. Krienitz, A. Ballot, K. Kotut, C. Wiegand, S. Pütz, J. S. Metcalf, G. A. Codd, S. Pflugmacher: Contribution of hot spring cyanobacteria to the mysterious deaths of Lesser Flamingos at Lake Bogoria, Kenya. In: FEMS microbiology ecology. Band 43, Nummer 2, März 2003, S. 141–148, doi:10.1111/j.1574-6941.2003.tb01053.x. PMID 19719674.
- Paul R. Gorham: Laboratory Studies on the Toxins Produced by Waterblooms of Blue-Green Algae. In: American Journal of Public Health and the Nations Health. 52, 1962, S. 2100–2105, doi:10.2105/AJPH.52.12.2100.
- H. F. Campell, O. E. Edwards, R. Kolt: Synthesis of nor-anatoxin-a and anatoxin-a. In: Canadian Journal of Chemistry. 55, 1977, S. 1372–1379, doi:10.1139/v77-190.
- Susanna A. Wood, John Paul Rasmussen u. a.: First Report of the Cyanotoxin Anatoxin-A from Aphanizomenon issatschenkoi (cyanobacteria). In: Journal of Phycology. 43, 2007, S. 356–365, doi:10.1111/j.1529-8817.2007.00318.x.
- https://www.spektrum.de/magazin/cyanobakterielle-toxine/821423; abgerufen am 16. September 2019
