Aluminiumphosphid
Aluminiumphosphid (AlP) ist das Reaktionsprodukt von Aluminium mit elementarem Phosphor.
| Kristallstruktur | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
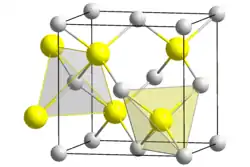 | |||||||||||||||||||
| _ Al3+ _ P3− | |||||||||||||||||||
| Kristallsystem |
kubisch[1] | ||||||||||||||||||
| Raumgruppe |
F43m (Nr. 216)[1] | ||||||||||||||||||
| Gitterparameter |
a = 546,35 pm[1] | ||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Aluminiumphosphid | ||||||||||||||||||
| Verhältnisformel | AlP | ||||||||||||||||||
| Kurzbeschreibung |
dunkelgelblicher bis grauer Feststoff mit carbidähnlichem Geruch[2] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 57,90 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
fest | ||||||||||||||||||
| Dichte |
2,4 g·cm−3[2] | ||||||||||||||||||
| Schmelzpunkt | |||||||||||||||||||
| Löslichkeit |
langsame Zersetzung in Wasser[2] | ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Thermodynamische Eigenschaften | |||||||||||||||||||
| ΔHf0 |
−166,5 kJ/mol[5] | ||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||||||||||||
Gewinnung und Darstellung
Aluminiumphosphid kann durch Zusammenschmelzen von rotem Phosphor mit Aluminium gewonnen werden:[6]
Alternativ kann ein äquimolares Gemisch von rotem Phosphor und Aluminium mittels Magnesiumband entzündet werden.[7] Durch die stark exotherme Reaktion treten jedoch ungewollte Nebenreaktionen auf. Andere Herstellungsverfahren (zum Beispiel Verwendung von gelbem Phosphor[8]) werden ebenfalls angewendet.
Eigenschaften
Aluminiumphosphid ist ein dunkelgrauer bis gelblicher kristalliner Feststoff, der beim Kontakt mit Wasser oder Säuren selbstentzündliches und giftiges Monophosphan (PH3) entwickelt.
Aluminiumphosphid besitzt eine kubische Zinkblende-Struktur (ähnlich wie Galliumarsenid), bei der alle Atome tetraederförmig angeordnet sind.
Verwendung
Aluminiumphosphid wird als Schädlingsbekämpfungsmittel (Insektizid und Rodentizid mit Wirkung über die Bildung von Phosphorwasserstoff, der als nukleophiles Agens wichtige Fermentsysteme blockiert.[9]) In der Halbleitertechnik und -forschung wird es als III-V-Halbleiter z. B. zur Herstellung von Aluminiumgalliumindiumphosphid/Indiumgalliumaluminiumphosphid verwendet.
Giftwirkung beim Menschen
In Wasser erfolgt eine Freisetzung von Monophosphan, das die Cytochrom-c-Oxidase sowie andere antioxidative Enzyme blockiert. Dadurch kommt es zum einen durch Hemmung der Atmungskette zu einer verminderten ATP-Produktion und zum anderen zur vermehrten Entstehen freier Sauerstoffradikale. Das Herzgewebe scheint hierbei besonders anfällig für die Giftwirkung.
Typische Symptome sind Atemnot und Zyanose, Brust- und Bauchschmerz, Übelkeit und Erbrechen und Blutdruckabfall bis zum Schock. Todesursache ist meist Multiorganversagen. Es existiert keine kausale Therapie, daher werden Patienten rein symptomatisch und supportiv auf der Intensivstation behandelt.
Literatur
- A. Müssigbrodt, J. Lauschke, G. P. Horn, W. Grimm, B. Maisch: Multiorganversagen nach Suizidversuch mit Aluminiumphosphid, in Intensivmedizin und Notfallmedizin 2007/2, S. 110–115. doi:10.1007/s00390-006-0722-1
Einzelnachweise
- semiconductors.co.uk: Properties of III-V Semiconductors
- Eintrag zu Aluminiumphosphid in der GESTIS-Stoffdatenbank des IFA, abgerufen am 1. Februar 2016. (JavaScript erforderlich)
- Eintrag zu Aluminium phosphide im Classification and Labelling Inventory der Europäischen Chemikalienagentur (ECHA), abgerufen am 1. Februar 2016. Hersteller bzw. Inverkehrbringer können die harmonisierte Einstufung und Kennzeichnung erweitern.
- Landolt Börnstein: Aluminum phosphide (AlP)
- David R. Lide (Hrsg.): CRC Handbook of Chemistry and Physics. 90. Auflage. (Internet-Version: 2010), CRC Press/Taylor and Francis, Boca Raton, FL, Standard Thermodynamic Properties of Chemical Substances, S. 5-5.
- Wayne E. White, A. H. Bushey, Henry F. Holtzclaw Jr., Frank W. Hengeveld: Aluminum Phosphide. In: Inorganic Syntheses. 4, 1953, S. 23–25. doi:10.1002/9780470132357.ch7.
- L. Moser und A. Brukl, Die gravimetrische Bestimmung des Phosphorwasserstoffes und ein neuer Apparat zur Gasanalyse in: Zeitschrift für anorganische und allgemeine Chemie 121, 73-94 (1922)
- Patent DE2945647A1: Verfahren zur Herstellung von Aluminiumphosphid und/oder Magnesiumphosphid. Angemeldet am 12. November 1979, veröffentlicht am 21. Mai 1981, Anmelder: Degesch, Erfinder: F. Horn, E. Fluck. Text
- Biologische Bundesanstalt für Land- und Forstwirtschaft: Berichte Heft 39/1998.


