3-Hydroxypyridin
3-Hydroxypyridin ist eine organische Verbindung mit der Summenformel C5H5NO. Sie ist isomer zu 2-Pyridon und 4-Pyridon, weist jedoch grundlegend verschiedene Eigenschaften und Reaktivität auf.
| Strukturformel | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | 3-Hydroxypyridin | |||||||||||||||
| Andere Namen |
| |||||||||||||||
| Summenformel | C5H5NO | |||||||||||||||
| Kurzbeschreibung |
farbloser Feststoff[1] | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 95,10 g·mol−1 | |||||||||||||||
| Aggregatzustand |
fest | |||||||||||||||
| Schmelzpunkt | ||||||||||||||||
| Löslichkeit |
mäßig in Wasser (33 g·l−1 bei 20 °C)[2] | |||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||
Darstellung
Die Synthese von 3-Hydroxypyridin verläuft durch Umsetzung von Furfural mit Ammoniak. Außerdem kann es durch Reaktion von 3-Brompyridin unter Druck in einer Alkalischmelze erhalten werden.[1]
Eigenschaften
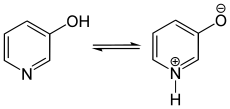
Bezüglich seiner Eigenschaften unterscheidet sich 3-Hydroxypyridin grundlegend von seinen Isomeren 2- und 4-Pyridon, da es keine Ketoform ausbilden kann. Hingegen besitzt 3-Hydroxypyridin eine zwitterionische Grenzstruktur, deren Anteil im chemischen Gleichgewicht vom Lösungsmittel abhängig ist. Somit reagiert 3-Hydroxypyridin phenolähnlich und nicht amidähnlich. Es wird bevorzugt am Stickstoff protoniert, der einen pKs-Wert von 5,2 besitzt.[3]
Vorkommen und Verwendung
3-Hydroxypyridin entsteht in geringen Konzentrationen während der Maillard-Reaktion[4]. Des Weiteren ist es als Pyridoxinstrukturelement beispielsweise in Vitamin B6 zu finden.
Es kann zur Herstellung von Insektiziden und Herbiziden eingesetzt werden. Des Weiteren kann es zur Synthese bestimmter Cholinesteraseinhibitoren, beispielsweise Pyridostigmin, Verwendung finden. Ferner kann es zu 3-Hydroxypiperidin reduziert werden.[1]
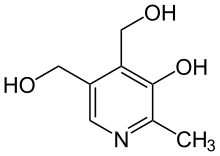 Strukturformel von Pyridoxin
Strukturformel von Pyridoxin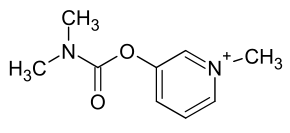 Strukturformel von Pyridostigmin
Strukturformel von Pyridostigmin
Einzelnachweise
- Eintrag zu Pyridinole. In: Römpp Online. Georg Thieme Verlag, abgerufen am 29. September 2014.
- Datenblatt 3-Pyridinol (PDF) bei Merck, abgerufen am 18. März 2011.
- J. A. Joules, K. Mills: Heterocyclic Chemistry 2000, 4. Auflage, Blackwell Science, Oxford, S. 88–91; ISBN 0-632-05453-0.
- Sh. Topova, D. Bojilov, S. Dagnon, O. Argirov: Hydroxypyridine Formation In Model System Monosodium Glutamate And 2-Fufural. In: Applied Science Reports. Band 2, Nr. 2, 2014, S. 71–77, doi:10.15192/PSCP.ASR.2014.2.2.7177 (englisch).
