1,1,1,2-Tetrafluorethan
1,1,1,2-Tetrafluorethan (häufig kurz, aber unpräzise Tetrafluorethan genannt, Handelsname R-134a) ist ein Fluorkohlenwasserstoff (ein Hydrofluoralkan), der als Treib- und Kältemittel sowie als Alternative zu Fluor-Chlor-Kohlenwasserstoffen Verwendung findet.
| Strukturformel | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
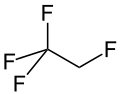 | ||||||||||||||||||||||
| Allgemeines | ||||||||||||||||||||||
| Freiname | Norfluran | |||||||||||||||||||||
| Andere Namen | ||||||||||||||||||||||
| Summenformel | C2H2F4 | |||||||||||||||||||||
| Kurzbeschreibung |
farbloses Gas mit schwach etherischem Geruch[2] | |||||||||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Eigenschaften | ||||||||||||||||||||||
| Molare Masse | 102,04 g·mol−1 | |||||||||||||||||||||
| Aggregatzustand |
gasförmig | |||||||||||||||||||||
| Dichte | ||||||||||||||||||||||
| Schmelzpunkt | ||||||||||||||||||||||
| Siedepunkt |
−26,1 °C[2] | |||||||||||||||||||||
| Dampfdruck | ||||||||||||||||||||||
| Löslichkeit |
schlecht in Wasser (63 mg·l−1 bei 25 °C)[2] | |||||||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||||||||
| ||||||||||||||||||||||
| MAK | ||||||||||||||||||||||
| Treibhauspotential |
1549 (bezogen auf 100 Jahre)[5] | |||||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||||||||
Neben 1,1,1,2-Tetrafluorethan gibt es noch dessen Isomer 1,1,2,2-Tetrafluorethan, das ebenfalls als Tetrafluorethan bezeichnet wird.
Eigenschaften
Tetrafluorethan ist ein farbloses und fast geruchloses Gas, welches durch Druck leicht verflüssigt werden kann. Der kritische Punkt liegt bei 101 °C und 40,6 bar.[2] Beim Abbau in der Umwelt entsteht durch Photooxidation die sehr persistente Trifluoressigsäure (TFA).[6]
Tetrafluorethan hat im Gegensatz zu den FCKW keine zerstörende Wirkung auf die Ozonschicht, ist jedoch ein starkes Treibhausgas. Seine Treibhauswirkung beträgt das 1430fache[7] der gleichen Menge Kohlendioxid bezogen auf einen Zeithorizont von 100 Jahren (siehe Treibhauspotenzial).
Anwendung
Wegen seiner günstigen Eigenschaften findet Tetrafluorethan Anwendung in Kältemaschinen, wie beispielsweise Kühlschränken, Luftentfeuchtern und beim Betrieb von Dampfturbinen im Organic Rankine Cycle ohne Wasserdampf als Arbeitsmittel.
Viele Klimaanlagen basieren auf R-134a als Kältemittel. Dieses darf aber seit 2011 in der EU nicht mehr für Klimaanlagen in Neuwagen genutzt werden.[8] Weitere Anwendung findet es als Test/Prüfmittel für optische Rauchmelder. Tetrafluorethan ist Hauptbestandteil in Kältesprays in der Elektronikindustrie.
Tetrafluorethan wird auch zur Schutzabdeckung von Magnesiumschmelzen verwendet. Hierzu dient in der Regel ein Gasgemisch mit Stickstoff. Das Mischungsverhältnis liegt bei etwa 99,5–99,8 % Stickstoff und 0,5–0,2 % Tetrafluorethan, je nach Einsatzgebiet. In Verbindung mit Luftfeuchte bildet Tetrafluorethan in der Hitze Fluorwasserstoffsäure, die bei Stahl zu erhöhter Korrosion führt.
In der Medizin dient es als Treibgas für Dosieraerosole, zum Beispiel bei einer Reihe von Arzneimitteln mit Wirkstoffen wie Salbutamol oder Fluticason.
Zukunft
Seit 2011 verbietet eine EU-Richtlinie den Einsatz von FKWs mit einem Treibhauspotential größer 150 (dazu zählt auch R-134a) in Klimaanlagen von Autos mit neuer Typenzulassung. Von 2017 an dürfen keine Neufahrzeuge mit solchen Kältemitteln mehr verkauft werden.[9][10] In Zukunft sollen stattdessen nicht oder wenig klimawirksame Kältemittel wie z. B. Kohlendioxid (R-744), Ammoniak, Propan (R-290) oder 2,3,3,3-Tetrafluorpropen (R1234yf) zum Einsatz kommen.
Weblinks
- Sicherheitsdatenblatt Tetrafluorethan (R134a) bei Air Liquide
Einzelnachweise
- Eintrag zu HYDROFLUOROCARBON 134A in der CosIng-Datenbank der EU-Kommission, abgerufen am 17. Dezember 2019.
- Eintrag zu 1,1,1,2-Tetrafluorethan in der GESTIS-Stoffdatenbank des IFA, abgerufen am 3. Januar 2022. (JavaScript erforderlich)
- Datenblatt Kältemittel R134a bei Agatex, abgerufen am 19. März 2018.
- Schweizerische Unfallversicherungsanstalt (Suva): Grenzwerte – Aktuelle MAK- und BAT-Werte (Suche nach 811-97-2 bzw. 1,1,1,2-Tetrafluorethan), abgerufen am 14. Mai 2020.
- G. Myhre, D. Shindell et al.: Climate Change 2013: The Physical Science Basis. Working Group I contribution to the IPCC Fifth Assessment Report. Hrsg.: Intergovernmental Panel on Climate Change. 2013, Chapter 8: Anthropogenic and Natural Radiative Forcing, S. 24–39; Table 8.SM.16 (ipcc.ch [PDF]).
- E.H. Christoph: Bilanzierung und Biomonitoring von Trifluoracetat und anderen Halogenacetaten, Dissertation, 2002, Universität Bayreuth
- Forster, P.; et al. (2007). Changes in Atmospheric Constituents and in Radiative Forcing.. Climate Change 2007: The Physical Science Basis. Contribution of Working Group I to the Fourth Assessment Report of the Intergovernmental Panel on Climate Change. Tabelle S. 212
- heise.de: Klimaanlagen spalten europäische Autohersteller, 24. Januar 2008.
- Richtlinie 2006/40/EG vom 17. Mai 2006 (PDF).
- Umweltbundesamt: Autoklimaanlagen mit fluorierten Kältemitteln, abgerufen am 25. März 2018.
