Vericiguat
Vericiguat ist ein Arzneistoff aus der Gruppe der sGC-Stimulatoren, der in der Behandlung der Herzinsuffizienz mit verminderter Auswurfleistung (englisch Heart Failure with reduced Ejection Fraction, HFrEF) eingesetzt wird.
| Strukturformel | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
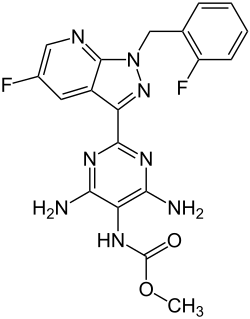 | ||||||||||||||||||||||
| Allgemeines | ||||||||||||||||||||||
| Freiname | Vericiguat | |||||||||||||||||||||
| Andere Namen |
| |||||||||||||||||||||
| Summenformel | C19H16F2N8O2 | |||||||||||||||||||||
| Kurzbeschreibung |
Weißes bis gelbliches Pulver[1] | |||||||||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Arzneistoffangaben | ||||||||||||||||||||||
| ATC-Code |
C01DX22 | |||||||||||||||||||||
| Wirkstoffklasse |
Vasodilatator | |||||||||||||||||||||
| Wirkmechanismus |
sGC-Stimulation | |||||||||||||||||||||
| Eigenschaften | ||||||||||||||||||||||
| Molare Masse | 426,38 g·mol−1 | |||||||||||||||||||||
| Löslichkeit |
| |||||||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||||||||
Wirkungsmechanismus
Vericiguat ist ein Stimulator der löslichen Guanylatcyclase (sGC), einem wichtigen Enzym im Stickstoffmonoxid-Signalweg. Wenn Stickstoffmonoxid (NO) an sGC bindet, katalysiert das Enzym die Synthese von intrazellulärem cyclischem Guanosinmonophosphat (cGMP), einem zweiten Botenstoff, der eine Rolle bei der Regulierung des Gefäßtonus, der Herzkontraktilität und dem kardialen Remodeling spielt. Herzinsuffizienz ist mit einer beeinträchtigten NO-Synthese und einer verminderten Aktivität von sGC verbunden, was zu einer myokardialen und vaskulären Fehlfunktion beitragen kann. Durch die direkte Stimulierung von sGC, unabhängig von und synergistisch mit NO, erhöht Vericiguat die intrazellulären cGMP-Spiegel, was zu einer Relaxation und Vasodilatation der glatten Muskulatur führt.[1]
Zulassung
Vericiguat wurde gemeinsam von den beiden Pharmaunternehmen Bayer und MSD entwickelt und erstmals als Verquvo im Januar 2021 in den USA zugelassen. Die Anwendung erfolgt peroral (als Tablette).[3]
Es wird in den USA vom Pharmaunternehmen MSD vermarktet, in allen übrigen Ländern liegen die Vermarktungsrechte bei Bayer. Im Juli 2021 hat die Europäische Kommission die Marktzulassung für Vericiguat unter dem Markennamen Verquvo in der Europäischen Union (EU) erteilt.[4][5]
Nebenwirkungen und Anwendungsbeschränkungen
Als häufige Nebenwirkungen wurden niedriger Blutdruck und niedrige Anzahl roter Blutkörperchen (Anämie) beobachtet.
Vericiguat darf nicht in der Schwangerschaft gegeben werden, da die Substanz embryo- und fetotoxisch ist. Während der Anwendung und bis zu einem Monat nach Therapieende muss eine zuverlässige Schwangerschaftsverhütung betrieben werden.[1]
Studien
Vericiguat wurde in einer randomisierten, placebokontrollierten, multizentrischen, doppelblinden Studie (VICTORIA, Vericiguat global study in patients with heart failure with reduced ejection fraction[6]) untersucht an 5050 Patienten mit chronischer Herzinsuffizienz und verminderter Auswurfleistung (weniger als 45 %), bei denen sich die Erkrankung weiter verschlechterte. Das Risiko für eine kardiovaskuläre Sterblichkeit und Krankenhauseinweisung konnte auf der Grundlage einer Time-to-Event-Analyse unter Vericiguat gegenüber Placebo statistisch signifikant gesenkt werden.[1]
Einzelnachweise
- Verquvo, Prescibing Information, FDA, Januar 2021.
- selleckchem.com: MSDS Vericiguat, abgerufen am 7. April 2021.
- Drug Trials Snapshot: VERQUVO, abgerufen am 6. April 2021.
- Verquvo® (Vericiguat) von Bayer in der EU zugelassen zur Behandlung der symptomatischen, chronischen Herzinsuffizienz. In: bayer.de. 21. Juli 2021, abgerufen am 22. Juli 2021.
- Grünes Licht für Bayer, In: Frankfurter Allgemeine Zeitung vom 22. Juli 2021
- D. Hüttmann: Arzneistoffkandidat wirksam bei chronischer Herzinsuffizienz, Pharmazeutische Zeitung, 19. November 2019.