Vadadustat
Vadadustat ist ein HIF-Prolyl-Hydroxylase-Inhibitor, der die Produktion von Hämoglobin und Erythrozyten stimuliert.[3][4] In Phase-III-Studien wird geprüft, ob das Medikament für die Behandlung von Anämien infolge chronischer Nierenerkrankungen geeignet ist. Eine Zulassung als Medikament besteht derzeit nicht (Stand: 2. Mai 2021).
| Strukturformel | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
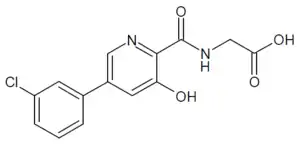 | ||||||||||||||||||||||
| Allgemeines | ||||||||||||||||||||||
| Freiname | Vadadustat | |||||||||||||||||||||
| Andere Namen |
| |||||||||||||||||||||
| Summenformel | C14H11ClN2O4 | |||||||||||||||||||||
| Kurzbeschreibung |
weißes bis grau-weißes Pulver[1] | |||||||||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Arzneistoffangaben | ||||||||||||||||||||||
| Wirkstoffklasse |
HIF-Prolyl-Hydroxylase-Inhibitor | |||||||||||||||||||||
| Wirkmechanismus |
Steigerung der Erythrozytenbildung | |||||||||||||||||||||
| Eigenschaften | ||||||||||||||||||||||
| Molare Masse | 306,70 g·mol−1 | |||||||||||||||||||||
| Löslichkeit | ||||||||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||||||||
Mechanismus
Der Hypoxie-induzierte Faktor (HIF, englisch Hypoxia-inducible factor) ist ein Transkriptionsfaktor der verschiedene physiologische Reaktionen auf eine Hypoxie reguliert. Insbesondere erhöht er die Produktion von Erythropoietin in der Leber und den Nieren. Erythropoietin erhöht die Produktion von Hämoglobin und Erythrozyten und verbessert so die Sauerstoffversorgung des Gewebes. Die Konzentration von HIF wird durch die Abbaugeschwindigkeit von HIF reguliert. Unter normalen Sauerstoffbedingungen wird HIF an zwei hoch konservierten Propyl-Resten hydroxyliert. Die Hydroxylierung erfolgt durch Sauerstoff-abhängige Prolyl-Hydroxylasen der PHD-Familie, die als Sauerstoff-Sensoren dienen. Die Hydroxylierung von HIF ermöglicht die Bindung an pHVL, das von Hippel-Lindau-Tumorsuppressor-Protein. pHVL ist Teil des Ubiquitin-Ligase-Komplexes. Die Ubiquierierung führt zu einem Abbau von HIF in den Proteasomen. Ein niedriger HIF-Spiegel vermindert die Produktion von Erythropoietin und damit der roten Blutkörperchen. Bei Sauerstoffmangel ist die Prolyl-Hydroxylase nicht aktiv, der Spiegel an HIF steigt und es werden mehr rote Blutkörperchen gebildet.[5] Das gleiche geschieht, wenn die Prolyl-Hydroxylase durch Vadadustat medikamentös gehemmt wird. Das Medikament täuscht also einen Sauerstoffmangel vor und fördert so die Bildung roter Blutkörperchen.[6]
HIF-PH-Inhibitoren
Gegenwärtig sind vier HIF-PH-Inhibitoren in Entwicklung. Alle sind oral verfügbar und zielen insbesondere auf Anämien, die durch eine Niereninsuffizienz ausgelöst sind.
| Freiname | INN | Plasma-Halbwertszeit / h | Anwendung | Status | Bemerkungen |
|---|---|---|---|---|---|
| Roxadustat | FG-4592 | 12–13 | 3× / Woche oral | Phase 3 | In einigen Ländern zugelassen[7] |
| Vadadustat | AKB-6548 | 4.5 | 1× täglich oral | Phase 3 | |
| Daprodustat | GSK-1278863 | 4 | 1× täglich oral | Phase 2 (US), Phase 3 (Japan) | |
| Molidustat | BAY 85-3934 | ? | 1× täglich oral | Phase 2 |
Anwendung von Vadadustat
Die Anfangsdosis beträgt 300 mg einmal täglich oral. In Abhängigkeit von der Erreichung des angestrebten Hämoglobinwertes (zum Beispiel 10–11 g / 100 ml) wird die Dosis auf 150 mg, 450 oder 600 mg angepasst.[6]
Ergebnisse bei Niereninsuffizienz
Bei Patienten mit Niereninsuffizienz tritt mit und ohne Dialyse häufig eine Anämie auf. Diese wird bisher mit Erythropoietin-Analoga behandelt. Dabei wurde ein Anstieg von Thrombosen, Herzinfarkten und Schlaganfällen beobachtet.[9] In vier Phase-III-Studien wurde daher nicht nur die Wirkung von Erythropoietin-Analoga mit Vadadustat verglichen, sondern auch die Rate der Nebenwirkungen. Unter MACE (major adverse cardiovascular event) wurden die Ereignisse: Tod jeglicher Ursache, nicht tödlicher Herzinfarkt oder Schlaganfall zusammengefasst.
| Studienname | Patienten | Teilstudie | Zahl | Wirksamkeit | MACE | Bemerkungen |
|---|---|---|---|---|---|---|
| PAO2TECT[10][6] | Niereninsuffizienz ohne Dialyse | 1. Teilstudie: keine Vorbehandlung mit Epo-Analoga 2. Teilstudie: Vorbehandlung mit Epo-Analoga |
3490 Patienten | kein Unterschied | MACE höher bei Vadadustat als bei Darbepoetin alfa | MACE insbesondere außerhalb der USA höher |
| INNO2VATE[11] | Niereninsuffizienz mit Dialyse | 1. Teilstudie: neu aufgetretene Niereninsuffizienz mit Dialyse 2. Teilstudie: bestehende Niereninsuffizienz mit Dialyse |
3923 Patienten | kein Unterschied | kein Unterschied |
In allen vier Studien erfolgte eine Randomisierung Vadadustat versus Darbepoetin alfa. Die Patienten waren mindestens 18 Jahre alt. Außer der Niereninsuffizienz durfte kein anderer Grund für die Anämie bestehen. Der Ferritinspiegel musste mindestens 10 ng / ml betragen, die Transferrin-Sättigung mindestens 20 %. Es sollte kein größeres Gefäßereignis vorausgehen.
Siehe auch
- Daprodustat
- Desidustat
- Molidustat
- Roxadustat
Einzelnachweise
- Vadadustat ( AKB-6548 ). Sun-shine Chemical, 2020, abgerufen am 16. Mai 2021 (englisch).
- Caymanchem: MSDS, abgerufen am 3. Mai 2021.
- PE Pergola, BS Spinowitz, CS Hartman, BJ Maroni, VH Haase: Vadadustat, a novel oral HIF stabilizer, provides effective anemia treatment in nondialysis-dependent chronic kidney disease. In: Kidney International. Band 90, Nr. 5, November 2016, S. 1115–1122, doi:10.1016/j.kint.2016.07.019, PMID 27650732.
- ER Martin, MT SmithT, BJ Maroni, QC Zuraw, EM deGoma: Clinical Trial of Vadadustat in Patients with Anemia Secondary to Stage 3 or 4 Chronic Kidney Disease. In: American Journal of Nephrology. Band 45, Nr. 5, 2017, S. 380–388, doi:10.1159/000464476, PMID 28343225, PMC 5452283 (freier Volltext).
- William G. Kaelin, Peter J. Ratcliffe: Oxygen Sensing by Metazoans: The Central Role of the HIF Hydroxylase Pathway. In: Molecular Cell. Band 30, Nr. 4, Mai 2008, S. 393–402, doi:10.1016/j.molcel.2008.04.009.
- Glenn M. Chertow, Pablo E. Pergola, Youssef M.K. Farag, Rajiv Agarwal, Susan Arnold: Vadadustat in Patients with Anemia and Non–Dialysis-Dependent CKD. In: New England Journal of Medicine. Band 384, Nr. 17, 29. April 2021, ISSN 0028-4793, S. 1589–1600, doi:10.1056/NEJMoa2035938.
- Adeera Levin: Therapy for Anemia in Chronic Kidney Disease — New Interventions and New Questions. In: New England Journal of Medicine. Band 384, Nr. 17, 29. April 2021, ISSN 0028-4793, S. 1657–1658, doi:10.1056/NEJMe2103937.
- Nupur Gupta, Jay B. Wish: Hypoxia-Inducible Factor Prolyl Hydroxylase Inhibitors: A Potential New Treatment for Anemia in Patients With CKD. In: American Journal of Kidney Diseases. Band 69, Nr. 6, Juni 2017, S. 815–826, doi:10.1053/j.ajkd.2016.12.011.
- Marc A. Pfeffer, Emmanuel A. Burdmann, Chao-Yin Chen, Mark E. Cooper, Dick de Zeeuw: A Trial of Darbepoetin Alfa in Type 2 Diabetes and Chronic Kidney Disease. In: New England Journal of Medicine. Band 361, Nr. 21, 19. November 2009, ISSN 0028-4793, S. 2019–2032, doi:10.1056/NEJMoa0907845.
- Glenn M. Chertow, Pablo E. Pergola, Rajiv Agarwal, Geoffrey A. Block, Youssef M.K. Farag: Cardiovascular safety and efficacy of vadadustat for the treatment of anemia in non-dialysis-dependent CKD: Design and baseline characteristics. In: American Heart Journal. Band 235, Mai 2021, S. 1–11, doi:10.1016/j.ahj.2020.10.068.
- Kai-Uwe Eckardt, Rajiv Agarwal, Ahmad Aswad, Ahmed Awad, Geoffrey A. Block: Safety and Efficacy of Vadadustat for Anemia in Patients Undergoing Dialysis. In: New England Journal of Medicine. Band 384, Nr. 17, 29. April 2021, ISSN 0028-4793, S. 1601–1612, doi:10.1056/NEJMoa2025956.