Trimethylzinnchlorid
Trimethylzinnchlorid ist eine chemische Verbindung aus der Gruppe derTrimethylzinn-Verbindungen die zu den zinnorganischen Verbindungen gehören.
| Strukturformel | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
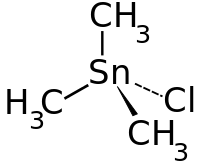 | ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | Trimethylzinnchlorid | |||||||||||||||
| Andere Namen |
| |||||||||||||||
| Summenformel | C3H9ClSn | |||||||||||||||
| Kurzbeschreibung |
weiß[1] | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 199,27 g·mol−1 | |||||||||||||||
| Aggregatzustand |
fest, kristallin[1] | |||||||||||||||
| Dichte |
1,65 g·cm−3 (20 °C)[2] | |||||||||||||||
| Schmelzpunkt | ||||||||||||||||
| Siedepunkt |
154 °C[3] | |||||||||||||||
| Dampfdruck | ||||||||||||||||
| Löslichkeit |
löslich in Wasser: 93,3 g·l−1[2] | |||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| MAK |
0,001 ml·m−3, 0,005 mg·m−3[3] | |||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||
Gewinnung und Darstellung
Trimethylzinnchlorid kann durch Umsetzung von Tetramethylzinn mit Chlorwasserstoff hergestellt werden:[4]
Eigenschaften
Physikalische Eigenschaften
Trimethylzinnchlorid ist ein weißer, brennbarer Feststoff mit einem Flammpunkt von 97 °C, der sich in Wasser langsam zersetzt.[1][3] Es hat in Benzol ein Dipolmoment von 3,46 Debye.[5]
Chemische Eigenschaften/Verwendung
Da der Chlorid-Ligand sehr reaktiv ist und leicht ersetzt werden kann, ist Trimethylzinnchlorid ein Ausgangsstoff zur Herstellung anderer Trimethylzinn-Verbindungen. So kann durch Reduktion von Trimethylzinnchlorid mit einem geeigneten Reduktionsmittel (z. B. Lithiumaluminiumhydrid) Trimethylzinnhydrid gewonnen werden:[4]
Die Umsetzung mit Lithiumalkylen liefert unter Bildung von Lithiumchlorid das entsprechende Trimethylalkylzinn:[4]
Sicherheitshinweise/Toxizität
Trimethylzinnchlorid ist wie viele andere organische Zinnverbindungen als giftig eingestuft und muss daher mit entsprechender Vorsicht gehandhabt werden. Die toxischen Wirkung zielt insbesondere auf die Nieren und das zentrale Nervensystem, in höherer Dosis auch auf Leber, Nebennieren, Thymus, Milz, Harnblase, Hoden und Nebenhoden.[2]
- Toxizität gegenüber Fischen: LC50 Oryzias latipes (48 h) 5,62 mg·l−1[1]
- Toxizität gegenüber wirbellosen Wassertieren: EC50 Daphnia magna (24 h) 0,47 mg·l−1[1]
- Toxizität gegenüber Algen: Wachstumshemmung EC50 Skeletonema costatum (72 h) 0,214 mg·l−1[1]
- Toxizität gegenüber Säugetieren: LD50 oral, Ratte 1,26 mg·kg−1[3]
- Bioakkumulationspotential: Cyprinodon sp. (Kärpfling) (45 d) 10 μg·l−1[1]
Einzelnachweise
- Datenblatt Trimethyltin chloride bei Sigma-Aldrich, abgerufen am 1. Mai 2015 (PDF).
- Methylzinnverbindungen. In: DFG (Hrsg.): The MAK Collection for Occupational Health and Safety. 2014, S. 13, doi:10.1002/3527600418.mb744031metd0056.
- Eintrag zu Trimethylzinnchlorid in der GESTIS-Stoffdatenbank des IFA, abgerufen am 1. Februar 2016. (JavaScript erforderlich)
- Didier Astruc: Organometallic Chemistry and Catalysis. Springer Science & Business Media, 2007, ISBN 978-3-540-46129-6, S. 336 (eingeschränkte Vorschau in der Google-Buchsuche).
- Jörg Lorberth, Heinrich Nöth: Dipolmomente einiger Organozinnchloride. In: Chemische Berichte. Band 98, Nr. 3, März 1965, S. 969–976, doi:10.1002/cber.19650980342.

