Lactoferrin
Lactoferrin (genauer: Lactotransferrin, aus lateinisch lacteus ‚Milch‘ und lat. ferrum ‚Eisen‘ und lat. transferre ‚hinübertragen‘) ist ein in Säugetieren vorkommendes Protein mit multifunktionalen[1] Enzymaktivitäten.
| Lactoferrin | ||
|---|---|---|
| ||
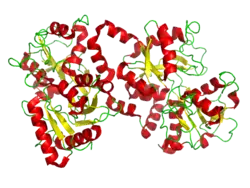
| Bändermodell nach PDB 1B0L | ||
|
Vorhandene Strukturdaten: 1B0L, 1BKA, 1CB6, 1DSN, 1EH3, 1FCK, 1H43, 1H44, 1H45, 1HSE, 1L5T, 1LCF, 1LCT, 1LFG, 1LFH, 1LFI, 1LGB, 1N76, 1SQY, 1U62, 1VFD, 1VFE, 1XV4, 1XV7, 1Z6V, 1Z6W, 2BJJ, 2DP4, 2GMC, 2GMD, 2HD4, 2PMS | ||
| Eigenschaften des menschlichen Proteins | ||
| Masse/Länge Primärstruktur | 691 Aminosäuren | |
| Bezeichner | ||
| Gen-Namen | LTF GIG12; HEL110; HLF2; LF | |
| Externe IDs | ||
| Enzymklassifikation | ||
| EC, Kategorie | 3.4.21.-, Serinprotease | |
| MEROPS | S60.001 | |
| Reaktionsart | Spaltung einer Peptidbindung | |
| Substrat | X-Arg-Ser-Arg-Arg-*-Y oder X-Arg-Arg-Ser-Arg-*-Y | |
| Produkte | Y + X-Arg-Ser-Arg-Arg oder X-Arg-Arg-Ser-Arg | |
| Vorkommen | ||
| Homologie-Familie | Transferrin | |
| Übergeordnetes Taxon | Euteleostomi | |
| Orthologe | ||
| Mensch | Hausmaus | |
| Entrez | 4057 | 17002 |
| Ensembl | ENSG00000012223 | ENSMUSG00000032496 |
| UniProt | P02788 | P08071 |
| Refseq (mRNA) | NM_001199149 | NM_008522 |
| Refseq (Protein) | NP_001186078 | NP_032548 |
| Genlocus | Chr 3: 46.44 – 46.49 Mb | Chr 9: 111.02 – 111.04 Mb |
| PubMed-Suche | 4057 | 17002 |
Evolution
Lactoferrin gehört zur Proteinfamilie der Transferrine.[2][3] Transferrine kommen nicht nur bei Säugetieren vor, homologe Gene finden sich auch bei anderen Wirbeltieren und Wirbellosen.[2][4]
Eigenschaften und Vorkommen
Lactoferrin besitzt sowohl antivirale[5], als auch antimikrobielle[6] Eigenschaften. Es fungiert einerseits als Peptidase (Spaltung von Peptiden), weshalb es der Gruppe der Serinproteasen zugeordnet wird, aber auch als eisen-bindendes Protein – ähnlich dem Transferrin – und zeigt zusätzlich Desoxyribonuklease-[7] und Ribonuklease-Aktivitäten[8], womit es den Nukleasen (EC 3.1.21.1) zugerechnet wird. Außerdem ist es ein starker Inhibitor für Tryptase.[9]
Lactoferrin ist in vielen Körperflüssigkeiten[10] der Säugetiere, in deren Milch,[6][11][12] Tränen,[6] Speichel,[6] Schweiß,[6] Vaginalsekret,[13] Seminalplasma,[14] Nasen- und Bronchialsekret[9] sowie anderen Sekreten zu finden. Außerdem ist es in weißen Blutkörperchen lokalisiert.[15][16]
Schon kleine Mengen entfalten enorme biologische Aktivität. Ein Liter Kuhmilch enthält 0,1 g Lactoferrin. Es ist nur zu einem geringen Teil mit Eisen gesättigt und kann mehr als das Fünffache seiner ursprünglichen Eisenladung binden.
Außerdem beeinflusst es die Zellteilung und stimuliert das Zellwachstum. Es entfaltet auch immunologische Wirkungen, indem es das Wachstum von Lymphozyten fördert.
Antibakterielle Schutzfunktion
Vom Organismus wird Lactoferrin eingesetzt, um Bakterien das lebensnotwendige Eisen zu entziehen. Da Bakterien essentiell auf Eisen angewiesen sind, wirkt die Eisenverarmung antibakteriell. Als Protease ist Lactoferrin in der Lage, mehrere für die Besiedlung wichtige Proteine des Krankheitserregers Haemophilus influenzae zu zerstören. Insbesondere die in der menschlichen Muttermilch vorkommende Konzentration an Lactoferrin kann die bei Kleinkindern oft auftretenden Atemwegsinfektionen mit diesem Keim verhindern. Außerdem beeinträchtigt es in Shigella und pathogenen Escherichia coli das Typ III-Sekretionssystem. Von Leukozyten freigesetzt, ist es so auch Teil des Immunsystems.[17][18][19][20]
Virale Interaktionen
Infektionen mit HTLV-1 über Muttermilch[21] oder Seminalplasma[22] werden durch Lactoferrin begünstigt. Auf der anderen Seite kann das Protein die Replikation des HIV-1 verhindern.[23]
Verwendung
Mehrere Untersuchungen zu Beginn des 21. Jahrhunderts zeigen bemerkenswerte Ergebnisse bei der Behandlung chronischer Parodontitis.[24]
Wegen seines breiten Wirkspektrums ist die pharmazeutische Industrie an diesem Protein interessiert. Industriell wird es aus Milch und Molke isoliert. Es wird in Baby- und Sportlernahrung, sowie in Kosmetika, Kaugummis und Functional Foods eingesetzt.
Wie eine Studie des Journal of the American Medical Association aus dem Jahr 2009 zeigte, kann die Gabe von Lactoferrin an Neugeborene mit Untergewicht (< 1500 g Geburtsgewicht) das Auftreten einer Sepsis sowie die Sepsis-assoziierte Mortalität signifikant und klinisch relevant senken.[25]
Literatur
- Lönnerdal B: Nutritional roles of lactoferrin. In: Curr Opin Clin Nutr Metab Care. 12, Nr. 3, Mai 2009, S. 293–7. doi:10.1097/MCO.0b013e328328d13e. PMID 19318940.
Einzelnachweise
- Ward PP, Paz E, Conneely OM: Multifunctional roles of lactoferrin: a critical overview. In: Cell. Mol. Life Sci.. 62, Nr. 22, November 2005, S. 2540–8. doi:10.1007/s00018-005-5369-8. PMID 16261256.
- John Williams: The evolution of transferrin. In: Trends in Biochemical Sciences. 7, 1982, S. 394–397, doi:10.1016/0968-0004(82)90183-9.
- Guo Ming Liang, Xun Ping Jiang: Positive selection drives lactoferrin evolution in mammals. In: Genetica. 138, 2010, S. 757–762, doi:10.1007/s10709-010-9456-x.
- Ciuraszkiewicz, Justyna et al.: Reptilian transferrins: evolution of disulphide bridges and conservation of iron-binding center. Gene, Band 396, Nr. 1, 2007, S. 28–38, doi:10.1016/j.gene.2007.02.018
- M. C. Harmsen, et al.: Antiviral Effects of Plasma and Milk Proteins: Lactoferrin Shows Potent Activity against Both Human Immunodeficiency Virus and Human Cytomegalovirus Replication In Vitro. In: Journal of Infectious Diseases. 172, 1995, S. 380–388, doi:10.1093/infdis/172.2.380.
- J. H. Park, G. T. Park, I. H. Cho, S. M. Sim, J. M. Yang, D. Y. Lee: An antimicrobial protein, lactoferrin exists in the sweat: proteomic analysis of sweat. In: Experimental Dermatology. Band 20, Nummer 4, April 2011, ISSN 1600-0625, S. 369–371, doi:10.1111/j.1600-0625.2010.01218.x, PMID 21366701
- Bennett, R. M., J. Davis: Lactoferrin interacts with deoxyribonucleic acid: a preferential reactivity with double-stranded DNA and dissociation of DNA-anti-DNA complexes. The Journal of Laboratory and Clinical Medicine, Band 99, Nr. 1, 1982, S. 127, PMID 6274982.
- Furmanski, Philip, et al.: Multiple molecular forms of human lactoferrin. Identification of a class of lactoferrins that possess ribonuclease activity and lack iron- binding capacity. In: Journal of Experimental Medicine. 170, 1989, S. 415–429, doi:10.1084/jem.170.2.415.
- Elrod, Kyle C., et al.: Lactoferrin, a Potent Tryptase Inhibitor, Abolishes Late-Phase Airway Responses in Allergic Sheep. In: American Journal of Respiratory and Critical Care Medicine. 156, 1997, S. 375–381, doi:10.1164/ajrccm.156.2.9607012.
- P.L. Masson, J.F. Heremans, C.H. Dive: An iron-binding protein common to many external secretions. In: Clinica Chimica Acta. 14, 1966, S. 735–739, doi:10.1016/0009-8981(66)90004-0.
- Neville, Margaret C. et al.: Lactoferrin secretion into mouse milk. Advances in Lactoferrin Research. Plenum Press, New York (1998), S. 141–153.
- Neville, M. C., P. Zhang: Lactoferrin secretion into milk: comparison between ruminant, murine, and human milk. (Seite nicht mehr abrufbar, Suche in Webarchiven) Info: Der Link wurde automatisch als defekt markiert. Bitte prüfe den Link gemäß Anleitung und entferne dann diesen Hinweis. (PDF; 1,4 MB) Journal of Animal Science, Band 78, Suppl 3, 2000, S. 26–35.
- Cohen, M. S. et al.: Preliminary observations on lactoferrin secretion in human vaginal mucus: variation during the menstrual cycle, evidence of hormonal regulation, and implications for infection with Neisseria gonorrhoeae. American Journal of Obstetrics and Gynecology, Band 157, Nr. 5, 1987, S. 1122–1125.
- W. M. Buckett, M. J. Luckas, M. R. Gazvani, I. A. Aird, D. I. Lewis-Jones: Seminal plasma lactoferrin concentrations in normal and abnormal semen samples. In: Journal of andrology. Band 18, Nummer 3, 1997 May-Jun, ISSN 0196-3635, S. 302–304, PMID 9203059.
- Legrand D, Pierce A, Elass E, Carpentier M, Mariller C, Mazurier J: Lactoferrin structure and functions. In: Adv. Exp. Med. Biol.. 606, 2008, S. 163–94. PMID 18183929.
- Anderson BF, Baker HM, Dodson EJ, et al: Structure of human lactoferrin at 3.2-A resolution. In: Proc. Natl. Acad. Sci. U.S.A.. 84, Nr. 7, April 1987, S. 1769–73. PMID 3470756. PMC 304522 (freier Volltext).
- Andrew G Plaut, Jiazhou Qiu, Joseph W St. Geme: Human lactoferrin proteolytic activity: analysis of the cleaved region in the IgA protease of Haemophilus influenzae. In: Vaccine. 19, 2000, S. S148–S152, doi:10.1016/S0264-410X(00)00296-6.
- Qiu J, Hendrixson DR, Baker EN, Murphy TF, St Geme JW, Plaut AG: Human milk lactoferrin inactivates two putative colonization factors expressed by Haemophilus influenzae. In: Proc. Natl. Acad. Sci. U.S.A.. 95, Nr. 21, Oktober 1998, S. 12641–6. PMID 9770539. PMC 22884 (freier Volltext).
- Hendrixson DR, Qiu J, Shewry SC, et al: Human milk lactoferrin is a serine protease that cleaves Haemophilus surface proteins at arginine-rich sites. In: Mol. Microbiol.. 47, Nr. 3, Februar 2003, S. 607–17. PMID 12535064.
- Ochoa TJ, Clearly TG: Lactoferrin disruption of bacterial type III secretion systems. In: Biometals. 17, Nr. 3, Juni 2004, S. 257–60. PMID 15222474.
- Moriuchi, Masako, and Hiroyuki Moriuchi: Induction of lactoferrin gene expression in myeloid or mammary gland cells by human T-cell leukemia virus type 1 (HTLV-1) tax: implications for milk-borne transmission of HTLV-1. Journal of Virology, Band 80, Nr. 14, 2006, S. 7118–7126.
- Moriuchi, Masako, Hiroyuki Moriuchi: Seminal fluid enhances replication of human T-cell leukemia virus type 1: implications for sexual transmission. Journal of Virology, Band 78, Nr. 22, 2004, S. 12709–12711.
- Moriuchi M, Moriuchi H: A milk protein lactoferrin enhances human T cell leukemia virus type I and suppresses HIV-1 infection. In: J. Immunol.. 166, Nr. 6, März 2001, S. 4231–6. PMID 11238676.
- F. Berlutti, A. Pilloni u. a.: Lactoferrin and oral diseases: current status and perspective in periodontitis. In: Annali di stomatologia. Band 2, Nummer 3–4, März 2011, ISSN 1824-0852, S. 10–18, PMID 22545184, PMC 3314318 (freier Volltext).
- Manzoni P, Rinaldi M, Cattani S, et al.: Bovine lactoferrin supplementation for prevention of late-onset sepsis in very low-birth-weight neonates: a randomized trial. In: JAMA. 302, Nr. 13, Oktober 2009, S. 1421–1428. doi:10.1001/jama.2009.1403. PMID 19809023.