Tenoxicam
Tenoxicam ist ein nichtsteroidales Antirheumatikum (NSAR) aus der Gruppe der Oxicame mit analgetischen, antiphlogistischen und antipyretischen Eigenschaften. Es ist zur oralen, rektalen und intravenösen Gabe vorgesehen und wird unter anderem bei Schmerzen des rheumatoiden Formenkreises, Osteoarthritis, Spondylitis ankylosans, Sehnenentzündung, Morbus Bechterew, posttraumatischen Schmerzen, Schleimbeutelentzündung, Tendinitis, Frozen Shoulder, Zerrungen und Verstauchungen oder akuter Gicht eingesetzt.[7]
| Strukturformel | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
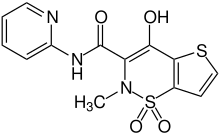 | ||||||||||||||||||||||
| Allgemeines | ||||||||||||||||||||||
| Freiname | Tenoxicam | |||||||||||||||||||||
| Andere Namen | ||||||||||||||||||||||
| Summenformel | C13H11N3O4S2 | |||||||||||||||||||||
| Kurzbeschreibung |
gelbes, kristallines Pulver[1] | |||||||||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Arzneistoffangaben | ||||||||||||||||||||||
| ATC-Code |
M01AC02 | |||||||||||||||||||||
| Wirkstoffklasse | ||||||||||||||||||||||
| Wirkmechanismus | ||||||||||||||||||||||
| Eigenschaften | ||||||||||||||||||||||
| Molare Masse | 337,37 g·mol−1 | |||||||||||||||||||||
| Aggregatzustand |
fest | |||||||||||||||||||||
| Schmelzpunkt | ||||||||||||||||||||||
| pKS-Wert |
4,78[3] | |||||||||||||||||||||
| Löslichkeit |
sehr gering in Wasser (14,1 mg·l−1)[4] | |||||||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Toxikologische Daten | ||||||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||||||||
Geschichte
Es wurde 1976 durch Hoffmann-La Roche patentiert, als Erfinder gelten Rudolf Pfister, Paul Zeller, Dieter Binder und Otto Hromatka.[8] In Europa wurde Tenoxicam 1982 in Frankreich eingeführt.[9] Kurz darauf begannen klinische Versuche für die Verwendung als Analgetika. In Deutschland war Tenoxicam als Analogwirkstoff zu Piroxicam zwischen 1987 und 2000 unter den Namen Liman und Tilcotil im Handel.[10]
Gewinnung
In der Literatur ist die Gewinnung ausgehend von einer Fiesselmann Thiophensynthese beschrieben.[11][12][13]
Eigenschaften
Die Keto-Enol-Tautomerie ist analog zum Derivat Lornoxicam.

Unter Standardbedingungen liegt Tenoxicam als gelbes, kristallines Pulver vor. Wie die meisten nichtsteroidalen Antiphlogistika ist es mit einem pKs von 4,78 eine schwache Säure.
Pharmakologie
Pharmakodynamik
Tenoxicam bewirkt eine Blockade der Prostaglandin-Synthese durch Hemmung von Cyclooxygenasen; es hemmt auch die Thrombozytenaggregation. Untersuchungen an Cyclooxygenase-Isoenzymen zeigten, dass Tenoxicam Cyclooxygenase-Isoenzyme im Verhältnis COX-2/COX-1 von 1,34 hemmt. Aus Versuchen mit Leukozytenperoxydase geht hervor, dass Tenoxicam am Entzündungsort als Radikalfänger wirkt.[7]
Pharmakokinetik
Der Wirkstoff wird in die Leber über Cytochrom P450 2C9 mit dem hauptsächlichen, inaktiven Metabolit 5-Hydroxy-tenoxicam bei einer absoluten Bioverfügbarkeit verstoffwechselt. Die maximalen Plasmakonzentrationen bei nüchterner Einnahme sind innerhalb der ersten zwei Stunden zu beobachten. Das Verteilungsvolumen liegt im Fließgleichgewicht im Mittel zwischen 10 und 11 Litern. Im Blut wird Tenoxicam zu mehr als 99 % an Albumin gebunden. Bis zu zwei Drittel werden im Urin ausgeschieden, der Rest über die Galle, hauptsächlich in Form glukuronidierter Verbindungen. Weniger als 1 % der verabreichten Dosis wird unverändert im Urin ausgeschieden.
Die Plasmahalbwertszeit liegt zwischen 49 und 81, im Mittel bei 72 Stunden.[14]
Die übliche Tagesdosis wird aufgrund der langsamen Verstoffwechslung einmal täglich eingenommen.[15] Obwohl die therapeutische Wirkung bald nach Behandlungsbeginn eintritt, nimmt sie während der ersten beiden Wochen weiterhin zu, bis die Plasmakonzentration das Fließgleichgewicht erreicht hat.
Klinische Angaben
Kontraindikationen
Im letzten Drittel der Schwangerschaft sollte kein Tenoxicam genommen werden. Weitere Gegenanzeigen sind Morbus Crohn, Colitis ulcerosa, schwere Leber-, Herz- oder Nierenfunktionsstörungen. Vor Narkosen oder chirurgischen Eingriffen sollen ältere Patienten, Kranke mit erhöhtem Risiko eines Nierenversagens sowie Patienten mit erhöhtem Blutungsrisiko das Mittel nicht erhalten, da wie bei allen NSAR das Risiko eines akuten Nierenversagens erhöht ist und die Möglichkeit von Hämostasestörungen besteht. Eine Kombinationsbehandlung mit Salicylaten oder anderen NSAR sollte wegen des erhöhten Risikos gastrointestinaler Nebenwirkungen vermieden werden.
Für Patienten unter 18 Jahren liegen noch zu wenig klinische Erfahrungen vor.[7]
Nebenwirkungen
Sehr häufig treten Magenschmerzen, Sodbrennen, Nausea, Diarrhö oder Verstopfung auf. Bei 1–2 % wurde auch Pruritus, Exanthem, Erythem, Urtikaria, Schwindel, Kopfschmerzen, Dyspepsie, Epigastrische und abdominelle Beschwerden oder ein Anstieg von Kreatinin, SGOT, SGPT oder Bilirubin beobachtet. Gelegentlich kommt es zu Ermüdungserscheinungen, Appetitlosigkeit, Schlafstörungen, Drehschwindel, Herzklopfen, Stomatitis, Gastritis, Erbrechen oder trockenem Mund. Selten bis sehr selten kann es zu einer Senkung der Hämoglobinwerte kommen, zu Anämie, Agranulozytose, Granulozytopenie, Leukopenie, Thrombozytopenie, leichten Ödemen, Photodermatose, gastrointestinalen Blutungen einschließlich Hämatemesis und Melaena, Ulzera, Überempfindlichkeitsreaktionen wie Dyspnoe, Asthma, Anaphylaxie, Angioödemen, Sehstörungen, Vasculitis, Lichtempfindlichkeit oder gastrointestinaler Perforation.
Die renalen Effekte der NSAR umfassen Flüssigkeitsretention mit Ödemen und/oder arterieller Hypertonie. Sehr selten können schwere, manchmal tödliche Hautreaktionen, einschließlich exfoliativer Dermatitis, Stevens-Johnson-Syndrom und toxischer epidermaler Nekrolyse auftreten. Die Anwendung von Tenoxicam kann die weibliche Fertilität beeinträchtigen und wird daher bei Frauen, die schwanger werden möchten nicht empfohlen.[7]
Wechselwirkungen
Bei gleichzeitiger Einnahme von Diuretika, Kortikosteroiden, Antikoagulantien vom Cumarin-Typ, selektiven Serotonin-Wiederaufnahmehemmern, Thrombozytenaggregationshemmern oder ACE-Hemmern ist Vorsicht geboten, die gleichzeitige Anwendung mit anderen nicht-steroidalen Entzündungshemmern, einschließlich COX-2-selektiver Inhibatoren, ist zu vermeiden.
Salicylate verdrängen Tenoxicam von den Proteinbindungsstellen und erhöhen damit das Verteilungsvolumen. Die gleichzeitige Anwendung von Methotrexat wurde mit reduzierter Sekretion der Nierentubuli, höheren Plasmakonzentrationen und schwerer Toxizität von Methotrexat in Verbindung gebracht. Plasmaspiegel sowie Toxizität von Lithium werden durch gleichzeitige Einnahme erhöht.
Handelsnamen
Tenoxicam wird allgemein als Monopräparat vertrieben.[15]
Handelsnamen: Dolmen (I), Rexalgan (I), Tilcotil (CH, B, I, J, TR), Tilko (TR), Vienoks (TR), Mobiflex (GB)
Siehe auch
Einzelnachweise
- Eintrag zu Tenoxicam bei ChemicalBook, abgerufen am 7. Juni 2021.
- Eintrag zu Tenoxicam. In: Römpp Online. Georg Thieme Verlag, abgerufen am 13. Februar 2016.
- Eintrag zu Tenoxicam in der Human Metabolome Database (HMDB), abgerufen am 19. Februar 2016.
- Eintrag zu Tenoxicam in der DrugBank der University of Alberta, abgerufen am 7. Juni 2021.
- Datenblatt Tenoxicam bei Sigma-Aldrich, abgerufen am 7. Juni 2021 (PDF).
- Eintrag zu Tenoxicam in der ChemIDplus-Datenbank der United States National Library of Medicine (NLM), abgerufen am 11. April 2016.
- Tilcotil. In: Arzneimittel-Kompendium der Schweiz; abgerufen im Februar 2016.
- Patentanmeldung DE2537070: Thiazine. Angemeldet am 20. August 1975, veröffentlicht am 18. März 1976, Anmelder: Hoffmann-La Roche Inc., Erfinder: Rudolf Pfister, Paul Zeller, Dieter Binder, Otto Hromatka.
- D Penso: Toxic epidermal necrolysis after oxicam use. In: Journal of the American Academy of Dermatology. 14, 1986, S. 275–6. doi:10.1016/s0190-9622(86)80342-5. PMID 3485122.
- Institut für Gesundheits- und Sozialforschung GmbH: Analog-Wirkstoffe im Arzneimittelmarkt: Therapeutischer Nutzen und Bedeutung für die Ausgaben der Krankenversicherungen (PDF; 1,2 MB) In: Strukturforschung im Gesundheitswesen, Band 30. Berlin 2001, ISBN 3-9808407-1-9, S. 138 f.; abgerufen am 26. Februar 2016.
- Dieter Binder, Otto Hromatka, Franz Geissler, Karl Schmied, Christian R. Noe, Kaspar Burri, Rudolf Pfister, Konrad Strub, Paul Zeller: Analogs and derivatives of tenoxicam. 1. Synthesis and antiinflammatory activities of analogs with different residues on the ring nitrogen and the amide nitrogen. In: Journal Med. Chem.. 30, April 1987, S. 678–682. doi:10.1021/jm00387a017.
- D. Binder, O. Hromatka, F. Geissler, K. Schmied, C. R. Noe, K. Burri, R. Pfister, K. Strub, P. Zeller: Analogues and derivatives of tenoxicam. 1. Synthesis and antiinflammatory activity of analogues with different residues on the ring nitrogen and the amide nitrogen. In: Journal of medicinal chemistry. Band 30, Nummer 4, April 1987, S. 678–682, PMID 3494124.
- Axel Kleemann, Jürgen Engel, Bernd Kutscher und Dietmar Reichert: Pharmaceutical Substances, 4. Auflage (2000), 2 Bände erschienen im Thieme-Verlag Stuttgart, ISBN 978-1-58890-031-9; seit 2003 online mit halbjährlichen Ergänzungen und Aktualisierungen.
- OG Nilsen: Clinical Pharmacokinetics of tenoxicam. In: Clin Pharmacokinet. 1, 1996, S. 16–43. PMID 8137596.
- Tenoxicam. Drugs.com International (englisch).