Siliciumtetrahalogenide
Als Siliciumtetrahalogenide, oder Tetrahalogensilane bezeichnet man Verbindungen des Siliciums mit den Halogenen Fluor, Chlor, Brom oder Iod vom Typ SiX4 (X=Halogen). Diese Halogensilane sind Derivate des Monosilans, wobei alle Wasserstoff-Atome durch Halogene ersetzt sind.[1] Es existieren von allen stabilen Halogeniden die reinen Tetrahalogensilane,[1] daneben sind auch gemischte Tetrahalogensilane bekannt.[2]
Darstellung
Die Synthese der Tetrahalogensilane kann aus den Elementen oder durch Umsetzung von Siliciumdioxid oder Silicium mit einem Überschuss Halogenwasserstoff erfolgen:[3][1][4]
Eigenschaften
Mit zunehmendem Molekulargewicht erhöhen sich Schmelz- und Siepunkte der Tetrahalogensilane: Unter Normalbedingungen liegt SiF4 als Gas vor, während es sich bei der Chlor- und Bromverbindung um Flüssigkeiten handelt. Das Iodid ist hingegen ein Feststoff.[1] Im Gegensatz zu ihren Kohlenstoffanaloga, den Halogenkohlenwasserstoffen vom Typ CX4, wie beispielsweise Tetrachlormethan, sind Tetrahalogensilane hochreaktive Verbindungen. Ihre Beständigkeit nimmt mit zunehmendem Molekulargewicht ab.[1]
| Tetrafluorsilan | Tetrachlorsilan | Tetrabromsilan | Tetraiodsilan | |
|---|---|---|---|---|
| Formel | SiF4 | SiCl4 | SiBr4 | SiI4 |
| Molare Masse | 104,1 g·mol−1 | 169,90 g·mol−1 | 347,72 g·mol−1 | 535,70 g·mol−1 |
| CAS | 7783-61-1 | 10026-04-7 | 7789-66-4 | 13465-84-4 |
| EG-Nummer | 232-015-5 | 233-054-0 | 232-182-4 | 236-706-2 |
| ECHA-Infocard | 100.029.104 | 100.030.037 | 100.029.257 | 100.033.355 |
| Aggregat | gasförmig[1] | flüssig[1] | flüssig[1] | fest[1] |
| Farbe | farblos[1] | |||
| Schmelzpunkt | −95,2 °C[5][Anm 1] | −70 °C[6] | 5 °C[7] | 120,5 °C[8] |
| Siedepunkt | 57 °C[6] | 154 °C[7] | 287,4 °C[8] | |
| Dichte | 4,372 kg·m−3 (15 °C)[5] | 1,48 g·cm−3[6] | 2,800 g·cm−3[7] | 4,198 g·cm−3 (25 °C)[8] |
| Brechungsindex | 1,41156 (25 °C)[9] | 1,5685 (31 °C)[9] | ||
| (kJ/mol) | −1615[1] | −663[1] | −415[1] | −110[1] |
| Si-X-Bindungslänge | 155 pm[1] | 209 pm[1] | 218 pm[1] | 243 pm[1] |
Anmerkungen:
- Sublimation
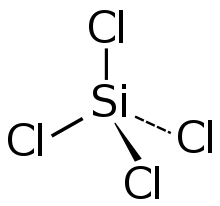
Die Tetrahalogensilane sind tetraedrisch aufgebaut. Durch den polaren Charakter ist die Si-X-Bindungslänge im SiF4 verkürzt (berechnet: 181 pm) und liegt zwischen einen Einfach- und einer Doppelbindung. Der Effekt auf die Bindungslänge nimmt zu den schwereren Halogenen hin ab (berechnet Si–Cl 216 pm, Si–Br 231 pm, Si–I 240 pm).[1]
Reaktionen
Die Silicium-Halogen-Bindung in Tetrahalogensilanen kann durch nukleophile Substitution leicht aufgespalten werden. Entsprechend sind Tetrahalogensilane sehr hydrolyseempfindlich und werden durch Wasser rasch in Kieselsäure umgewandelt.[1] Durch Umsetzung mit Alkoholen (Alkoholyse) entstehende die entsprechenden Alkoholate.[1]
Durch Umsetzung mit Alkoholen (Alkoholyse) entstehen die entsprechenden Alkoholate, wie Tetraethoxysilan.[1]
Gemischte Tetraholgensilane
Unter den gemischten Tetrahalogensilane sind wie z. B. bekannt:[2]
- Chlortrifluorsilan SiClF3
- Dichlordifluorsilan SiCl2F2
- Trichlorfluorsilan SiCl3F
Einzelnachweise
- A. F. Holleman, E. Wiberg, N. Wiberg: Lehrbuch der Anorganischen Chemie. 102. Auflage. Walter de Gruyter, Berlin 2007, ISBN 978-3-11-017770-1, S. 944–947.
- O. Yu. Troshin, A. D. Bulanov, O. Yu. Chernova: Liquid–Vapor Equilibria in the SiCl4–A (A = SiCl4 − nFn (n = 1–4) Impurity) Systems. In: Inorganic Materials. Band 54, Nr. 8, 2018, S. 840–843, doi:10.1134/S0020168518080162.
- Jöns Jacob Berzelius: Chlorkiesel. In: Lehrbuch der Chemie, 5. Auflage. Band 1. Arnold-Verlag, Dresden 1856, S. 325–326 (digitale-sammlungen.de).
- W. B. Schumb, R. C. Young: Silicobromoform. In: Harold Simmons Booth (Hrsg.): Inorganic Syntheses. Band 1, 1939, ISSN 1934-4716, S. 38–42, doi:10.1002/9780470132326.ch14.
- Eintrag zu Siliciumtetrafluorid in der GESTIS-Stoffdatenbank des IFA, abgerufen am 8. Januar 2021. (JavaScript erforderlich)
- Eintrag zu Siliciumtetrachlorid in der GESTIS-Stoffdatenbank des IFA, abgerufen am 1. Februar 2016. (JavaScript erforderlich)
- Datenblatt Silicium(IV) bromide bei AlfaAesar, abgerufen am 2. August 2013 (PDF) (JavaScript erforderlich).
- Datenblatt Silicon tetraiodide, ≥99.9% trace metals basis bei Sigma-Aldrich, abgerufen am 5. Januar 2014 (PDF).
- David R. Lide (Hrsg.): CRC Handbook of Chemistry and Physics. 90. Auflage. (Internet-Version: 2010), CRC Press/Taylor and Francis, Boca Raton, FL, Index of Refraction of Inorganic Liquids, S. 4-140.