Selentetrabromid
Selentetrabromid ist eine anorganische chemische Verbindung des Selens aus der Gruppe der Bromide.
| Kristallstruktur | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
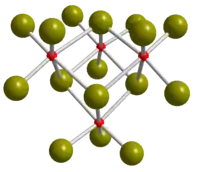 | ||||||||||||||||
| _ Se4+ _ Br− Se4Br16-Einheit in der Kristallstruktur von SeBr4 | ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | Selentetrabromid | |||||||||||||||
| Andere Namen |
Selen(IV)-bromid | |||||||||||||||
| Verhältnisformel | SeBr4 | |||||||||||||||
| Kurzbeschreibung |
ockergelber Feststoff[1] | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 398,60 g·mol−1 | |||||||||||||||
| Aggregatzustand |
fest[2] | |||||||||||||||
| Schmelzpunkt | ||||||||||||||||
| Löslichkeit |
| |||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||
Gewinnung und Darstellung
Selentetrabromid kann durch Reaktion von Selen mit Brom gewonnen werden.[1]
Eigenschaften
Selentetrabromid ist ein hygroskopischer feuchtigkeitsempfindlicher ockergelber Feststoff, der sich in Wasser über Selenoxybromid zu Selenige Säure[3] zersetzt und löslich in Kohlenstoffdisulfid, Chloroform und Ethylbromid ist.[2] Er hat einen unangenehmem, an Dischwefeldichlorid erinnernden Geruch und zerfällt an feuchter Luft in Brom, Diselendibromid und Selen unter Verfärbung nach Braunrot. Beim Erhitzen tritt Brom-Abspaltung ein, und zwischen 75 °C und 80 °C sublimiert ein Gemenge von Selentetrabromid und Diselendibromid in schwarzen, glänzenden Kristallen.[1] Mit Ammoniak reagiert die Verbindung unter Druck zu Tetraselentetranitrid.[3] Seine Kristallstruktur ist tetramer und ähnelt der von Cuban.[4] In konzentrierter Bromwasserstoffsäure bildet es mit Alkalibromiden Hexabromoselenate(IV), wie z. B. das rote Caesiumhexachloroselenat(IV) Cs2[SeBr6].[5]
Einzelnachweise
- Georg Brauer (Hrsg.), unter Mitarbeit von Marianne Baudler u. a.: Handbuch der Präparativen Anorganischen Chemie. 3., umgearbeitete Auflage. Band I, Ferdinand Enke, Stuttgart 1975, ISBN 3-432-02328-6, S. 419.
- Datenblatt Selenium(IV) bromide, 99+% bei AlfaAesar, abgerufen am 25. November 2013 (PDF) (JavaScript erforderlich).
- A. F. Holleman, E. Wiberg, N. Wiberg: Lehrbuch der Anorganischen Chemie. 101. Auflage. Walter de Gruyter, Berlin 1995, ISBN 3-11-012641-9, S. 621.
- Balaram Sahoo, Nimain C. Nayak, Asutosh Samantaray, Prafulla K. Pujapanda, Sahoo Balaram, nayak Nimai Charan, samantaray Asutosh, pujapanda Prafulla Kumar: Inorganic Chemistry. 2012, ISBN 978-81-203-4308-5, S. 490 (eingeschränkte Vorschau in der Google-Buchsuche).
- Synthese, Charakterisierung und strukturchemische Aspekte von Kupfer- und Silberchalkogenohalogeniden sowie von Halogeno- und Oxochalkogenaten(IV), von Cand. Paed. Michael Wagener, Universität Siegen 2005.


