Rydberg-Formel
Die Rydberg-Formel (auch Rydberg-Ritz-Formel) wird in der Atomphysik benutzt, um das Linienspektrum des vom Wasserstoff emittierten Lichtes zu bestimmen. Sie zeigt, dass die Bindungsenergie des Elektrons im Wasserstoffatom umgekehrt proportional zum Quadrat der Hauptquantenzahl ist.
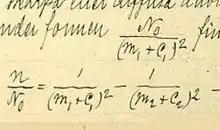
Die Formel wurde am 5. November 1888 vom schwedischen Physiker Johannes Rydberg vorgestellt; auch Walter Ritz arbeitete an ihr.
Korrekturen aufgrund von Drehimpulsen oder relativistischen Effekten werden in der Rydberg-Formel nicht berücksichtigt. Später wurde sie erweitert, um das Spektrum anderer Elemente zu bestimmen (s. u. Erweiterungen).
Rydberg-Formel für Wasserstoff
Formulierung
Dabei sind
- die Wellenlänge des Lichts im Vakuum
- die Rydberg-Konstante für das jeweilige Element: mit
- die Masse des Elektrons
- die Kernmasse (abhängig vom vorliegenden Isotop)
- die Rydberg-Konstante für unendliche Kernmasse. Da
- und ganzzahlige Werte der Hauptquantenzahl (mit ): ist die Quantenzahl des Orbits, von dem aus das Elektron in den tiefer gelegenen Orbit übergeht – also etwa vom dritten Orbit in den zweiten (siehe Bohrsches Atommodell).
Energie
Für die Energie des emittierten Photons gilt:
mit
- Lichtgeschwindigkeit im Vakuum
- Planckscher Konstante .
Entsprechend gilt für die Energiestufen der beiden o. g. Orbits im Atom (siehe Rydberg-Energie):
- .
Mit folgt daraus:
- .
Nachdem die Bedeutung der Hauptquantenzahl im Term für die Energieniveaus erkannt worden war, bürgerten sich die Begriffe Termsymbol und Termschema für damit zusammenhängende Werkzeuge ein.
Spektrallinien-Serien
Mit (Grundzustand) und erhält man eine Serie von Spektrallinien, die auch Lyman-Serie genannt wird. Der erste Übergang der Serie hat eine Wellenlänge von 121 nm, die Seriengrenze liegt bei 91 nm. Analog ergeben sich die anderen Serien:
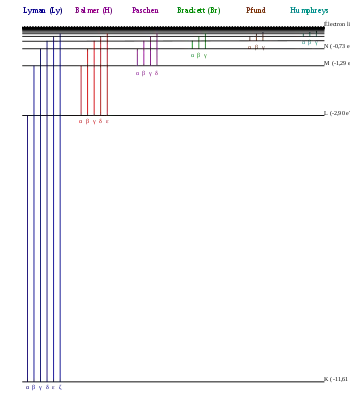
| Name | Wellenlänge des ersten Übergangs (α-Linie) |
konvergiert gegen Seriengrenze | ||
|---|---|---|---|---|
| 1 | 2 bis ∞ | Lyman-Serie | 121 nm | 91,13 nm |
| 2 | 3 bis ∞ | Balmer-Serie | 656 nm | 364,51 nm |
| 3 | 4 bis ∞ | Paschen-Serie | 1.874 nm | 820,14 nm |
| 4 | 5 bis ∞ | Brackett-Serie | 4.051 nm | 1458,03 nm |
| 5 | 6 bis ∞ | Pfund-Serie | 7.456 nm | 2278,17 nm |
| 6 | 7 bis ∞ | Humphreys-Serie | 12.365 nm | 3280,56 nm |
Erweiterungen
Für wasserstoffähnliche Atome
Für wasserstoffähnliche Ionen, d. h. Ionen, die nur ein einziges Elektron besitzen, wie z. B. He+, Li2+, Be3+ oder Na10+, lässt sich obige Formel erweitern zu:
mit
- der Kernladungszahl , d. h. der Anzahl der Protonen im Atomkern
- die um den Quantendefekt korrigierten effektiven Hauptquantenzahlen .
Für Atome mit einem Valenzelektron
Eine weitere Verallgemeinerung auf die Lichtemission von Atomen, die in ihrer äußersten Schale ein einzelnes Elektron besitzen, darunter aber evtl. weitere Elektronen in abgeschlossenen Schalen, führt zum Moseleyschen Gesetz.
Literatur
- Joseph Reader, Charles H. Corliss: Line Spectra of the Elements. In: CRC Handbook of Chemistry and Physics
Weblinks
- Umfangreiche Datenbank mit 568 Emissionslinien des Wasserstoffs des National Institute of Standards and Technology (A. Kramida, Yu. Ralchenko, J. Reader, and NIST ASD Team (2014). NIST Atomic Spectra Database (ver. 5.2))