Quercetin
Quercetin (von lateinisch quercus „Eiche“) ist ein gelber Naturfarbstoff aus der Gruppe der Polyphenole und Flavonoide. Als Pentahydroxyflavon zählt es zur Untergruppe der Flavonole. Quercetin ist ein Oxidationsprodukt[6] des Anthocyanin-Farbstoffs Cyanidin.[7]
| Strukturformel | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
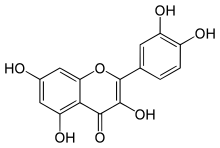 | ||||||||||||||||||||||
| Allgemeines | ||||||||||||||||||||||
| Name | Quercetin | |||||||||||||||||||||
| Andere Namen | ||||||||||||||||||||||
| Summenformel | C15H10O7 | |||||||||||||||||||||
| Kurzbeschreibung |
gelber, geruchloser Feststoff [2] | |||||||||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Eigenschaften | ||||||||||||||||||||||
| Molare Masse | 302,24 g·mol−1 | |||||||||||||||||||||
| Aggregatzustand |
fest | |||||||||||||||||||||
| Schmelzpunkt | ||||||||||||||||||||||
| Löslichkeit |
| |||||||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Toxikologische Daten | ||||||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||||||||
Vorkommen
Wie Cyanidin kommt Quercetin in der Natur als Glycosid oder Methylether vor. Für das Quercetin sind 179 verschiedene Glykoside bekannt[8] (z. B. Rutin oder Isorhamnetin).
Es ist weit verbreitet im Pflanzenreich und somit auch in der Nahrung. Große Mengen an Quercetin können in Zwiebeln, Äpfeln, Brokkoli oder grünen Bohnen gefunden werden, die je nach Art der Zubereitung teilweise zerstört werden. Auch durch das Schälen von Obst und Gemüse sinkt der Flavonoid-Anteil drastisch, denn speziell in den farbigen Schalen (Flavonoide sind Pflanzenfarbstoffe) ist der Flavonoidgehalt hoch. Ebenso ist es im Wein enthalten. Da Quercetin hauptsächlich in der Traubenschale vorkommt, sind die Gehalte im Rotwein höher als im Weißwein. Daneben trägt auch eine Holzfasslagerung zum Quercetingehalt bei, da die Substanz während der Lagerung langsam vom Holz in den Wein übergeht.

Einen hohen Gehalt an Quercetin findet man in folgenden Lebensmitteln:
- Kaper (1800 mg/kg)
- Liebstöckel (1700 mg/kg)
- Tee (Camellia sinensis)
- Zwiebel – besonders in den äußersten Ringen (284–486 mg/kg)
- Heidelbeere (kultiviert 74 mg/kg, wild 146–158 mg/kg)
- Grünkohl (60–110 mg/kg)
- rote Traube
- Apfel (21–440 mg/kg)
- Schnittlauch (245 mg/kg)
- Zitrusfrüchte
- Brokkoli (30 mg/kg) und anderem grünen Blattgemüse
- grüne Bohne (39 mg/kg)
- Kirsche (32 mg/kg)
- Himbeere
- Schwarze Johannisbeere (69 mg/kg)
- Brombeere (45 mg/kg)
- Preiselbeere (kultiviert 83–156 mg/kg, wild 121 mg/kg)
- Süße Eberesche (85 mg/kg)
- Sanddorn (62 mg/kg)
- Krähenbeere (kultiviert 53 mg/kg, wild 56 mg/kg).
Eine 2007 durchgeführte Studie ergab, dass Tomaten aus biologischem Anbau 79 % mehr Quercetin enthielten als bei konventionellem Anbau.[9]
Physiologische Bedeutung
Die Wirkung von Quercetin auf Säugetiere ist aktuell (Stand 2016) Gegenstand intensiver Forschung. Quercetin werden weitreichende, physiologisch positive Effekte zugesprochen. So zeigte sich u. a. inzwischen, dass 1000 mg/Tag Quercetin über 14 Tage nach hohen Belastungen zu hoch signifikant weniger Muskelkater und einer signifikant höheren Leistung im Doppelblindversuch bei Sportlern führte als ein Placebo.[10] Hervorzuheben ist das antioxidative Potential, da Quercetin ähnlich wie die Vitamine A, C und E als Radikalfänger wirkt. Der genaue Ablauf der Oxidations-Inhibierung in vivo wird allerdings noch diskutiert.
Quercetin gehört zwar auch zur Gruppe von Flavonoiden mit deutlich mutagenen Eigenschaften, es gibt aber keine Hinweise auf eine Toxizität beim Menschen, Tierversuche zeigten keine kanzerogene Wirkung von Flavonoiden.[11][8] Im Vergleich zu Taxifolin[12] weist Quercetin eine deutliche Mutagenität auf, allerdings ist dies an gewisse Bedingungen in der Zelle geknüpft.[13] Auch wirkt Quercetin direkt gegen Krebs, indem es Tumorzellen am Wachstum hindert und deren Tod hervorrufen kann.[14]
Ein Toxizitätsmodell in vitro hat gezeigt, dass die erhöhte oder längerfristige Gabe von Quercetin toxisch wirken kann.[15]
Quercetin hemmt in vitro die Wirkung des Medikaments Bortezomib durch direkte chemische Reaktion zwischen Quercetin und der Borongruppe.[16]
In vitro-Untersuchungen zeigten, dass es ähnlich dem Allopurinol die Xanthinoxidase hemmt und somit Hyperurikämie und daraus folgender Gicht entgegenwirken könnte.[17]
Quercetin könnte hemmend auf das für COVID-19 verantwortliche Virus SARS-CoV-2 wirken, da es die für die Vermehrung des Virus verantwortliche Protease 3CLpro hemmt.[18][19][20]
Einzelnachweise
- Eintrag zu QUERCETIN in der CosIng-Datenbank der EU-Kommission, abgerufen am 24. Oktober 2021.
- Datenblatt Quercetin (PDF) bei Carl Roth, abgerufen am 20. Juli 2007.
- Eintrag zu Quercetin. In: Römpp Online. Georg Thieme Verlag, abgerufen am 25. Juli 2011.
- Datenblatt Quercetin bei Sigma-Aldrich, abgerufen am 23. Oktober 2016 (PDF).
- Eintrag zu Quercetin in der ChemIDplus-Datenbank der United States National Library of Medicine (NLM)
- Jens Fleschhut: Untersuchungen zum Metabolismus, zur Bioverfügbarkeit und zur antioxidativen Wirkung von Anthocyanen, Dissertation, 2004 DNB 974478490 urn:nbn:de:swb:90-26403
- P. Schmid: Idacin-abbauende Enzyme in Äpfeln. In: Zeitschrift für Lebensmittel-Untersuchung und -Forschung. 133, 1967, S. 304–310, doi:10.1007/BF01074568.
- Bernhard Watzl, Gerhard Rechkemmer: Basiswissen aktualisiert: Flavonoide. In: Ernährungs-Umschau. Band 48, Nr. 12, 2001 (ernaehrungs-umschau.de).
- A. E. Mitchell u. a.: Ten-year comparison of the influence of organic and conventional crop management practices on the content of flavonoids in tomatoes. In: Journal of agricultural and food chemistry. 55, Nr. 15, 2007, S. 6154–6159, PMID 17590007.
- Ilenia Bazzucchi, Federica Patrizio, Roberta Ceci et al. (2019). The Effects of Quercetin Supplementation on Eccentric Exercise-Induced Muscle Damage. In: Nutrients 11(1), 205; https://doi.org/10.3390/nu11010205 aufg. 30. Januar 2019
- S. J. Duthie u. a.: The effect of dietary flavonoids on DNA damage (strand breaks and oxidised pyrimidines) and growth in human cells. In: Mutation Research. 390, Nr. 1–2, 1997, S. 141–151, PMID 9150762.
- Taxifolin ((2R,3R)-Dihydroquercetin) wirkt nicht mutagen und nur wenig toxisch. Taxifolin ist redox-äquivalent (~ konstitutionsisomer) zu Cyanidin.
- P. S. Makena u. a.: Comparative mutagenic effects of structurally similar flavonoids quercetin and taxifolin on tester strains Salmonella typhimurium TA102 and Escherichia coli WP-2 uvrA. In: Environmental and Molecular Mutagenesis. 50, Nr. 6, 2009 S. 451–459, PMID 19326464.
- Anja Klappan: Einfluss des Flavonoids Quercetin auf den mTOR-Signalweg von Zervix- und Mammakarzinomzellen. München 2014, DNB 1048361322, urn:nbn:de:bvb:19-165609 (Dissertation, LMU München).
- B. Ossola u. a.: Time-dependent protective and harmful effects of quercetin on 6-OHDA-induced toxicity in neuronal SH-SY5Y cells. In: Toxicology 250, Nr. 1, 2008, S. 1–8, PMID 18756631.
- F. T. Liu u. a.: Dietary flavonoids inhibit the anti-cancer effects of the proteasome inhibitor Bortezomib. In: Blood. 112, Nr. 9, 2008, S. 3835–3846, PMID 18633129.
- J. M. Pauff, R. Hille: Inhibition studies of bovine xanthine oxidase by luteolin, silibinin, quercetin, and curcumin. In: Journal of natural products. Band 72, Nummer 4, April 2009, S. 725–731, doi:10.1021/np8007123, PMID 19388706, PMC 2673521 (freier Volltext).
- Olga Abian, David Ortega-Alarcon, Ana Jimenez-Alesanco, Laura Ceballos-Laita, Sonia Vega, Hugh T. Reyburn, Bruno Rizzuti, Adrian Velazquez-Campoy: Structural stability of SARS-CoV-2 3CLpro and identification of quercetin as an inhibitor by experimental screening. In: International Journal of Biological Macromolecules. 3. September 2020, abgerufen am 23. August 2021 (englisch).
- https://www.ncbi.nlm.nih.gov/pmc/articles/PMC7985176/
- https://pubmed.ncbi.nlm.nih.gov/34194240/
Literatur
- S. U. Mertens-Talcott, S. S. Percival: Ellagic acid and quercetin interact synergistically with resveratrol in the induction of apoptosis and cause transient cell cycle arrest in human leukemia cells. In: Cancer Letters. 218, Nr. 2, 2005, S. 141–152, doi:10.1016/j.canlet.2004.06.007.
- J. M. Davis u. a.: Quercetin reduces susceptibility to influenza infection following stressful exercise. In: American Journal of Physiology-Regulatory, Integrative and Comparative Physiology. 2008;295:S. R505–R509, doi:10.1152/ajpregu.90319.2008.
