QS-21
QS-21 ist ein Extrakt aus dem chilenischen Seifenrindenbaum Quillaja saponaria, das bei Impfstoffen als Adjuvans verwendet wird. Es zählt zu einem der stärksten Adjuvanzien.
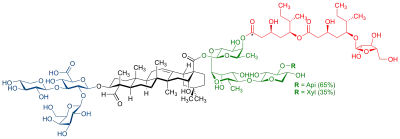
Eigenschaften
QS-21 enthält Saponine. Die enthaltenen Saponine bestehen aus einem am zentralen Fucose-Rest acylierten linearen Tetrasaccharid, welches an das C28-Atom eines Triterpens (Quillajasäure) gebunden ist.[1] Weiterhin trägt die Quillajasäure am C3-Atom ein verzweigtes Trisaccharid.[1] Die drei inneren Saccharide des Tetrasaccharids sind für die adjuvante Wirkung der Saponine notwendig.[1] Die hauptsächlich im Extrakt enthaltenen Saponine sind QS-21-Apiose und QS-21-Xylose im Verhältnis 2:1 und unterscheiden sich im endständigen Saccharid.[1][2][3] QS-21 neigt zur Hydrolyse an der Acylgruppe, wodurch die adjuvante Wirkung sinkt.[1] Eine synthetische Variante von QS-21 wurde beschrieben, wies aber nicht die gleiche adjuvante Wirkung auf.[1] Zusammen mit Monophosphoryl-Lipid-A (3-O-Desacyl-4′-monophosphoryl Lipid A, MPL) ist QS-21 Bestandteil des Adjuvans AS01 (liposomal) und AS02 (Emulsion).[4][5]
QS-21 verstärkt sowohl die humorale Immunantwort als auch die zelluläre Immunantwort.[2] In Mäusen wird zudem auch das NLRP3-Inflammasom aktiviert, was ein Freisetzen von Caspase-1-abhängigen Zytokinen ermöglicht.[3]
Gewinnung
QS-21 wird durch RP-HPLC aus dem wässrigen Extrakt QuilA der Rinde von Q. saponaria Molina gereinigt.[6] Unter den Fraktionen des QuilA sind QS-7, QS-17, Q-18 und QS-21 adjuvant.[6] Während die in der größten Menge vorkommende adjuvante Fraktion QS-18 in Mäusen toxisch ist, sind die weniger toxischen adjuvanten Fraktionen QS-7 und QS-21 verwendbar.[2] QS-21 ist die in größerer Menge vorkommende dieser beiden Fraktionen.[2]
Es wurden mehr als 50 QS-21-Analoga synthetisiert.[3]
Die Verfügbarkeit von Quillajaextrakt ist aufgrund geringer und übernutzter Bestände des Seifenrindenbaums begrenzt. Um Engpässen bei der Verwendung im SARS-CoV-2-Impfstoffkandidat NVX-CoV2373 zu begegnen, wird an der synthetischen Herstellung geforscht.[7]
Verwendung
QS-21 ist Bestandteil des Herpes-Zoster-Totimpfstoffs Shingrix.[8] Daneben wird es als Adjuvans bei Krebsimpfstoffen und Malariaimpfstoffen wie RTS,S untersucht.[2][4] Ein anderer, als Matrix-M bezeichneter Extrakt aus der Rinde von Q. saponaria wird als Adjuvans im SARS-CoV-2-Impfstoffkandidat NVX-CoV2373 verwendet.[9]
Geschichte
Die adjuvante Wirkung des Quillaja-Extrakts QuilA wurde erstmals 1925 von Gaston Ramon beschrieben, neben der adjuvanten Wirkung von Brotkrümeln, Tapiokamehl und Sojastärke bei der Diphtherieimpfung von Pferden.[10][11] Ab 1964 wurden die Saponine aus QuilA näher untersucht.[12] Aufgrund von Toxizität, Hämolyse und chemischer Instabilität war QS-21 bis Anfang der 2000er nicht für die Anwendung am Menschen zugelassen.[13] Im Jahr 2017 wurde der QS-21-enthaltende Herpes Zoster-Impfstoff Shingrix in den USA, 2018 in der EU zugelassen.
Literatur
- S. R. Bonam, C. D. Partidos, S. K. Halmuthur, S. Muller: An Overview of Novel Adjuvants Designed for Improving Vaccine Efficacy. In: Trends in pharmacological sciences, Band 38, Nummer 9, September 2017, S. 771–793, doi:10.1016/j.tips.2017.06.002, PMID 28668223.
- D. J. Marciani: Is fucose the answer to the immunomodulatory paradox of Quillaja saponins? In: International immunopharmacology, Band 29, Nummer 2, Dezember 2015, S. 908–913, doi:10.1016/j.intimp.2015.10.028, PMID 26603552.
Einzelnachweise
- E. K. Chea, A. Fernández-Tejada, P. Damani, M. M. Adams, J. R. Gardner, P. O. Livingston, G. Ragupathi, D. Y. Gin: Synthesis and preclinical evaluation of QS-21 variants leading to simplified vaccine adjuvants and mechanistic probes. In: Journal of the American Chemical Society, Band 134, Nummer 32, August 2012, S. 13448–13457, doi:10.1021/ja305121q, PMID 22866694, PMC 3436428 (freier Volltext).
- G. Ragupathi, J. R. Gardner, P. O. Livingston, D. Y. Gin: Natural and synthetic saponin adjuvant QS-21 for vaccines against cancer. In: Expert review of vaccines, Band 10, Nummer 4, April 2011, S. 463–470, doi:10.1586/erv.11.18, PMID 21506644, PMC 3658151 (freier Volltext).
- Marie-Aleth Lacaille-Dubois: Updated insights into the mechanism of action and clinical profile of the immunoadjuvant QS-21: A review. In: Phytomedicine (= 90th birthday of Professor Hildebert Wagner). Band 60, 1. Juli 2019, S. 152905, doi:10.1016/j.phymed.2019.152905.
- A. M. Didierlaurent, B. Laupèze, A. Di Pasquale, N. Hergli, C. Collignon, N. Garçon: Adjuvant system AS01: helping to overcome the challenges of modern vaccines. In: Expert review of vaccines, Band 16, Nummer 1, Januar 2017, S. 55–63, doi:10.1080/14760584.2016.1213632, PMID 27448771.
- N. Garçon, M. Van Mechelen: Recent clinical experience with vaccines using MPL- and QS-21-containing adjuvant systems. In: Expert review of vaccines, Band 10, Nummer 4, April 2011, S. 471–486, doi:10.1586/erv.11.29, PMID 21506645.
- C. R. Kensil, U. Patel, M. Lennick, D. Marciani: Separation and characterization of saponins with adjuvant activity from Quillaja saponaria Molina cortex. In: Journal of Immunology, Band 146, Nummer 2, Januar 1991, S. 431–437, PMID 1987271.
- A vaccine ingredient (in short supply) from Chile. Abgerufen am 3. Februar 2022 (englisch).
- Marie-Aleth Lacaille-Dubois: Updated insights into the mechanism of action and clinical profile of the immunoadjuvant QS-21: A review. In: Phytomedicine: International Journal of Phytotherapy and Phytopharmacology. Band 60, Juli 2019, S. 152905, doi:10.1016/j.phymed.2019.152905, PMID 31182297.
- Brendan Borrell: The Tree That Could Help Stop the Pandemic. 21. Oktober 2020, abgerufen am 5. November 2021 (englisch).
- G. Ramon: Sur l’augmentation anormale de L’antitoxine chez les chevaux producteurs de serum antidiphtherique. In: Bull. Soc. Centr. Med. Vet., 1925, Band 101, S. 227–234.
- H. J. Warshakoon, J. D. Hood, M. R. Kimbrell, S. Malladi, W. Y. Wu, N. M. Shukla, G. Agnihotri, D. Sil, S. A. David: Potential adjuvantic properties of innate immune stimuli. In: Human vaccines, Band 5, Nummer 6, Juni 2009, S. 381–394, PMID 19270494.
- R. Richou, R. Jensen, C. Belin: [Research on Saponin, an Adjuvant Substance which Stimulates Immunity. I]. (in french) In: Revue d’immunologie et de thérapie antimicrobienne, Band 28, 1964 Jan-Mar, S. 49–62, PMID 14187805.
- Z. I. Rajput, S. H. Hu, C. W. Xiao, A. G. Arijo: Adjuvant effects of saponins on animal immune responses. In: Journal of Zhejiang University. Science. B, Band 8, Nummer 3, März 2007, S. 153–161, doi:10.1631/jzus.2007.B0153, PMID 17323426, PMC 1810383 (freier Volltext).