Polymerelektrolytbrennstoffzelle
Die Polymerelektrolytbrennstoffzelle (engl. "Polymer Electrolyte Fuel Cell", PEFC, auch Protonenaustauschmembran-Brennstoffzelle, engl. Proton Exchange Membrane Fuel Cell, PEMFC oder Niedertemperatur-Polymerelektrolytmembran-Brennstoffzelle, NT-PEMFC, engl. Low Temperature Polymer Electrolyte Membrane Fuel Cell, LT-PEMFC oder Feststoffpolymer-Brennstoffzelle, engl. Solid Polymer Fuel Cell, SPFC[1]) ist eine Niedrigtemperatur-Brennstoffzelle.
Geschichte
Die PEMFC wurde zu Beginn der 1960er Jahre bei General Electric entwickelt. Willard Thomas Grubb entwickelte in Schenectady (New York) eine Ionenaustauschermembran auf der Basis von sulfoniertem Polystyrol, auf welcher Leonard Niedrach drei Jahre später Platin abscheiden konnte.[2] In der englischsprachigen Literatur wird dieser Brennstoffzellentyp zu Ehren der beiden GE-Wissenschaftler auch Grubb-Niedrach fuel cell genannt. Mitte der 1960er Jahre kam die Polymerelektrolytbrennstoffzelle im amerikanischen Raumflugprojekt Gemini das erste Mal zum Einsatz.[3][4]
Prinzip
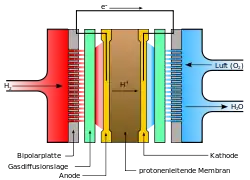

Unter Verwendung von Wasserstoff (H2) und Sauerstoff (O2) wird chemische in elektrische Energie umgewandelt. Der elektrische Wirkungsgrad beträgt je nach Arbeitspunkt etwa 60 Prozent. Als Elektrolyt dient dabei normalerweise eine feste Polymermembran, beispielsweise aus Nafion. Die Betriebstemperatur liegt im Bereich von 60 bis 120 °C, wobei für den kontinuierlichen Betrieb bevorzugt Temperaturen zwischen 60 und 85 °C gewählt werden. Die Membran ist beidseitig mit einer katalytisch aktiven Elektrode beschichtet, einer Mischung aus Kohlenstoff (Ruß) und einem Katalysator, häufig Platin oder ein Gemisch aus Platin und Ruthenium (PtRu-Elektroden), Platin und Nickel (PtNi-Elektroden), oder Platin und Cobalt (PtCo-Elektroden). H2-Moleküle dissoziieren auf der Anodenseite und werden unter Abgabe von zwei Elektronen zu je zwei Protonen oxidiert. Diese Protonen diffundieren durch die Membran. Auf der Kathodenseite wird Sauerstoff durch die Elektronen, die zuvor in einem äußeren Stromkreis elektrische Arbeit verrichten konnten, reduziert; zusammen mit den durch den Elektrolyt transportierten Protonen entsteht Wasser. Um die elektrische Arbeit nutzen zu können, werden Anode und Kathode an den elektrischen Verbraucher angeschaltet.
Reaktionsgleichungen
| Gleichung | |
|---|---|
| Anode | Oxidation / Elektronenabgabe |
| Kathode | Reduktion / Elektronenaufnahme |
| Gesamtreaktion | Redoxreaktion / Zellreaktion |
Der innere Ladungstransport erfolgt mittels Oxonium-Ionen. Auf der Anodenseite benötigt die Reaktion Wasser, welches sie auf der Kathodenseite wieder abgibt. Um den Wasserbedarf auf der Anodenseite zu decken, ist ein aufwändiges Wassermanagement erforderlich. Realisiert wird dies unter anderem durch Rückdiffusion durch die Membran und Befeuchtung der Edukte.[5][6]
Anwendungsbereiche
Als Hauptanwendungsgebiete sind mobile Anwendungen ohne Nutzung der Abwärme, etwa in Brennstoffzellenfahrzeugen, U-Booten, Raumschiffen oder Akkumulatorladegeräten für unterwegs zu sehen. Auch stationäre Kleinanlagen mit einem Abwärmeniveau um 60 bis 80 °C sind möglich. Um eine technisch relevante elektrische Spannung zu erzielen, werden mehrere Zellen (zehn bis mehrere hundert) zu einem so genannten Stack (dt.: Stapel) hintereinander in Reihe geschaltet.[7] Die Temperaturregelung des Stacks erfolgt in einem eigenen zusätzlichen Kühlkreislauf.
Es ist auch ein wärmegeführter, stationärer Einsatz, z. B. in Wohnhäusern, bei einem Nutzwärmeniveau von 80 °C möglich, wobei in etwa gleichem Verhältnis Wärme und elektrischer Strom aus Biowasserstoff oder Wasserstoff, der nach dem Kværner-Verfahren aus Erdgas erzeugt wird, produziert werden. Dies ist eine Form der Kraft-Wärme-Kopplung, bei der ein Gesamtwirkungsgrad von 90 Prozent realistisch ist.[7]
CO-Toleranz
Da die Reaktionen bei relativ niedrigen Temperaturen (60 bis 120 °C) ablaufen, stellt die Toleranz gegen Kohlenstoffmonoxid (CO) ein Problem dar. Die CO-Konzentration der Kathoden-seitig zugeführten Luft sowie das auf der Anoden-Seite zugeführte wasserstoffreiche Gasgemisch sollte bei Platin-Elektroden deutlich unter 10 ppm und bei Platin-Ruthenium-Elektroden deutlich unter 30 ppm liegen. Andernfalls werden zu viele katalytisch aktive Zentren der Membranoberfläche durch CO-Moleküle blockiert. Die Sauerstoff-Moleküle bzw. Wasserstoff-Moleküle können nicht mehr adsorbiert werden und die Reaktion bricht in kürzester Zeit zusammen. Durch das Spülen der Brennstoffzelle mit reinem Inertgas oder reinem Wasserstoff kann das CO wieder von der Membran entfernt werden. CO führt auch innerhalb der Toleranzbereiche zu einer beschleunigten, irreversiblen Alterung der Membran; allerdings kann dieser Effekt durch eine Beimischung geringer Luftmengen (≤ 1 Vol.-%) aufgehoben werden. In diesem Fall sind Betriebszeiten von mehr als 15.000 h nachweisbar.[8]
Ziel der aktuellen Forschung an der Niedertemperatur-Polymerelektrolytmembran-Brennstoffzelle ist daher, die CO-Toleranz der Membranen zu erhöhen sowie den Brennstoffzellen-Stack bei einer höheren Betriebstemperatur betreiben zu können. Problematisch ist derzeit noch, ein geeignetes Ionomer für diesen Temperaturbereich zu finden. Bei Nafion steigt der elektrische Widerstand zu stark an und es verliert seine Eigenschaft Protonen leiten zu können. Dies liegt daran, dass für die Protonenleitfähigkeit der Membran flüssiges Wasser nötig ist.[9]
Im Gegensatz zur Niedertemperatur-Polymerelektrolytmembran-Brennstoffzelle wird in der Hochtemperatur-Polymerelektrolytmembran-Brennstoffzelle eine Säure mit hohem Siedepunkt als Elektrolyt verwendet.[10]
Schwefelgehalt
Schwefel und Schwefelverbindungen (hier insbesondere Schwefelwasserstoff) sind starke Katalysatorgifte. Verursacht wird dies durch eine starke Chemisorption auf der katalytisch aktiven Membranoberfläche. Es erfolgt eine nicht reversible Zerstörung.[11] Die Konzentration dieser Verbindungen im Gasstrom muss im unteren zweistelligen ppb-Bereich liegen, um eine solche Schädigung zu vermeiden.[12]
Vor- und Nachteile gegenüber anderen Brennstoffzellen
Die Vorteile einer Niedertemperatur-PEM (Nafion-Basis) sind:
- Fester Elektrolyt, das heißt, es können keine aggressiven Flüssigkeiten auslaufen.
- Die Zelle weist eine hohe Leistungsdichte auf[5] und
- hat ein gutes dynamisches Verhalten.
- Auf der Kathodenseite kann Luft verwendet werden. Es ist kein Reingas (Sauerstoff) erforderlich.[5]
- Der Elektrolyt ist CO2-beständig
Die Nachteile sind:
- Der Zelltyp ist sehr empfindlich gegen Verschmutzungen durch CO, NH3 und Schwefelverbindungen im Brenngas.[12]
- Das Wassermanagement ist aufwändig, da ein Austrocknen der Membran vermieden werden muss.[6] Außerdem muss auch das Gefrieren des Wassers in der Membran verhindert werden.[5]
- Der Anlagenwirkungsgrad ist mit 34 %[13] oder 50 bis 68 %[14] eher niedrig, wobei für Wirkungsgrade über 50 % relativ hohe Temperaturen (bis zu 800 °C) erforderlich sind.[15]
Weblinks
- Institut für Energie- und Klimaforschung des Forschungszentrums Jülich – PEM-Elektrolyse. (Nicht mehr online verfügbar.) Archiviert vom Original am 7. April 2019.
- PEMFC - proton exchange membrane fuel cell: Informationen zum Thema Brennstoffzelle.
- Wasserstoffbasiertes Speicherkraftwerk soll in der Lausitz entstehen. heise.de, 16. Dezember 2019 (ein kleines Versuchsmodell).
Einzelnachweise
- Wissenschaft-Online-Lexika: Eintrag zu Polymerelektrolytmembran-Brennstoffzelle im Lexikon der Physik, abgerufen am 5. Januar 2009
- Grubb, Willard Thomas. Bei: encyclopedia of earth, abgerufen am 7. August 2012
- History. In: Fuel Cell Today – Knowledge. FuelCellsWorks, abgerufen am 15. Juni 2021 (englisch).
- Fuel Cell, Gemini, Cutaway. In: National Air and Space Museum Collection. Smithsonian's National Air and Space Museum, abgerufen am 15. Juni 2021 (englisch).
- Peter Kurzweil, Ottmar Schmid: Brennstoffzellentechnik: Grundlagen, Komponenten, Systeme, Anwendungen. 3. Auflage. Springer Fachmedien, Wiesbaden 2016, ISBN 978-3-658-14935-2, Kapitel 4: Polymerelektrolyt-Brennstoffzelle, S. 98, doi:10.1007/978-3-658-14935-2_4 (eingeschränkte Vorschau in der Google-Buchsuche).
- Colleen Spiegel: Water Management For PEM Fuel Cells. In: Fuel Cell Basics. Fuel Cell Store, 7. November 2017, abgerufen am 14. Juni 2021 (englisch).
- Dominic A. Notter, Katerina Kouravelou, Theodoros Karachalios, Maria K. Daletou and Nara Tudela Haberlandad: Life cycle assessment of PEM FC applications: electric mobility and μ-CHP. In: Energy and Environmental Science 8, (2015), 1969–1985, doi:10.1039/C5EE01082A.
- J. Scholta, J. Pawlik, N. Chmielewski, L. Jörissen: Longevity test results for reformate polymer electrolyte membrane fuel cell stacks. In: Journal of Power Sources 196, (2011), 5264–5271, doi:10.1016/j.jpowsour.2010.08.113.
- Shawn Litster, Cullen R. Buie, Tibor Fabian, John K. Eaton, Juan G. Santiago: Active Water Management for PEM Fuel Cells. In: Journal of The Electrochemical Society. Band 154, Nr. 10, 2007, S. B1049, doi:10.1149/1.2766650 (iop.org [abgerufen am 25. Juli 2021]).
- Thomas J. Schmidt: Durability and Degradation in High-Temperature Polymer Electrolyte Fuel Cells. In: ECS Transactions. Band 1, Nr. 8, 21. Dezember 2019, ISSN 1938-6737, S. 19–31, doi:10.1149/1.2214541 (iop.org [abgerufen am 25. Juli 2021]).
- Janine Ellner: Untersuchungen zum Einfluss von Schwefelverbindungen auf Wirkungsgrad und Degradation biogasbetriebener PEM-Brennstoffzellensysteme. Dissertation. Fakultät III Prozesswissenschaften der Technischen Universität, Berlin 2013, DNB 1065665393 (tu-berlin.de [PDF; 4,0 MB]).
- Wasserstoffqualitätsanforderungen: Anforderungen der ISO/DIS 14687 bzw. DIN EN 17124 an die verschiedenen Wasserstoffqualitäten und Auswirkungen hinsichtlich H2- und H2-Gemischtransport sowie resultierende Vermarktungs- und Einsatzmöglichkeiten für Gasversorger. (PDF, 1,7 MB) Studie. DBI - Gastechnologisches Institut gGmbH Freiberg, 27. November 2020, S. 9, abgerufen am 15. Juni 2021.
- Brennstoffzellensysteme in der Entwicklung. (Nicht mehr online verfügbar.) Forschungszentrum Jülich, Institut für Energie- und Klimaforschung (IEF), archiviert vom Original am 18. Januar 2017 (Informationen nach Stand der Technik von 2012).
- Peter Kurzweil, Ottmar Schmid: Brennstoffzellentechnik: Grundlagen, Komponenten, Systeme, Anwendungen. 3. Auflage. Springer Fachmedien, Wiesbaden 2016, ISBN 978-3-658-14935-2, Kapitel 4: Polymerelektrolyt-Brennstoffzelle, S. 79, doi:10.1007/978-3-658-14935-2_4 (eingeschränkte Vorschau in der Google-Buchsuche).
- Tobias Schlößer: Reversible Brennstoffzelle bricht Wirkungsgrad-Rekord. Pressemitteilung. Forschungszentrum Jülich, 18. Dezember 2018, abgerufen am 30. Juli 2019.