Plazomicin
Plazomicin (Internationaler Freiname) ist ein „Next-generation“-Aminoglykosid-Antibiotikum. Es ist ein Derivat von Sisomicin, welches in den USA unter dem Handelsnamen Zemdri vertrieben wird.[2] Vor der Markteinführung war der Codename in Publikationen ACHN-490.[3]
| Strukturformel | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
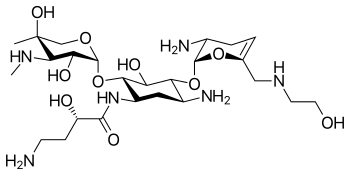 | ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Freiname | Plazomicin | |||||||||||||||
| Andere Namen |
| |||||||||||||||
| Summenformel | C25H48N6O | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Arzneistoffangaben | ||||||||||||||||
| Wirkstoffklasse | ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 592,68 g·mol−1 | |||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||
Entdeckung
Seit den fünfziger Jahren werden Aminoglykoside als Breitbandantibiotika zur Bekämpfung von bakteriellen Infektionen eingesetzt. Diese Medikamente binden an die A-Seite bakterieller Ribosomen und blockieren so die Proteinsynthese. Im Laufe der Jahre entwickelten sich aber verschiedene resistente Bakterienstämme. Die Resistenzmechanismen werden unter dem Begriff AME (Aminoglykosid-modifizierende Enzyme) zusammengefasst. Zum Beispiel wurden Aminoglykoside durch eine AAC (Aminoglykosid-Acetyltransferase) N-acetyliert, durch eine ABT (Aminoglykosid-Nucleotidyltransferase) O-adenyliert oder durch eine APH (Aminoglykosid-Phosphotransferase) O-phosphoryliert. Die Arbeitsgruppe um Aggen versuchte Aminoglykoside zu entwickeln, welche diese Resistenz überwinden könnten.[3] Unter 400 Derivaten erwies sich Plazomicin als besonders aussichtsreich. Plazomicin wurde von der Firma Achaogen zur Behandlung von Infektionen mit multiresistenten Erregern geprüft. Im Jahr 2012 hat die US-amerikanische FDA eine so genannte "fast-track"-Zulassungsprüfung beschlossen. Im Januar 2015 verlieh die FDA Plazomicin das Zertifikat „Qualified Infectious Disease Product“ (QIDP).[4] Im Juni 2018 erhielt Plazomicin in den USA die FDA-Zulassung zur Behandlung von komplizierten Harnwegsinfekten ohne Sepsis.[5] Die beantragte Zulassung für septischen Harnwegsinfekt wurde von der FDA abgelehnt, weil der Wirksamkeitsnachweis nicht erbracht wurde.
Gewinnung
Plazomicin kann aus Sisomicin durch Einfügung von Hydroxyaminobuttersäure (HABA) an Position 1 und einer Hydroxyethyl-Gruppe an Position 6' synthetisiert werden.[3][6]
Wirkspektrum
In in-vitro-Studien konnte nachgewiesen werden, dass Plazomicin in Kombination mit Daptomycin oder Ceftobiprol gegen MRSA (Methicillin-resistenter Staphylococcus aureus) und VRSA (Vancomycin-resistenter Staphylococcus aureus) synergistisch wirksam ist. Plazomicin hemmt in Kombination mit Cefepim, Doripenem, Imipenem oder Piperacillin/Tazobactam auch das Wachstum von Pseudomonas aeruginosa.[6] Ferner konnte eine Wirksamkeit gegen Carbapenem-resistentem Acinetobacter baumannii festgestellt werden.[7] Plazomicin allein hatte keine ausreichende Hemmung von Streptokokken (inklusive Streptococcus pneumoniae), Enterokokken (inklusive Enterococcus faecalis, Enterococcus faecium), Anaerobier, Stenotrophomonas maltophilia and Acinetobacter spp und eine variable Hemmung von Pseudomonas aeruginosa.[8]
Klinische Anwendung
In einer Phase-III-Studie CARE wurde die Wirksamkeit von Plazomicin bei ambulant erworbener Lungenentzündung oder Sepsis mit CRE (Carbapenem-resistenten Enterobacteriaceae) geprüft.[9] Die eine Gruppe erhielt Plazomicin 15 mg/kg Körpergewicht täglich, die andere Colistin 5 mg/kg täglich, jeweils in Kombination mit Meropenem oder Tigecyclin. Die Überlebensrate war mit Plazomicin höher als mit Colistin.
In der EPIC-Studie wurde die Wirkung von Plazomicin in einer Phase-III-Studie bei Patienten mit komplizierter Harnwegsinfektion geprüft.[10] Dabei erhielt die eine Gruppe Plazomicin 15 mg/kg Körpergewicht, die andere Meropenem 1 g alle 8 Stunden. Im Ergebnis war Plazomicin Meropenem nicht unterlegen. Nach Plazomicin erlitten weniger Patienten einen Rückfall.
Plazomicin wird einmal täglich als intravenöse Infusion angewendet.[11] Eine Ampulle enthält 500 mg Plazomicin-Sulfat für 10 ml Lösung (50 mg/ml).
Kontraindikationen
Plazomicin darf nicht angewendet werden, wenn eine Überempfindlichkeit gegen irgendein Aminoglykosid besteht. Wie alle Aminoglykoside schädigt Plazomicin den Fötus schwangerer Frauen. Die Substanz passiert den Mutterkuchen und geht auf den Feten über.
Nebenwirkungen[2]
Nephrotoxizität
Plazomicin kann die Nieren schädigen. In 21 von 300 Patienten wurde ein Anstieg des Kreatinins um 0,5 mg/dl oder mehr beobachtet. In den meisten Fällen normalisiert sich die Nierenfunktion nach Absetzen des Medikaments. Ein erhöhtes Risiko besteht bei vorbestehender Nierenfunktionsstörung, bei älteren Patienten und bei gleichzeitiger Einnahme anderer nierenschädigender Medikamente.
Ototoxizität
Eine Innenohrschädigung kann sich durch Hörminderung, Tinnitus (Pfeifgeräusch)oder Schwindel äußern. Tritt diese Symptomatik nach Behandlung mit Plazomicin auf, so kann sie irreversibel sein. In manchen Fällen traten die Zeichen der Innenohrschädigung erst nach Abschluss der Behandlung auf. Ein erhöhtes Risiko einer Innenohrschädigung besteht bei einer Familienanamnese mit Hörverlust, bei eingeschränkter Nierenfunktion und bei höherer Dosis oder längerer Anwendung des Medikaments als empfohlen.
Neuromuskuläre Blockade
Wie alle Aminoglykoside kann Plazomicin eine Muskelschwäche bei Patienten mit einer vorbestehenden neuromuskulären Erkrankung verstärken. Nach Gabe von Muskelrelaxantien kann die Erholung der Muskelfunktion verzögert werden. Bei Patienten mit Myasthenia gravis ist eine besondere Überwachung notwendig.
Anaphylaxie
Selten wurden ernste gegebenenfalls tödliche Überempfindlichkeitsreaktionen beobachtet. In diesen Fällen besteht eine Überempfindlichkeit gegenüber allen Aminoglykosiden. Vor der Anwendung von Plazomicin muss sorgfältig nach früheren Reaktionen nach der Gabe von Aminoglykosiden gefragt werden.
Clostridium-difficile-assoziierte Diarrhoe (CDAD)
Bei allen Antibiotika-Gaben wird die natürliche Darmflora gestört und es kann zu einem starken Wachstum von Clostridium difficile kommen. Je nach Ausprägung führt dies zu einer leichten Durchfallerkrankung bis hin zu einer lebensbedrohlichen Dickdarmentzündung. Eine CDAD kann auch bis zu 2 Monate nach einer antibiotischen Behandlung auftreten
Einzelnachweise
- Dieser Stoff wurde in Bezug auf seine Gefährlichkeit entweder noch nicht eingestuft oder eine verlässliche und zitierfähige Quelle hierzu wurde noch nicht gefunden.
- ZEMDRI (plazomicin) Injection. For adult patients with cUTI, including pyelonephritis, due to certain Enterobacteriaceae. ACHAOGEN,, Oktober 2018, abgerufen am 12. März 2019 (englisch).
- James B Aggen, Eliana S Armstrong, Adam A Goldblum, Paola Dozzo, Martin S Linsell: Synthesis and spectrum of the neoglycoside ACHN-490. In: Antimicrobial Agents and Chemotherapy. Band 54, Nr. 11, November 2010, S. 4636–4642, doi:10.1128/AAC.00572-10, PMID 20805391, PMC 2976124 (freier Volltext).
- Candice Knoll: Achaogen Announces Plazomicin Granted QIDP Designation by FDA. GlobeNewswire, 8. Januar 2015, abgerufen am 12. März 2019 (englisch).
- Jennie Walters: FDA approves plazomicin for cUTI, but not blood infections. Biocentury, 8. Januar 2015, abgerufen am 12. März 2019 (englisch).
- George G Zhanel, Christopher D Lawson, Sheryl Zelenitsky, Brandon Findlay, Frank Schweizer: Comparison of the next-generation aminoglycoside plazomicin to gentamicin, tobramycin and amikacin. In: Expert Review of Anti-Infective Therapy. Band 10, Nr. 4, April 2012, S. 459–473, doi:10.1586/eri.12.25, PMID 22512755.
- Cristina García-Salguero, Iciar Rodríguez-Avial, Juan J Picazo, Esther Culebras: Can Plazomicin Alone or in Combination Be a Therapeutic Option against Carbapenem-Resistant Acinetobacter baumannii? In: Antimicrobial Agents and Chemotherapy. Band 59, Nr. 10, Oktober 2015, S. 5959–5966, doi:10.1128/AAC.00873-15, PMID 26169398, PMC 4576036 (freier Volltext).
- CENTER FOR DRUG EVALUATION AND RESEARCH: Drug Approval Package: ZEMDRI (plazomicin). FDA, 27. Oktober 2017, abgerufen am 12. März 2019 (englisch).
- James A. McKinnell, Jamie P. Dwyer, George H. Talbot, Lynn E. Connolly, Ian Friedland: Plazomicin for Infections Caused by Carbapenem-Resistant Enterobacteriaceae. In: New England Journal of Medicine. Band 380, Nr. 8, 21. Februar 2019, S. 791–793, doi:10.1056/NEJMc1807634.
- Florian M E Wagenlehner, Daniel J Cloutier, Allison S Komirenko, Deborah S Cebrik, Kevin M Krause: Once-Daily Plazomicin for Complicated Urinary Tract Infections. In: New England Journal of Medicine. Band 380, Nr. 8, 21. Februar 2019, S. 729–740, doi:10.1056/NEJMoa1801467.
- Medscape Log In. In: www.medscape.com. Abgerufen am 3. Juli 2018.