Vancomycin
Vancomycin ist ein Antibiotikum aus der Wirkstoffgruppe der Glykopeptid-Antibiotika. Es wurde 1955 aus Kulturen von Amycolatopsis orientalis (Streptomyces orientalis) isoliert,[1] und ab 1980 als wirksame Alternative gegen multiresistente Staphylokokken eingesetzt. Staphylokokken kommen neben Enterokokken häufig in Krankenhäusern als Verursacher nosokomialer Infektionen vor. Vancomycin ist ein Antibiotikum der dritten Linie, das eingesetzt wird, wenn andere Mittel aufgrund von Resistenz nicht mehr wirksam sind. Vom Darm wird es nicht aufgenommen, was man sich bei der antibiotikaassoziierten Kolitis zunutze machen kann.
| Vancomycin | ||
|---|---|---|
| ||
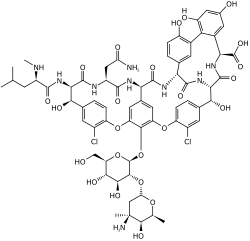
| Strukturformel | ||
| Masse/Länge Primärstruktur | 7 Aminosäuren (teilmodifiziert), 1450 Dalton | |
| Bezeichner | ||
| Externe IDs |
| |
| Arzneistoffangaben | ||
| ATC-Code | A07AA09 J01XA01 | |
| DrugBank | DB00512 | |
| Wirkstoffklasse | Glykopeptid-Antibiotikum | |
Wirkungsmechanismus
Vancomycin hemmt den Aufbau der Bakterien-Zellwand, indem es mit den endständigen L-Lysin-D-Alanyl-D-Alanin-Gruppen des bakteriellen Zellwandbestandteils Murein einen Komplex bildet.[2] Damit blockiert es die Bausteine der Quervernetzung der Zellwand grampositiver Bakterien durch eine Brücke aus fünf Glycinresten (Pentaglycinbrücke/Pentapeptidseitenkette),[3] sodass bestimmte für die Quervernetzung bedeutsame Bausteine (N-Acetylglucosamin, N-Acetylmuraminsäure) nicht mehr in die wachsende Bakterienzellwand eingebaut werden. Der Wirkmechanismus von Vancomycin als Glycopeptid beruht nicht auf der Bindung an die Transglykosylase.[4] Da Bakterien einen relativ hohen osmotischen Druck haben, kann die Zellwand ohne die Vernetzung diesem Druck nicht standhalten, und das Bakterium platzt.
Synthese
Glycosyltransferasen GtfB glycosylieren in Tandemaktion den Präkursor zum wirksamen Vancomycin.[5]
Verwendung
Systemische Behandlung
Die Anwendung von Vancomycin erfolgt als intravenöse Infusion oder Injektion zur Behandlung schwerer Infektionen durch grampositive Erreger, die gegen andere Antibiotika resistent sind (z. B. Oxacillin-resistenter Staphylococcus aureus). Vancomycin galt lange als letzte Hoffnung zur Behandlung lebensbedrohlicher Infektionen durch grampositive kugelförmige Bakterien (Kokken), als Reserveantibiotikum. Diese Hoffnung endete 1987, als Vancomycin-resistente Enterokokken (VRE) in den Krankenhäusern auftraten.
Seit einigen Jahren gilt Linezolid als Reserveantibiotikum (Last line of defense).
Eine weitere Anwendung findet Vancomycin in der perioperativen Antibiotikaprophylaxe, z. B. bei Implantation eines Portkatheters bei gleichzeitig bestehender Neutropenie.
Bei gleichzeitiger Therapie mit Aminoglykosiden, bei Patienten mit instabiler Nierenfunktion, dialysepflichtigen Patienten oder bei hoher Dosierung und längerer Therapiedauer sowie bei schweren Infektionen sind die Serumspiegel (Spitzenspiegel: 30–40 mg/L; Talspiegel: 10–15 mg/L) von Vancomycin zu kontrollieren.[6]
Nebenwirkungen
Insbesondere bei schneller Infusion kann es zu einer generalisierten Rötung der Haut kommen. Dieses wurde bei der Erstbeschreibung 1959 als red man syndrome bezeichnet. Wegen der rassistischen Implikation wurde vorgeschlagen, eine Umbenennung in "Vancomycin-Flush-Reaktion" vorzunehmen. Diese Nebenwirkung lässt sich mit Antihistaminika beherrschen und muss von einer echten Allergie unterschieden werden. Nach einer "Vancomycin-Flush-Reaktion" kann im Notfall Vancomycin mit langsamer Infusion und Histamin-Gabe erneut verwendet werden.[7] Zusätzlich gibt es echte allergische Reaktionen wie die IgE-vermittelte Typ-I-Hypersensitivität, die verzögerte Typ-II-Hypersensitivität, die lineare, bullöse IgA-Dermatose (LABD) und den medikament-induzierten Ausschlag mit Eosinophilie und Allgemeinsymptomen. Weitere mögliche Nebenwirkungen sind eine Schädigung der Nieren (Nephrotoxizität oder akute interstitielle Nephritis), eine Verschlechterung des Gehörs (Ototoxizität) und Blutbildveränderungen (Neutropenie, Thrombozytopenie).[8]
Topische Behandlung
Vancomycin wirkt sehr gut bei antibiotikaassoziierter pseudomembranöser Enterocolitis durch Clostridioides difficile. Das im Darm nicht resorbierbare Antibiotikum wird dazu oral verabreicht. In erster Linie wird bei der pseudomembranösen Enterocolitis jedoch das wesentlich preisgünstigere Metronidazol eingesetzt, mit dem es auch weniger Probleme mit Resistenzentwicklungen (Vancomycin-resistente Enterokokken, VRE) gibt.
Resistenzbildung
Vancomycin-Resistenz ist zum Teil auf die Expression einer alternativen D-Alanyl:D-Alanin-Ligase zurückzuführen. Dieses alternative Enzym ligiert D-Lactat anstelle von D-Alanin, was zu einem (–OH)- anstelle eines (–NH2)-Terminus führt. Dadurch wird die Bindung von Vancomycin verhindert und die Vernetzung des Mureins über eine Depsipeptidbindung ermöglicht. Eine andere Art der Resistenzbildung ist die Expression einer D-Ala:D-Ser-Ligase anstelle der D-Ala:D-Ala-Ligase.
Als Auslöser für die Verbreitung Vancomycin-resistenter Enterokokken gilt der Wachstumsbeschleuniger Avoparcin,[9] der strukturelle Ähnlichkeit zu Vancomycin aufweist. Er wurde bis 1996 in Deutschland in der Tiermast verwendet. Seit 1997 darf Avoparcin in der Europäischen Union nicht mehr als Futtermittelzusatz benutzt werden.[10]
2020 wurden die Ergebnisse einer Arbeitsgruppe an der Universitätsklinik Heidelberg veröffentlicht, die zeigen, dass durch eine vergleichsweise einfache Modifikation mit einem kationischen Oligopeptid, bestehend aus sechs Arginin-Einheiten in der Position VN, auch Vancomycin-resistente Bakterienstämme abgetötet werden können. Gegenüber unmodifiziertem Vancomycin konnte die Aktivität um den Faktor 1 000 gesteigert werden.[11] Der Wirkstoff ist noch in der präklinischen Entwicklung und deshalb noch Jahre von einer möglichen Zulassung entfernt.
Fertigarzneimittel
Vancomycin wurde von Eli Lilly entwickelt und ab 1955 im Markt eingeführt, zunächst in den USA. Arzneilich verwendet wird ausschließlich das wasserlösliche Vancomycinhydrochlorid, entweder als Pulver zur Herstellung einer Infusionslösung (für die systemische Therapie) sowie als Pulver zur Herstellung einer Lösung zum Einnehmen oder als Kapsel (für die topische Therapie).
Vancomycinhaltige Arzneimittel sind unter dem Markennamen Vancocin („Lilly“) und unter dem generischen Namen (Freinamen) auf dem Markt (z. B. Vancomycin CP Lilly).
Siehe auch
Literatur
- Constanze Wendt, Henning Rüden, Michael Edmond: Vancomycin-resistente Enterokokken: Epidemiologie, Risikofaktoren und Prävention. In: Deutsches Ärzteblatt. (Köln) 95(25), 1998, S. A1604–A1611.
- Dudley H. Williams, Ben Bardsley: Die Vancomycin-Antibiotika und der Kampf gegen resistente Bakterien. In: Angewandte Chemie. 111(9), 1999, S. 1264–1286.
- G. Schulze, W. Schott, G. Hildebrandt: Vancomycin-resistente Enterokokken – Krankenhausküche als Vektor? In: Bundesgesundheitsblatt. 44(7), 2001, S. 732–737.
- F. Dieber, G. Gorkiewicz, J. Kofer: Nachweis von Vancomycin-resistenten Enterokokken in der Tierproduktion der Steiermark. In: Arbeitstagung des Arbeitsgebietes Lebensmittelhygiene. 44, 2003, S. 449–454.
- Brian K. Hubbard, Christopher T. Walsh: Der Aufbau von Vancomycin: so macht es die Natur. In: Angewandte Chemie. 115(7), 2003, S. 752–789.
- Hermann Feldmeier: Antibiotikaresistenz durch widernatürliche Fütterung. In: Naturwissenschaftliche Rundschau. 57(11), S. 632–633.
- A. Simon, N. Gröger, S. Engelhart, G. Molitor, M. Exner, U. Bode, G. Fleischhack: Vancomycin-resistente Enterokokken (VRE) – Übersicht zu Bedeutung, Prävention und Management in der Pädiatrie. In: Hygiene und Medizin. 29(7/8), 2004, S. 259 ff.
- W. Witte, I. Klare, G. Werner: Selective pressure by antibiotics as feed additives. In: Infection. 27 (Suppl 2), 1999, S. 35–38.
Einzelnachweise
- Karl Wurm, A. M. Walter: Infektionskrankheiten. In: Ludwig Heilmeyer (Hrsg.): Lehrbuch der Inneren Medizin. Springer-Verlag, Berlin/Göttingen/Heidelberg 1955; 2. Auflage ebenda 1961, S. 9–223, hier: S. 53.
- Igor Pochorovski: Synthese von Vancomycinsonden für Activity-Based Protein Profiling in der Google-Buchsuche
- K. Aktories, U. Förstermann, F. Hofmann, K. Starke: Allgemeine und spezielle Pharmakologie und Toxikologie. 10. Auflage. Elsevier, München 2009, ISBN 978-3-437-42522-6.
- William Barry Hugo, S. P. Denyer, Norman A. Hodges, S. P. Gorman: Hugo and Russell's pharmaceutical microbiology. John Wiley & Sons, 2004, ISBN 978-0-632-06467-0 (eingeschränkte Vorschau in der Google-Buchsuche).
- Heather C. Losey, Mark W. Peczuh, Zhong Chen, Ulrike S. Eggert, Steven D. Dong, Istvan Pelczer, Daniel Kahne, Christopher T. Walsh: Tandem action of glycosyltransferases in the maturation of vancomycin and teicoplanin aglycones: novel glycopeptides. In: Biochemistry. Band 40, Nr. 15, 2001, S. 4745–4755, doi:10.1021/bi010050w.
- Marianne Abele-Horn: Antimikrobielle Therapie. Entscheidungshilfen zur Behandlung und Prophylaxe von Infektionskrankheiten. Unter Mitarbeit von Werner Heinz, Hartwig Klinker, Johann Schurz und August Stich, 2., überarbeitete und erweiterte Auflage. Peter Wiehl, Marburg 2009, ISBN 978-3-927219-14-4, S. 335–337.
- Santiago Alvarez-Arango, S. Michelle Ogunwole, Thomas D. Sequist, Caitlin M. Burk, Kimberly G. Blumenthal: Vancomycin Infusion Reaction — Moving beyond “Red Man Syndrome”. In: New England Journal of Medicine. Band 384, Nr. 14, 8. April 2021, ISSN 0028-4793, S. 1283–1286, doi:10.1056/NEJMp2031891 (nejm.org [abgerufen am 1. Mai 2021]).
- Vanthida Huang, Nicola A. Clayton, Kimberly H. Welker: Glycopeptide Hypersensitivity and Adverse Reactions. In: Pharmacy. Band 8, Nr. 2, 21. April 2020, ISSN 2226-4787, S. 70, doi:10.3390/pharmacy8020070, PMID 32326261, PMC 7357119 (freier Volltext) – (mdpi.com [abgerufen am 1. Mai 2021]).
- Avoparcin-Verbot in Deutschland durch BgVV initiiert. BfR, abgerufen am 20. Februar 2011.
- A. E. van den Bogaard, N. Bruinsma and E. E. Stobberingh: The effect of banning avoparcin on VRE carriage in The Netherlands. In: Journal of Antimicrobial Chemotherapy. Band 46, Nr. 1. The British Society for Antimicrobial Chemotherapy, 2000, S. 146–148, doi:10.1093/jac/46.1.146 (oup.com [abgerufen am 20. Februar 2011]).
- F. Umstätter, C. Domhan, T. Hertlein, K. Ohlsen, E. Mühlberg, C. Kleist, S. Zimmermann, B. Beijer, K. D. Klika, U. Haberkorn, W. Mier, P. Uhl: Vancomycin Resistance Is Overcome by Conjugation of Polycationic Peptides. In: Angewandte Chemie. Band 59, Nummer 23, 06 2020, S. 8823–8827, doi:10.1002/anie.202002727, PMID 32190958, PMC 7323874 (freier Volltext) (deutschsprachige Version).