Phenylbrenztraubensäure
Phenylbrenztraubensäure ist als Derivat der Brenztraubensäure eine α-Ketosäure und Abbauprodukt der Aminosäure Phenylalanin.
| Strukturformel | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
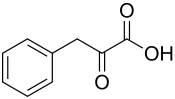 | ||||||||||||||||||||||
| Allgemeines | ||||||||||||||||||||||
| Name | Phenylbrenztraubensäure | |||||||||||||||||||||
| Andere Namen |
| |||||||||||||||||||||
| Summenformel | C9H8O3 | |||||||||||||||||||||
| Kurzbeschreibung |
farbloses bis beiges Pulver[1] | |||||||||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Eigenschaften | ||||||||||||||||||||||
| Molare Masse | 164,16 g·mol−1 | |||||||||||||||||||||
| Aggregatzustand |
fest | |||||||||||||||||||||
| Schmelzpunkt | ||||||||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||||||||
Herstellung und Gewinnung
Eine technische Synthese von Phenylbrenztraubensäure geht vom Benzylchlorid aus, welches mittels Kohlenmonoxid und Dicobaltoctacarbonyl als Katalysator doppelt carbonyliert wird.[3]
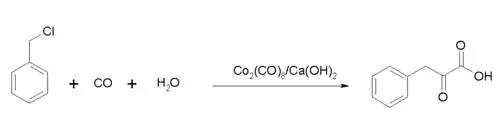
Eigenschaften
Physikalische Eigenschaften
Für die Verbindung kann ein Tautomeriegleichgewicht mit einer Keto- und einer Enolstruktur formuliert werden. In fester Phase können zwei polymorphe Formen auftreten, die bei 155 °C (Form I) und 162 °C (Form II) schmelzen. Form II ist bei Raumtemperatur instabil und wandelt sich innerhalb von zwei Tagen in Form I um. IR- und Raman-spektroskopische Untersuchungen zeigten, dass in beiden festen Formen die Enolstruktur vorliegt.[2] In Lösung hängt die Lage des Tautomeriegleichgewichts von der Art des Lösungsmittels ab. Während in aprotischen Lösungsmitteln wie Tetrachlorkohlenstoff und DMSO die Enolform dominiert, liegt in wässriger Lösung eine durch Hydratation stabilisierte Ketoform vor.[4][5] Mit einem pKS-Wert von 2,54 ist Phenylbrenztraubensäure eine starke Säure.[6]
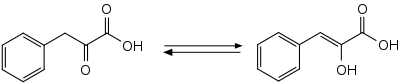
Chemische Eigenschaften
Phenylbrenztraubensäure kann durch die Behandlung mit Ammoniak oder Ammoniumsulfat in wässrigem Medium in racemisches Phenylalanin bzw. dessen Säureamid überführt werden.[7] Die Synthese des enantiomerenreinen (S)-Isomers[8] oder (R)-Isomers[9] gelingt in enzymatischen Reaktionen.
Biologische Bedeutung
Phenylbrenztraubensäure wird bei der angeborenen Stoffwechselstörung Phenylketonurie in hohen Konzentrationen mit dem Urin ausgeschieden. Gibt man der Säure bei der Fölling-Probe Eisen(III)-chlorid bei, tritt eine charakteristische Grünfärbung auf.
Einzelnachweise
- Datenblatt Phenylpyruvic acid, 98% bei Sigma-Aldrich, abgerufen am 27. Dezember 2019 (PDF).
- Ho-Hi Lee, Kouji Kimura, Takatomo Takai, Hitoshi Senda, Akio Kuwae, Kazuhiko Hanai: Polymorphism of phenylpyruvic acid studied by IR, Raman and solid state 13C NMR spectroscopy. In: Spectrochim. Acta A. 55, (1999), S. 2877–2882, doi:10.1016/S1386-1425(99)00109-2.
- W. Bertleff, M. Roeper, X. Sava: Carbonylation In: Ullmann's Encyclopedia of Industrial Chemistry. Wiley-VCH, Weinheim 2007, doi:10.1002/14356007.a05_217.pub2.
- Kazuhiko Hanai, Akio Kuwae, Satoshi Kawai, Yoko Ono: Keto-enol tautomerism and vibrational spectra of phenylpyruvic acids. In: J. Phys. Chem. 93 (1989), S. 6013–6016, doi:10.1021/j100353a016.
- Kazuhiko Hanai, Satoshi Kawai: Vibrational and NMR spectra of phenylpyruvic acid and its salts in aqueous solution. In: J. Mol. Struct. 245 (1991), S. 21–27, doi:10.1016/0022-2860(91)87003-Z.
- N. Kishoref, M. J. Holden, J. B. Tewari, R. N. Goldberg: A thermodynamic investigation of some reactions involving prephenic acid. In: J. Chem. Thermodyn. 31 (1999), S. 211–227, doi:10.1006/jcht.1998.0444.
- Hiroshi Yanagawa, Yumiko Makino, Kazuki Sato, Masato Nishizawa, Fujio Egami: Novel formation of α-amino acid from α-oxo acids and ammonia in an aqueous medium. In: Origins of Life and Evolution of Biospheres. 14 (1984), S. 163–169, doi:10.1007/BF00933654.
- Yasuhisa Asano: Enzymatic Synthesis of (S)-Phenylalanine and Related (S)-Amino Acids by Phenylalanine Dehydrogenase. In: J. L. Barredo (Hrsg.): Methods in Biotechnology. Vol. 17: Microbial Enzymes and Biotransformations. Humana Press, Totowa, NJ, S. 141.
- C. T. Evans, W. Peterson, C. Choma, M. Misawa: Biotransformation of phenylpyruvic acid to l-phenylalanine using a strain of Pseudomonas fluorescens ATCC 11250 with high transaminase activity. In: Applied Microbiology and Biotechnology. 26 (1987), S. 305–312, doi:10.1007/BF00256659.