Pektine
Pektine (auch Pektinstoffe) (v. griech.: πηκτός pektós = fest, geronnen) sind pflanzliche Polysaccharide (Vielfachzucker), genauer Polyuronide, die im Wesentlichen aus α-1,4-glycosidisch verknüpften D-Galacturonsäure-Einheiten bestehen. Ernährungsphysiologisch betrachtet sind Pektine für den Menschen Nahrungsfasern. Viele Mikroorganismen dagegen sind in der Lage, Pektine in ihrem Stoffwechsel zu verwerten. In der Industrie finden Pektine hauptsächlich Verwendung als Geliermittel.
Vorkommen
Pektine kommen in allen höheren Landpflanzen vor. Hier findet man Pektine in allen festeren Bestandteilen, beispielsweise den Stängeln, Blüten, Blättern usw. Die Pektine sind in den Mittellamellen und primären Zellwänden enthalten und übernehmen dort eine festigende und wasserregulierende Funktion. Die Pektinzusammensetzung ist nicht nur von Pflanze zu Pflanze unterschiedlich, sondern hängt ebenso vom Typ und Alter des Pflanzengewebes ab. Besonders pektinreich sind Pflanzenteile mit relativ zähen/harten Bestandteilen, z. B. Citrusfrüchte oder Fruchtstände von Sonnenblumen. Pektinarm hingegen sind weiche Früchte, z. B. Erdbeeren.


Gehalt an Pektinen in Früchten und Gemüse (bezogen auf Frischgewicht):[1]
- Hagebutte ca. 15 % (in der Arzneidroge)[2]
- Apfel 1–1,5 %
- Apfeltrester ca. 15 %
- Quitte 0,5 %[3]
- Orange 0,5–3,5 %
- Citrusschalen (aus Orangen und Zitronen) ca. 30 %
- Aprikose 1 %
- Kirsche 0,4 %
- Möhren 1,4 %
Bei der Extraktion von Pektinen aus den pflanzlichen Geweben werden diese chemisch verändert. Darum werden die nativen pflanzlichen Pektine Protopektine genannt, um sie von den veränderten Pektinen abzugrenzen.
Gewinnung
Weltweit werden etwa 40.000 Tonnen Pektin pro Jahr produziert. Die Gewinnung von Pektin erfolgt aus pflanzlichen Rohstoffen mit hohem Pektingehalt, beispielsweise Apfel-, Citrus- oder Rübentrester. Durch die verschiedenen Ausgangsmaterialien und die je nach Hersteller variierenden Gewinnungsmethoden und Modifikationen entstehen verschiedene Pektintypen mit unterschiedlichen Eigenschaften. Trotz dieser großen Variationsbreite kann man ein Grundschema der Extraktion und Modifikation formulieren:
- Extraktion aller wasserlöslichen Substanzen aus den Rohstoffen mit heißem Wasser;
- Trennung der Pektine von den übrigen wasserlöslichen Substanzen durch Fällung mit Ethanol, Methanol oder Isopropanol;
- Mehrmaliges Zentrifugieren/Filtrieren und Waschen;
- Modifikation mit Salzsäure zur Senkung des Veresterungsgrads oder mit Ammoniak zur Bildung amidierter Pektine;
- Nochmaliges Filtrieren, Waschen und Trocknen liefert ein weißes bis gräuliches Pektinpulver;
- Durch Zusatzstoffe wird das Pektin seinem Einsatzbereich angepasst (z. B. Rohrzucker zur Standardisierung, Puffer-Substanzen zur Regulation des pH-Werts und der Calciumverfügbarkeit).
Chemische Struktur und Eigenschaften
Die Substanzklasse der Pektine tritt in einer Vielzahl von Strukturen auf. Allen gemein ist, dass es sich hierbei um Polysaccharide handelt, deren Hauptbestandteil (zu mind. 65 Gewichts-%) die α-D-Galacturonsäure (pKa-Wert 2,9) als Monomer ist. Diese Galacturonsäure-Monomere sind über α-1,4-, meist auch zu einem geringen Anteil über β-1,4-glycosidische Bindungen miteinander verbunden und bilden so das Rückgrat des Pektinmoleküls.
| Strukturmerkmale verschiedener Pektine |
|---|
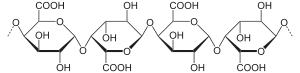 Ausschnitt aus dem Rückgrat von Pektinen: Poly-α-(1→4)-Galacturonsäure. |
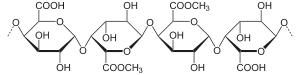 Teilweise veresterter Abschnitt des Rückgrats |
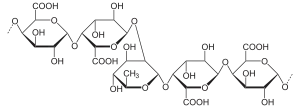 Rhamnogalacturonan: Rückgrat mit „Knick“ durch eingebaute Rhamnose |
Dieses lineare Rückgrat wird periodisch durch 1,2-Bindungen mit α-L-Rhamnose unterbrochen. Daher ist die systematische Bezeichnung für Pektin Rhamno-Galacturonsäure. Der Einbau von Rhamnose-Einheiten führt dazu, dass es in der formal geradlinigen Polygalacturonsäurekette zu Störungen kommt: die Ketten werden „geknickt“. Die Rhamnose-Bausteine in natürlichen Pektinen wiederum tragen oligomere Seitenketten aus den Zuckern Arabinose, Galactose oder Xylose. Diese Neutralzuckerseitenketten können wiederum in Arabinane, Galactane und Arabinogalactan-I sowie Arabinogalactan-II, welches mit Proteinen verknüpft ist, allerdings oft auch zu den Hemicellulosen gezählt wird, unterteilt werden. Die Seitenketten liegen meist zwischen einer und 50 Zuckereinheiten. Bei der industriellen Gewinnung der Pektine gehen diese Seitenketten zum Großteil, jedoch insbesondere die säurelabile Arabinofuranose verloren. Die Verzweigungen in der Kette durch L-Rhamnose und ihre Seitenketten treten nicht regelmäßig auf, sondern häufen sich in den sogenannten hairy regions. Im Gegensatz dazu heißen die linearen Teile der Kette smooth regions.
Neben den Verzweigungen der Hauptkette finden sich weitere Merkmale des Pektinmakromoleküls. Die Hydroxygruppen am C2- oder C3-Atom der Galacturonsäureeinheiten sind zu geringen Teilen acetyliert oder durch weitere Neutralzucker wie D-Galactose, D-Xylose, L-Arabinose oder L-Rhamnose substituiert – auch hier vorwiegend in den hairy regions. Die Carboxygruppen der Polygalacturonsäure sind oft mit Methanol verestert. Der Grad der Veresterung und Acetylierung schwankt mit der Herkunft des Pektins, hat aber entscheidenden Einfluss auf die chemischen Eigenschaften. Deshalb werden Pektine anhand ihres mittleren Veresterungsgrads VE klassifiziert.
Geschichte
Pektin wurde zuerst 1790 von dem französischen Chemiker und Apotheker Louis-Nicolas Vauquelin in Fruchtsäften entdeckt. Seinen Namen erhielt es jedoch erst 1824, als der französische Botaniker und Chemiker Henri Braconnot die Forschungen fortsetzte und die gallertbildende Substanz Pektinsäure nannte. Einhundert Jahre später vermutete dann K. Smolenski als erster, dass Pektin aus polymerer Galakturonsäure bestehen könnte. 1930 wurde dann von Meyer und Mark die Kettenform des Pektinmoleküls erkannt und 1937 von Schneider und Bock eine Formel für Pektin aufgestellt. Erst zu Beginn des 20. Jahrhunderts erkannte man die praktischen Verwendungsmöglichkeiten von Pektinen, die durch ihr gutes Geliervermögen für die Herstellung von Nahrungsmitteln genutzt werden können.[4]
Die wohl bekannteste Marke für pektinhaltige Geliermittel seit 1928 war Opekta.
Klassifizierung der Pektine
Hochmethylierte oder hochveresterte Pektine
- haben per Definition einen Veresterungsgrad größer 50 %,
- gelieren bei einem Zuckergehalt von mindestens 55 Gewichts-%,
- brauchen dafür einen pH-Wert von 1–3,5,
- können also nur in sauren, stark zuckerhaltigen Produkten eingesetzt werden, z. B. in Konfitüren und Fruchtfüllungen.
Niedrigmethylierte, niederveresterte Pektine
- haben per Definition einen Veresterungsgrad von 5–50 %,
- können in Anwesenheit von mehrwertigen Kationen auch ohne Zucker Gelee bilden,
- brauchen dafür einen pH-Wert von 1–7,
- werden zur Herstellung von pumpfähigen Fruchtzubereitungen vor allem für Milchprodukte verwendet.
- werden zur Herstellung von kalorienreduzierten Fruchtaufstrichen verwendet.
Pektinsäuren
- haben per Definition einen Veresterungsgrad kleiner 5 %,
- gelieren wie niedrigmethylierte Pektine (s. o.),
- und fallen bei hohen pH-Werten und großen Gehalten an mehrwertigen Kationen als Pektate, Salze der unveresterten Pektinsäuren, aus.
Amidopektine (amidierte Pektine, E 440ii)
- fallen in die Gruppe der niedrigmethylierten Pektine, wobei ein bestimmter Anteil der Carbonsäure-Gruppen durch die Umsetzung mit Ammoniak als Amid vorliegt,
- gelieren wie niedrigmethylierte Pektine sowohl mit Zucker als auch mit mehrwertigen Kationen,
- die Gelee-Eigenschaften werden aber vom Gehalt an mehrwertigen Kationen, insbesondere Calcium, weniger beeinflusst. Sie sind somit robuster in der Anwendung.
Der anwendungstechnische Hauptunterschied zwischen den Modifikationen liegt in der Neigung, Gele aus wässrigen Lösungen zu bilden, sowie in den Eigenschaften der gebildeten Gele. Mit dem Veresterungsgrad und der Verwendung von weiteren Zusatzstoffen können Geschwindigkeit der Gelbildung, Gelfestigkeit, Aromafreigabe und Streichfestigkeit gezielt gesteuert werden.
Anwendungen
Aufgrund ihrer Fähigkeit, Gele zu bilden, sind Pektine in der Lebensmittelindustrie, der Pharmaindustrie oder für Kosmetika ein unverzichtbarer Bestandteil vieler Produkte, bei denen aus den verschiedenen Gründen Geliermittel, Verdickungsmittel und/oder Stabilisierungsmittel eingesetzt werden.[5] In der Nahrungsmittelindustrie und teils auch im Haushalt wird Pektin zur Herstellung von Gelees, Konfitüren und Marmeladen, Süßwaren, Backwaren, zur Getränkestabilisation und in Milcherzeugnissen verwendet. Pektine können ebenso wie Agar-Agar, Carrageen oder Alginsäure als rein pflanzliches Ersatzmittel von Gelatine dienen.
Niedrig methylierte Pektine finden Anwendung in der Joghurt-Produktion und bei der Pasteurisierung von Sauermilchprodukten, wo die Koagulation des Caseins durch die Anwesenheit von Pektin unterbunden wird.
Sie sind in der EU als Lebensmittelzusatzstoff der Nummer E 440 ohne numerische Höchstmengenbeschränkung (quantum satis) für fast alle Lebensmittel zugelassen. Nicht als Lebensmittelzusatzstoffe in diesem Sinne gelten danach jedoch Erzeugnisse, die Pektin enthalten und aus getrockneten Rückständen ausgepresster Äpfel oder aus getrockneten Schalen von Zitrusfrüchten oder aus einer Mischung daraus durch Behandlung mit verdünnter Säure und anschließender teilweiser Neutralisierung mit Natrium- oder Kaliumsalzen gewonnen wurden („flüssiges Pektin“)[6].
Ihre Eigenschaften als Verdickungsmittel, Schutzkolloide und Stabilisatoren werden auch in der Pharma- und Kosmetikindustrie genutzt, um die Viskosität und Stabilität von Emulsionen und Suspensionen zu erhöhen und verschiedene Gele, Cremes und Pasten zu erzeugen. In Kosmetikartikeln wird es in der Liste der Inhaltsstoffe unter PECTIN (INCI)[7] aufgeführt.
Weitere medizinische Anwendungen der Pektine ergeben sich aus der Fähigkeit, als Komplexbildner bei der Entgiftung von Schwermetallvergiftungen mitzuwirken und durch ihre Eigenschaft, den Cholesterinwert im Blut zu senken. Außerdem werden sie in manchen Medikamenten zur Durchfallbehandlung eingesetzt.
Geliermechanismen
Pektinmoleküle sind Makromoleküle und sollten wegen ihrer hohen Molmasse nur schwer in Wasser zu lösen sein. Tatsächlich aber kann man relativ große Mengen Pektin in nur wenig warmem Wasser lösen. Die Ursache dieses Phänomens sind die freien Carbonsäure-Gruppen der Galacturonsäure-Bausteine. In wässriger Lösung dissoziieren die Säuregruppen. Dadurch entstehen anionische Säurereste, die mehr oder weniger gleichmäßig über das Makromolekül verteilt sind. Die negative Ladung sorgt dafür, dass sich die Pektinmoleküle elektrostatisch abstoßen. Weiterhin bilden sich um diese Ladungsträger große Hydrathüllen, die zusätzlich verhindern, dass sich die Moleküle einander annähern. Auf diese Weise bleiben Pektine in Suspension, weswegen sie der Gruppe der Hydrokolloide zugeordnet werden.
Zum Gelieren muss die Barriere aus elektrostatischer Abstoßung und Hydrathüllen überwunden werden. Dazu gibt es zwei Mechanismen:
Gelierung mit mehrwertigen Kationen
Ein mehrwertiges Kation wird durch zwei oder mehr anionische Carboxylat-Gruppen in einem Chelatkomplex gebunden, so dass sich ein Gel ausbildet, in dem mehrwertige Kationen die Pektinketten in einem dreidimensionalen Netzwerk zusammenhalten. Die Gelierung erfolgt dabei nach dem sogenannten „egg-box“-Modell.
Gelierung mit Zucker und Säure
Die Säure überführt viele der anionischen Säurereste in Säuregruppen, wodurch die elektrostatische Abstoßung zwischen den Pektinketten sinkt. Große Mengen Zucker haben einen wasserentziehenden Effekt, d. h., sie binden auch Wasser aus den großen Hydrathüllen der Pektine. Dadurch können sich die Pektinketten, z. T. auch unter Einbeziehung des Zuckers, einander annähern und bilden ein durch Wasserstoffbrückenbindungen verknüpftes, dreidimensionales Netzwerk aus.
Weblinks
- International Pectin Producers’ Association (IPPA) Internationaler Pektinproduzentenverband
- WHO/JECFA-Spezifikation für Pektin (PDF; 174 kB)
Einzelnachweise
- Eintrag zu Pektine. In: Römpp Online. Georg Thieme Verlag, abgerufen am 2. April 2012.
- Max Wichtl (Hrsg.): Herbal Drugs and Phytopharmaceuticals. CRC Press, London, New Yorck, und weitere 2004, Seite 520 (Rosae pseudofructus cum fructibus).
- Eintrag zu Quitte. In: Römpp Online. Georg Thieme Verlag, abgerufen am 8. Juni 2013.
- Bericht über Pektine (PDF; 621 kB) der Fabrikantin Herbstreith & Fox GmbH & Co. KG, Neuenbürg.
- Pektine. In: Kompaktlexikon der Biologie, Wissenschaft Online; abgerufen am 19. Juli 2010.
- Artikel 3 Abs. 2 S.2 iv) Verordnung (EG) Nr. 1333/2008 des Europäischen Parlaments und dese Rates vom 16. Dezember 2008 über Lebensmittelzusatzstoffe. In ihrem Anhang II Teil E für diverse Lebensmittelgruppen mit Beschränkungen für Pektine
- Eintrag zu PECTIN in der CosIng-Datenbank der EU-Kommission, abgerufen am 23. Oktober 2021.