p-Phenylendiamin
p-Phenylendiamin ist eine chemische Verbindung aus der Gruppe der Phenylendiamine.
| Strukturformel | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
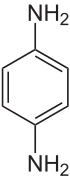 | ||||||||||||||||||||||
| Allgemeines | ||||||||||||||||||||||
| Name | p-Phenylendiamin | |||||||||||||||||||||
| Andere Namen | ||||||||||||||||||||||
| Summenformel | C6H8N2 | |||||||||||||||||||||
| Kurzbeschreibung |
schwer entzündbarer kristallin farblos bis schwach roter Feststoff[2] | |||||||||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Eigenschaften | ||||||||||||||||||||||
| Molare Masse | 108,14 g·mol−1 | |||||||||||||||||||||
| Aggregatzustand |
fest[2] | |||||||||||||||||||||
| Dichte | ||||||||||||||||||||||
| Schmelzpunkt |
140 °C[2] | |||||||||||||||||||||
| Siedepunkt |
267 °C[2] | |||||||||||||||||||||
| Löslichkeit |
löslich in Wasser (40 g·l−1 bei 24 °C)[2] | |||||||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Toxikologische Daten | ||||||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||||||||
Gewinnung und Darstellung
p-Phenylendiamin kann durch mehrere Verfahren synthetisiert werden. Am häufigsten wird 4-Nitrochlorbenzol mit Ammoniak im Sinne einer nukleophilen aromatischen Substitution umgesetzt und das erhaltene 4-Nitroanilin katalytisch hydriert:[4]
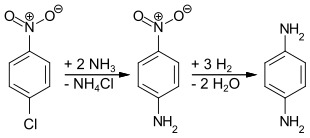
Bei dem von DuPont verwendeten Verfahren wird Anilin mit Stickoxiden diazotiert und das Diazoniumsalz mit überschüssigem Anilin zum 1,3-Diphenyltriazen umgesetzt. Das Triazen wird säurekatalysiert zum 4-Aminoazobenzol umgelagert und dieses zu p-Phenylendiamin und Anilin hydriert.[5]
.svg.png.webp)
Eigenschaften
p-Phenylendiamin ist ein kristalliner, farbloser bis schwach roter Feststoff, der löslich in Wasser ist. Der Flammpunkt liegt bei 156 °C, die Zündtemperatur bei 567 °C und die untere Explosionsgrenze bei 1,5 %.[2]
Verwendung
Die Kunststoffindustrie produziert p-Phenylendiamin in großen Mengen für die Herstellung aromatischer Polyamide. Es ist dort zusammen mit Terephthalsäure wesentlicher Bestandteil der Aramide. p-Phenylendiamin fällt bei der Herstellung von Azofarbstoffen als Zwischenprodukt an. Die Synthesewege einiger Pharmazeutika und Photochemikalien verlaufen ebenso oft über diese Verbindung. Aufgrund seiner färbenden Eigenschaften finden p-Phenylendiamin und einige seiner Derivate in Kosmetika Verwendung (insbesondere für Haarfärbemittel, diese Verwendung wurde 1888 von Ernst Erdmann entdeckt). Vermutlich beruhen viele allergische Reaktionen bei Friseuren auf dem Kontakt mit diesem Farbstoff. In einigen fotografischen Entwicklern ist die alkalische Lösung von p-Phenylendiamin aktive Komponente.[4] Dies wurde 1888 durch Andresen entdeckt.[6]
1863 stellte Haussman fest, dass eine Mischung aus para-Phenylendiamin und einem Oxidationsmittel eine Verfärbung hervorruft. Im Jahre 1883 wurde das erste Patent für die Ausnutzung dieser Beobachtung in der Haarfärbung von Monnet erworben, der tatsächlich 2,5-Diaminotoluol und Wasserstoffperoxid verwendete. Kurz danach wurden Patente von H. und E. Erdmann über den Zeitraum 1888–1897 für die Verwendung als Haarfärbemittel einer Vielzahl von para-Phenylendiaminen und Aminophenolen mit Wasserstoffperoxid erhalten.[7]
p-Phenylendiamin dient als Nachweisreagenz für Flechtensäuren (z. B. Fumarprotocetrarsäure). Dafür kommt eine jeweils frisch zubereitete Lösung von 10 mg p-Phenylendiamin in 10 mL Ethanol zum Einsatz. Neben der Betrachtung im Tageslicht erfolgt die Auswertung per Fluoreszenz im UV365-Licht.[8]
Sicherheitshinweise
p-Phenylendiamin wird zu den Allergenen gezählt, da es bei Hautkontakt zu Reizungen und zur Sensibilisierung führen kann. Ferner wird diese Chemikalie in einigen Urlaubsorten auch zur Farbintensivierung und zum „Schwärzen“ von rotbraunen Henna-Tattoos verwendet.[9] Vermutlich beruhen viele allergische Reaktionen bei Friseuren auf dem Kontakt mit p‑Phenylendiamin-haltigen Haarfärbemitteln.[10][11][12]
Einzelnachweise
- Eintrag zu P-PHENYLENEDIAMINE in der CosIng-Datenbank der EU-Kommission, abgerufen am 20. November 2021.
- Eintrag zu p-Phenylendiamin in der GESTIS-Stoffdatenbank des IFA, abgerufen am 8. Januar 2021. (JavaScript erforderlich)
- Eintrag zu p-phenylenediamine im Classification and Labelling Inventory der Europäischen Chemikalienagentur (ECHA), abgerufen am 30. Dezember 2019. Hersteller bzw. Inverkehrbringer können die harmonisierte Einstufung und Kennzeichnung erweitern.
- Eintrag zu 1,4-Benzenediamine in der Hazardous Substances Data Bank, abgerufen am 21. April 2017 (online auf PubChem).
- Ullmann's Encyclopedia of Industrial Chemistry. Wiley-VCH Verlag & Co. KGaA, 2000, ISBN 978-3-527-30673-2, Phenylene- and Toluenediamines, doi:10.1002/14356007.a19_405.
- Ralph Jacobson, Sidney Ray, Geoffrey G. Attridge, Norman Axford: Manual of Photography. Taylor & Francis, 2000, ISBN 978-1-136-09118-6, S. 275 (eingeschränkte Vorschau in der Google-Buchsuche).
- IARC Monographs: Occupational Exposures of Hairdressers and Barbers and Personal Use of Hair Colourants.
- Egon Stahl, Werner Schild: Isolierung und Charakterisierung von Naturstoffen. 1. Auflage. Gustav Fischer Verlag, Stuttgart/New York 1986, ISBN 3-437-30511-5, S. 174.
- Deutscher Ärzteverlag GmbH, Redaktion Deutsches Ärzteblatt: Henna/p-Phenylendiamin-Kontaktallergie: Folgenschwere Dermatosen nach Henna-Tätowierungen. In: aerzteblatt.de. Deutsches Ärzteblatt, 2001, abgerufen am 5. Dezember 2021.
- BAUA: Begründung zu 2-Nitro-p-phenylendiamin in TRGS 907, Ausgabe: Dezember 2011, Stand: Mai 2011, abgerufen am 5. Dezember 2021
- WELT.de/AFP: Kosmetik: Allergisch vom Haarfärbemittel. In: Welt Online. 2007, abgerufen am 5. Dezember 2021.
- Grundlagen - Allergieinformationsdienst. In: allergieinformationsdienst.de. Abgerufen am 5. Dezember 2021.

