Nitroniumtetrafluoroborat
Nitroniumtetrafluoroborat ist eine chemische Verbindung. Es handelt sich um das Tetrafluorborat-Salz des Nitroniumions.
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
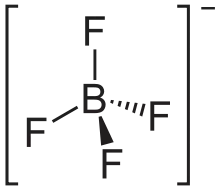 | |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Nitroniumtetrafluoroborat | ||||||||||||||||||
| Summenformel | NO2[BF4] | ||||||||||||||||||
| Kurzbeschreibung |
farbloser Feststoff[1] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 132,81 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
fest | ||||||||||||||||||
| Schmelzpunkt | |||||||||||||||||||
| Löslichkeit |
Zersetzung in Wasser[1] | ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| MAK |
2,5 mg·m−3[1] | ||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||||||||||||
Darstellung
Das Salz kann durch Reaktion von wasserfreier Fluorwasserstoffsäure mit Bortrifluorid und Distickstoffpentoxid in Nitromethan hergestellt werden.[3]
Verwendung
Nitroniumtetrafluoroborat wird als reaktives Reagenz zur Nitrierung von Aromaten verwendet. Nitrierungen laufen mit diesem Salz besser und unter milderen Bedingungen ab als mit dem herkömmlichen Protokoll zur Nitrierung, in welchem Nitroniumionen in situ aus Salpetersäure und Schwefelsäure hergestellt werden. Es nitriert Benzol zu Nitrobenzol[4] und selbst 2,6-Dibrompyridin.[5]
Einzelnachweise
- Datenblatt Nitroniumtetrafluoroborat bei AlfaAesar, abgerufen am 2. März 2010 (PDF) (JavaScript erforderlich).
- Datenblatt Nitronium tetrafluoroborate bei Sigma-Aldrich, abgerufen am 16. April 2011 (PDF).
- K. Schofield: Aromatic nitration. 1. Auflage. Cambridge University Press, Cambridge, ISBN 0-521-23362-3, S. 88.
- J. Buddrus: Grundlagen der Organischen Chemie. 3. Auflage. de Gruyter Verlag, 2003, ISBN 3-11-014683-5, S. 344.
- J. L. Duffy, K. K. Laali: Aprotic Nitration (NO2+BF4−) of 2-Halo- and 2,6-Dihalopyridines and Transfer-Nitration Chemistry of Their N-Nitropyridinium Cations. In: J. Org. Chem. 1991, 56, S. 3006–3009. doi:10.1021/jo00009a015
This article is issued from Wikipedia. The text is licensed under Creative Commons - Attribution - Sharealike. The authors of the article are listed here. Additional terms may apply for the media files, click on images to show image meta data.

