Naturstoff-Nomenklatur
Die Naturstoff-Nomenklatur bezeichnet die chemische Nomenklatur der Naturstoffe. Sie folgt nicht den Richtlinien der systematischen chemischen Nomenklatur, da sie durch die sehr komplexen Strukturen zu sehr langen und nicht praktikablen Namen führen würde. Bestimmte Naturstoffe erhalten ihre Namen von den Autoren, die deren Struktur geklärt und erstmals in der wissenschaftlichen Literatur beschrieben haben. Für diese Stoffe wird ein System verwendet, das auf Trivialnamen für Grundgerüste (engl. skeleton) beruht, an dem die Substituenten ergänzt werden. Unter Substituenten sind sowohl funktionelle Gruppen wie Hydroxyl- oder Oxogruppen als auch Ester kleinerer Säuren sowie Zucker zu verstehen. Diese halbsystematische Nomenklatur ist ebenfalls von der IUPAC akzeptiert.[1] Zwischen der halbsystematischen Nomenklatur und Trivialnamen gibt es fließende Übergänge, sodass für viele Naturstoffe unterschiedliche mehr oder weniger systematische Bezeichnungen gebraucht werden können. Häufig werden die Trivialnamen der Aglyca als Namensbestandteil verwendet, z. B. bei Flavonen oder Terpenglycosiden. Die Gerüste werden nicht unbedingt nach der unter Nomenklatur beschriebenen Methodik benannt. Die Nummerierung basiert auf der Biosynthese oder auf Traditionen (z. B. ist die Bezifferung vieler Diterpene und Triterpene an die Steroidnummerierung angelehnt).
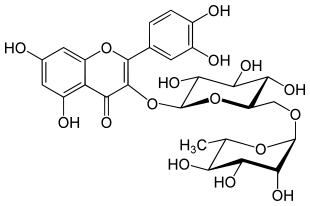
Beispiel Rutin:
- Systematischer Name nach IUPAC: 2-(3,4-dihydroxyphenyl)-5,7-dihydroxy-3-[(2S,3R,4S,5S,6R)-3,4,5-trihydroxy-6-[{(2R,3R,4R,5R,6S)-3,4,5-trihydroxy-6-methyloxan-2-yl}oxymethyl]oxan-2-yl]oxychromen-4-on
- Halbsystematischer Name: 3,3′,4′,5,7-Pentahydroxyflavone 3-O-[α-L-rhamnopyranosyl-(1→6)-β-D-glucopyranosid]
- Abgeleitet vom Aglycon Quercetin: Quercetin-3-O-[α-L-rhamnopyranosyl-(1→6)-β-D-glucopyranosid]
- Zusammengesetzt aus dem Trivialnamen des Aglycons und dem Trivialnamen des Disaccharids: Quercetin-3-rutinosid
Grundgerüste
Im engeren Sinne versteht man unter dem Grundgerüst in der Naturstoffchemie das Kohlenstoffgerüst eines Naturstoffs. Bei vielen Naturstoffklassen werden auch einige hetereocyclische Ringe mit in das Grundgerüst einbezogen. Bei Alkaloiden zählen z. B. alle Ringe, in die Stickstoff integriert ist, ebenfalls zum Grundgerüst, bei Flavonen der Sauerstoff im Pyronring. Nicht zum Grundgerüst, sondern als Substituenten (umgangssprachlich meist als "Reste" bezeichnet) gezählt werden dagegen z. B. Methylendioxyringe an Flavonen oder Lignanen oder zum Chromanring cyclisierte Prenylreste. Viele aromatische Systeme zählen zum Grundgerüst, wenn sie für die Substanzklasse typisch sind. Beispielsweise enthalten Mutterkornalkaloide (Ergoline) einen Indolring, der zum Grundgerüst gerechnet wird. Typische Endung für Alkaloid-Gerüste ist "-in", wobei nicht jeder Naturstoff, der auf "-in" endet, ein Alkaloid bzw. Alkaloidgerüst ist (z. B. Quercetin, oder Cumarin). Bei Terpenen wird als Grundgerüst grundsätzlich nur das gesättigte Kohlenwasserstoffgerüst gewertet, selbst wenn es Vertreter mit aromatischen Ringen gibt. So zählt z. B. die Carnosolsäure zum Diterpen-Grundgerüst der Abietane. Die Namen der Terpengrundgerüste enden daher analog zu den Kohlenwasserstoffen auf "-an". Auch bei der Endung "-an" gibt es aber Naturstoffe bzw. Naturstoffgerüste, die weder Terpen noch gesättigter Kohlenwasserstoff sind, z. B. Lignan.
Prefixe für modifizierte Grundgerüste
Wenn das Grundgerüst durch eine Folgereaktion aus dem Grundgerüst eines anderen Naturstoffs entstanden ist, wird der strukturelle Unterschied manchmal durch Vorsilben beschrieben. Die Nummerierung des ursprünglichen Systems wird dabei beibehalten.
Nor
Die Vorsilbe nor wird verwendet, um das Fehlen eines C-Atoms zu beschreiben. Meistens handelt es sich um fehlende Methylgruppen, die durch oxidativen Abbau (Decarboxylierung) abgespalten wurden. Zum Beispiel wird das vom Tropan abgeleitete Grundgerüst, das am Stickstoff keine N-Methylgruppe, sondern nur ein Proton trägt, als nor-Tropan bezeichnet. Wenn mehr als ein C-Atom im Vergleich zum Grundgerüst fehlt, werden die üblichen aus Ziffernpräfixe der chemischen Nomenklatur verwendet. Limonoide leiten sich von tetracyclischen Triterpenen ab, denen 4 C-Atome aus der an den Fünfring (D-Ring) gebundenen Kette fehlen, daher werden sie auch als Tetra-nor-Triterpene bezeichnet.
Homo
Umgekehrt zu nor wird homo verwendet, also für zusätzlich zum Grundgerüst angefügte Kohlenstoffatome. Homo wird jedoch nur verwendet, wenn das zusätzliche Kohlenstoffatom über eine CC-Verknüpfung an das Grundgerüst angefügt wurde, d. h. N- oder O-Methylierungen zählen als Substituenten und werden nicht als homo bezeichnet. Beispiele für homo-Cholestane sind Ergosterin bzw. Sitosterin, die ein bzw. zwei zusätzliche Kohlenstoffatome in Form einer Methyl- bzw. Ethylgruppe verglichen mit dem Cholesterin aufweisen.
Seco
Wenn eine CC-Bindung gespalten wird, wird die Vorsilbe seco (von seco, lat. zerschneiden) verwendet. Bekanntestes Beispiel sind die Seco-Iridoide, die sich von den Iridoiden durch Spaltung der Bindung zwischen C-6 und C-7 ableiten (vgl. Loganin und Seco-Loganin). Da die Nummerierung des ursprünglichen Gerüstes beibehalten wird, ist sie mitunter nicht auf den ersten Blick als systematisch nachzuvollziehen.
Cyclo
Zusätzlich geschlossene Ringe, die durch Verknüpfung zweier C-Atome gebildet werden, können durch die Vorsilbe cyclo beschrieben werden, z. B. in den 2,2'- bzw. 2,7'- Cyclolignanen, die sich von den Lignanen ableiten. Meist wird das neue Gerüst aber mit einem neuen Namen belegt.
Abeo
Abeo wird verwendet, wenn eine CC-Bindung „verschoben“ wurde. Ein Beispiel sind die vom Taxan abgeleiteten 11(15→1)-Abeo-Taxane. Im Taxan gibt es eine CC-Bindung zwischen C-11 und C-15, im 11(15→1)-Abeo-Taxan liegt stattdessen eine Bindung zwischen den C-Atomen C-11 und C-1 vor.
Epi
Mit dem Präfix epi werden Naturstoffe beschrieben, die sich an einem Stereozentrum von der entsprechenden Grundstruktur unterscheiden. Meist bezieht sich diese Vorsilbe nicht auf die Nomenklatur in Grundgerüsten, sondern in funktionalisierten Naturstoffen. Beispielsweise ist das Epicatechin das Epimere des Catechins. Da im Catechin zwei Stereozentren vorhanden sind, lautet die korrekte Bezeichnung 3-Epi-catechin.
Nummerierung
Die Nummerierung der Grundgerüste richtet sich entweder nach der (vermeintlichen) Biosynthese, orientiert sich an traditionellen Nummerierungen für bereits sehr lange bekannte Naturstoffe oder beginnt an einer häufig vom Entdecker des Gerüstes mehr oder weniger willkürlich festgelegten Position. Die Nummerierung der meisten Naturstoffgrundgerüste ist in der frei verfügbaren Dokumentation zum Dictionary of Natural Products nachzulesen (s. Weblinks).
Beispiele für Biosynthese-basierte Nummerierung
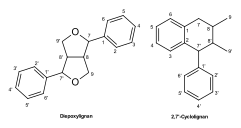
Lignane entstehen durch Dimerisierung von zwei Phenylpropanen. Die Nummerierung nimmt auf diese beiden Bestandteile Bezug und nummeriert sie jeweils von 1 bis 9 bzw. von 1' bis 9'.
Einige Diterpengerüste werden durch Cyclisierung des 14-gliedrigen Cembranrings gebildet. Der Cembranring wird – entsprechend der systematischen IUPAC-Nomenklatur – nummeriert. Diese Systematik wird z. B. im Taxan-System übernommen, während andere Diterpengerüste, die sich ebenfalls vom Cembran ableiten, z. B. Tigliane und Fusicoccoane, anders gezählt werden.
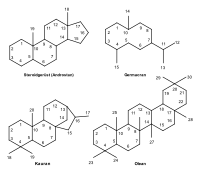
Beispiele für Nummerierung angelehnt an die traditionelle Steroidnummerierung
Viele Sesqui-, Di- und Triterpengerüste werden in Analogie zu Steroiden nummeriert, d. h. oben im A-Ring wird mit 1 begonnen, dann gegen den Uhrzeigersinn beginnend durch das Molekül gezählt. Bei Triterpen und Diterpengerüsten, die ebenfalls ein Dekalinsystem aufweisen, ist die Analogie zum Steroid noch einfach zu erkennen. Bei einigen anderen Gerüsten, z. B. dem 10-Ring-Sesquiterpengerüst Germacran ist es nur noch nachvollziehbar, wenn der Ring in der richtigen Orientierung gezeichnet wird.
Glycoside
Viele Naturstoffe tragen lineare oder verzweigte Zuckerketten als Substituenten. Für die halbsystematische Nomenklatur gibt es ebenfalls Empfehlungen der IUPAC.[2] Für die häufig in Naturstoffen vorkommenden Monosaccharide werden Trivialnamen verwendet. Üblich ist auch die Verwendung von Kürzeln aus drei Buchstaben für die Monosaccharide. Die absolute Stereochemie wird durch D bzw. L beschrieben, die Verknüpfung am anomeren Zentrum durch die α/β-Nomenklatur. Außerdem gibt ein kleines kursives f bzw. p an, ob der Zucker als Pyranose (6-Ring) oder Furanose (Fünfring) vorliegt.
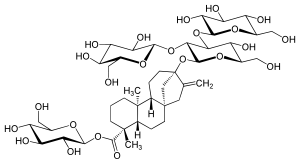
Die Verknüpfung der Zucker in linearen oder verzweigten Ketten wird wie folgt beschrieben:
- Wenn die Zucker nach der Bezeichnung des Grundgerüstes stehen, bekommen sie die Endung „side“, wenn sie davor stehen, wird als Endung „osyl“ verwendet
- Der Zucker, der direkt an das Grundgerüst gebunden ist, steht am Ende der Zuckerkettenbezeichnung
- Verzweigungen werden durch ggf. verschachtelte Klammern voneinander abgegrenzt
Beispiel Rutin (Aglycon Quercetin mit zwei Zuckern): Quercetin 3-O-[α-L-rhamnopyranosyl-(1-6)-β-D-glucoside]
Beispiel Rebaudiosid A (Aglycon Steviol mit einem verzweigten Glycosid aus 3 Glucosen an C-13 des Kaurans und einer einzelnen Glucose als Ester am C-18 des Kaurangerüstes): 19-O-β-D-Glucopyranosyl-13-O-(β-D-glucopyranosyl(1-2)-β-D-glucopyranosyl(1-3))-β-D-glucopyranosyl-13-hydroxykaur-16-en-19-säure
Weblinks
- Die umfangreichste Übersicht der bekannten Naturstoffgrundgerüste findet sich auf der Seite des Dictionary of Natural Products: http://dnp.chemnetbase.com/HelpFiles/DNP_Introduction.pdf, (abgerufen am 16. Januar 2018).
Einzelnachweise
- H. A. Favre, P. M. Giles, K.-H. Hellwich, A. D. McNaught, G. P. Moss: Revised Section F: Natural products and related compounds (IUPAC Recommendations 1999). Corrections and modifications (2004). In: Pure and Applied Chemistry. Band 76, Nr. 6, 1. Januar 2004, doi:10.1351/pac200476061283.
- A. D. McNaught: Nomenclature of carbohydrates (IUPAC Recommendations 1996). In: Pure and Applied Chemistry. Band 68, Nr. 10, 1. Januar 1996, doi:10.1351/pac199668101919.