NMR-Shift-Reagenzien
NMR-Shift-Reagenzien sind chemische Verbindungen, die in der NMR-Spektroskopie eingesetzt werden, um entweder die Auflösung des Spektrums zu erhöhen, oder im Fall der chiralen Shift-Reagenzien, die Unterscheidung von Enantiomeren ermöglicht. Es werden drei Arten von Shift-Reagenzien unterschieden: Derivatisierungsreagenzien, Solvationsreagenzien und Lanthanoid-Shift-Reagenzien.[1]
Derivatisierungsreagenzien
Derivatisierungsreagenzien werden mit dem Analyten umgesetzt, um kovalente Bindungen zu bilden. Voraussetzung dafür sind funktionelle Gruppen, wie Alkohole, Amine oder Carbonsäuren im Analyten. Durch die Derivatisierung entsteht ein neues Molekül, dessen Resonanzen im NMR-Spektrum verschieden zur ursprünglichen Substanz liegen. Die Resonanzen werden also geshiftet und so besser aufgelöst.[1]
Chirale Derivatisierungsreagenzien können zur Strukturaufklärung und zur Bestimmung der optischen Reinheit von chiralen Verbindungen verwendet werden. Dabei werden durch die Derivatisierung die Enantiomere in Diastereomere überführt. Da Diastereomere meist unterschiedliche Eigenschaften aufweisen, können sie durch NMR-Spektroskopie unterschieden werden.
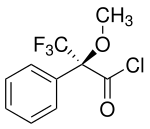
Eines der bekanntesten chiralen Derivatisierungsreagenzien ist die Mosher-Säure. Diese kann in Form des Säurechlorids mit Aminen und Alkoholen umgesetzt werden und bildet dabei Diastereomere.[2] Diese können sowohl mit 1H-NMR-Spektroskopie als auch mit der sensitiveren 19F-Spektroskopie untersucht werden.
Chirale Solvatationsreagenzien
Solvationsreagenzien werden im Gegensatz zu den Derivatisierungsreagenzien nicht mit dem Analyten umgesetzt, sondern bilden, je nach Art des Solvatationsreagenzes, nur Wechselwirkungen, wie Van-der-Waals-Kräfte, dipolare oder ionische Wechselwirkungen aus und bilden so ein Solvat. Racemische Analyten, die in eine enantiomerenreine Umgebung gebracht werden, verhalten sich wie Diastereomere, welche im NMR verschiedene Verschiebungen zeigen können. Einzige strukturelle Voraussetzung für ein chirales Solvations-Reagenz ist die Enantiomerenreinheit.[3] Solvationsreagenzien lassen sich in verschiedene Gruppen einteilen:[4]
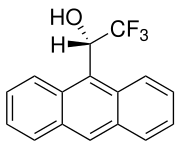
- Solvatationsreagenzien mit niedrigem Molekulargewicht, wie Pirkles Alkohol[5]
- Solvatationsreagenzien, die einen Ionen-Paar-Effekt ausnutzen
- molekulare Pinzetten
- synthetische Makrocyclen
- Cyclodextrine
- Naturstoffe
Der Name suggeriert zwar, dass die Analyten im Solvatationsreagenz gelöst werden, in der Praxis wird jedoch meist ein Verhältnis von 2:1 von Solvatationsreagenz zu Analyt verwendet. Die Substanzmischung wird dann in einem deuterierten Lösungsmittel gelöst und untersucht.
Lanthanoid-Shift-Reagenzien
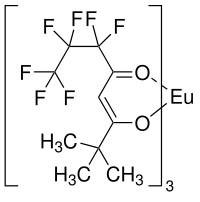
Lanthanoid-Shift-Reagenzien bilden in der Regel keine kovalente Bindung zum Substrat aus, müssen also auch nicht in einer Reaktion umgesetzt werden, sondern können im NMR-Röhrchen mit dem Analyten versetzt werden. Die Interaktion mit dem Analyten findet über Lewis-Säure-Base-Addukte statt. Dafür müssen im Analyten Lewis-basische Zentren, wie z. B. Alkohole, Ether, Amine oder Thiole vorhanden sein.[1] Der Shift der Resonanzen lässt sich durch den Paramagnetismus der Shift-Reagenzien erklären.[6] Da die Shift-Intensität von der räumlichen Struktur des Analyten abhängt, kann auf diesem Weg Strukturaufklärung betrieben werden. Gängige Lanthanoid-Shift-Reagenzien sind z. B. Eu(fod)3 und Eu(dmp)3.
Weiterhin existieren chirale Shift-Reagenzien, wie z. B. Eu(tfc)3 oder Eu(hfc)3, die zur Bestimmung der absoluten Konfiguration eingesetzt werden können.
Einzelnachweise
- Sachin Rama Chaudhari, N Suryaprakash: Recent NMR methodological developments for chiral analysis in isotropic solutions. In: Journal of the Indian Institute of Science. Band 94, Nr. 4, 29. Oktober 2014, S. 485–516.
- James A. Dale, Harry S. Mosher: Nuclear magnetic resonance enantiomer regents. Configurational correlations via nuclear magnetic resonance chemical shifts of diastereomeric mandelate, O-methylmandelate, and .alpha.-methoxy-.alpha.-trifluoromethylphenylacetate (MTPA) esters. In: Journal of the American Chemical Society. Band 95, Nr. 2, Januar 1973, S. 512–519, doi:10.1021/ja00783a034.
- Lu Yang, Thomas Wenzel, R. Thomas Williamson, Melodie Christensen, Wes Schafer: Expedited Selection of NMR Chiral Solvating Agents for Determination of Enantiopurity. In: ACS Central Science. Band 2, Nr. 5, 25. Mai 2016, S. 332–340, doi:10.1021/acscentsci.6b00062, PMID 27280168, PMC 4882744 (freier Volltext).
- Federica Balzano, Gloria Uccello-Barretta, Federica Aiello: Chiral Analysis by NMR Spectroscopy: Chiral Solvating Agents. In: Chiral Analysis. Elsevier, 2018, ISBN 978-0-444-64027-7, S. 367–427, doi:10.1016/b978-0-444-64027-7.00009-4.
- William H. Pirkle, Dennis J. Hoover: NMR Chiral Solvating Agents. In: Topics in Stereochemistry. John Wiley & Sons, Inc., Hoboken, NJ, USA 2007, ISBN 978-0-470-14722-1, S. 263–331, doi:10.1002/9780470147221.ch4.
- Carlos F.G.C. Geraldes: Lanthanides: Shift Reagents. In: Encyclopedia of Inorganic and Bioinorganic Chemistry. John Wiley & Sons, Ltd, Chichester, UK 2012, ISBN 978-1-119-95143-8, S. eibc2050, doi:10.1002/9781119951438.eibc2050.