Lanthanoid-Shift-Reagenzien
Lanthanoid-Shift-Reagenzien sind Verbindungen, die in der NMR-Spektroskopie eingesetzt werden, um Signale zu verschieben (shiften).
Struktur und Reaktivität
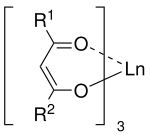
Bei Lanthanoid-Shift-Reagenzien handelt es sich um Komplexe, die aus einem Lanthanoid und drei β-Diketonaten bestehen. Dabei kommen verschieden substituierte Diketonate zum Einsatz. Populär sind vor allem fluorierte Varianten.
Um einen Shift zu induzieren, muss der Komplex paramagnetisch sein. In den gängigen Komplexen der Form LnL3 können allerdings nicht alle Lanthanoide eingesetzt werden, da Lanthan und Lutetium in der Oxidationsstufe +III diamagnetisch sind. Eine weitere Ausnahme bildet Gd(III), dessen sieben f-Elektronen in den sieben f-Orbitalen istotrop verteilt sind und somit nicht zu einem Paramagnetismus führen.[1] Bei der Wahl des Lanthanoids muss nicht nur beachtet werden, wie groß die induzierte Verschiebung ist, sondern auch, ob eine signifikante Peak-Verbreiterung eintritt. In der Praxis haben sich deshalb Europium-Komplexe, um einen Tieffeld-Shift zu induzieren, und Praseodym-Komplexe, um einen Hochfeld-Shift zu induzieren, durchgesetzt.[2]
Für eine erfolgreiche Verwendung in der NMR-Spektroskopie sind vor allem der Kontakt- sowie der Pseudokontakt-Shift wichtig. Kontakt-Shifts entstehen, wenn der Lewis-acide Lanthanoid-Komplex mit Atomen interagiert, die freie Elektronenpaare besitzen und somit Lewis-basisch sind. Kontakt-Shifts entstehen häufig an O-, N-, S- oder P-Atomen. Über die Intensität des Kontakt-Shifts können Rückschlüsse auf die Struktur des Analyten gezogen werden. Während die Wechselwirkung bei Kontakt-Shifts über Bindungen stattfindet, tritt der Pseudokontakt-Shift, eine dipolare Wechselwirkung, durch den Raum auf. Somit ist diese Wechselwirkung nicht auf Lewis-basische Zentren angewiesen und ist auch bei H-, C- und F-Atomen ausgeprägt.[3]
Chirale Shift-Reagenzien
3.svg.png.webp)
Neben den achiralen Lanthanoid-Shift-Reagenzien existieren auch enantiomerenreine Reagenzien. Die Wirkungsweise ist analog zu der der achiralen Varianten, mit dem Unterschied, dass für Enantiomere eine Aufspaltung der Signale auftritt. Bei ausreichender Trennung der Signale der Enantiomere kann durch Integration das Enantiomeren-Verhältnis bestimmt werden und es können Schlüsse auf die absolute Konfiguration gezogen werden. Die Aufspaltung der Signale der Enantiomere beruht darauf, dass sich diastereomere Aggregate bilden, die – im Gegensatz zu Enantiomeren – im NMR unterschieden werden können. Die Aggregatbildung beruht meist auf einer Interaktion zwischen Lewis-Säure und Lewis-Base. Das bekannteste optisch aktive Shift-Reagenz ist das Eu(hfc)3, welches auf enantiomerenreinem Campher basiert.
Verwendung
Die Handhabung der Shift-Reagenzien ist simpel. Die verwendeten Lanthanoid-Komplexe können direkt im NMR-Röhrchen mit dem Analyten versetzt werden. Es muss jedoch möglichst wasserfrei gearbeitet werden, da die Shift-Reagenzien sonst hydrolysieren. Als Lösungsmittel werden nicht-komplexierende Stoffe eingesetzt, wie z. B. CCl4, CDCl3 und CD2Cl2.[2] Am gängigsten ist die Verwendung in 1H-Spektren, Lanthanoid-Shift-Reagenzien finden aber auch bei der Spektroskopie anderer Kerne Anwendung. Während 1H, 13C sowie 19F nur durch dipolare Wechselwirkung Verschiebungen erfahren, können in Spektren von 14N, 15N, 17O oder 31P auch Kontakt-Shifts beobachtet werden.[4]
Historie
.svg.png.webp)
Die grundlegende Entdeckung, dass paramagnetische Substanzen einen Shift in NMR-Spektren induzieren können, wurde 1960 von Taube gemacht. Er untersuchte Wasser und seine Interaktion mit Ionen mittels 17O-NMR-Spektroskopie.[5] 1969 wurde Eu(dmp)3 von Hinckley bei der NMR-spektroskopischen Untersuchung von Cholesterin verwendet.[6] Dies stellt den Beginn der Nutzung der Lanthanoid-Shift-Reagenzien dar. 1970 folgten die ersten enantiomerenreinen Shift-Reagenzien zur Untersuchung von chiralen Verbindungen. Whitesides und Lewis synthetisierten einen Europium(III)-Komplex, der drei auf Campher basierende Liganden trägt.[7] Eine bedeutende Weiterentwicklung der Shift-Reagenzien gelang Rondeau und Sievers. Sie verwendeten 1971 erstmals ein fluoriertes Shift-Reagenz. Verbindungen wie Eu(fod)3 zeichnen sich durch bessere Löslichkeit und höhere Lewis-Acidität aus.[8] Die verbesserten Eigenschaften der fluorierten Shift-Reagnzien inspirierten auch die Forschung auf dem Gebiet der chiralen-Shift-Reagenzien, sodass bereits 1971 ein enantiomerenreines fluoriertes Shift-Reagenz von Fraser, Petit und Saunders synthetisiert und untersucht wurde.[9] Dieses Reagenz ist unter dem Namen Eu(hfc)3 bekannt.
Auf Grund der immer besseren Auflösung der NMR-Spektrometer werden reine Shift-Reagenzien nur noch selten verwendet. Höhepunkt waren die 1970er- und 1980er-Jahre. Chirale Shift-Reagenzien werden immer noch zur Strukturaufklärung und Überprüfung der optischen Reinheit verwendet.
Einzelnachweise
- Carlos F.G.C. Geraldes: Lanthanides: Shift Reagents. In: Encyclopedia of Inorganic and Bioinorganic Chemistry. John Wiley & Sons, Ltd, Chichester, UK 2012, ISBN 978-1-119-95143-8, S. eibc2050, doi:10.1002/9781119951438.eibc2050.
- 8-TECH-7 Lanthanide Induced Shifts (LIS). Abgerufen am 5. Februar 2020.
- B. D. Flockhart, J. Jonas: Lanthanide Shift Reagents in Nuclear Magnetic Resonance Spectroscopy. In: Critical Reviews in Analytical Chemistry. Band 6, Nr. 1, Januar 1976, S. 69–130, doi:10.1080/10408347608542690.
- Anthony F. Cockerill, Geoffrey L. O. Davies, Raymond C. Harden, David M. Rackham: Lanthanide Shift Reagents in Nuclear Magnetic Resonance Spectroscopy. In: Chemical Reviews. Band 73, Nr. 6, Dezember 1973, S. 553–588, doi:10.1021/cr60286a001.
- Jasper A. Jackson, Joe F. Lemons, Henry Taube: Nuclear Magnetic Resonance Studies on Hydration of Cations. In: The Journal of Chemical Physics. Band 32, Nr. 2, Februar 1960, S. 553–555, doi:10.1063/1.1730733.
- Conrad C. Hinckley: Paramagnetic Shifts in Solutions of Cholesterol and the Dipyridine Adduct of Trisdipivalomethanatoeuropium(III). A Shift Reagent. In: Journal of the American Chemical Society. Band 91, Nr. 18, August 1969, S. 5160–5162, doi:10.1021/ja01046a038.
- George M. Whitesides, Daniel William. Lewis: Tris[3-(tert-butylhydroxymethylene)-d-camphorato]europium(III). A reagent for determining enantiomeric purity. In: Journal of the American Chemical Society. Band 92, Nr. 23, November 1970, S. 6979–6980, doi:10.1021/ja00726a049.
- Robert E. Sievers, Roger E. Rondeau: New Superior Paramagnetic Shift Reagents for Nuclear Magnetic Resonance Spectral Clarification. In: Journal of the American Chemical Society. Band 93, Nr. 6, März 1971, S. 1522–1524, doi:10.1021/ja00735a049.
- Robert R. Fraser, Michel A. Petit, John K. Saunders: Determination of enantiomeric purity by an optically active nuclear magnetic resonance shift reagent of wide applicability. In: Journal of the Chemical Society D: Chemical Communications. Nr. 22, 1971, S. 1450, doi:10.1039/c29710001450.