Methylglycol
Methylglycol (Ethylenglycolmonomethylether (EGMM), 2-Methoxyethanol) ist eine farblose, angenehm riechende Flüssigkeit aus der Gruppe der Glycolether, die als Lösungsmittel für Lacke, Farben und Harze eingesetzt wurde.
| Strukturformel | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
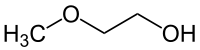 | ||||||||||||||||||||||
| Allgemeines | ||||||||||||||||||||||
| Name | Methylglycol | |||||||||||||||||||||
| Andere Namen | ||||||||||||||||||||||
| Summenformel | C3H8O2 | |||||||||||||||||||||
| Kurzbeschreibung |
farblose Flüssigkeit mit etherischem Geruch[2] | |||||||||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Eigenschaften | ||||||||||||||||||||||
| Molare Masse | 76,10 g·mol−1 | |||||||||||||||||||||
| Aggregatzustand |
flüssig[2] | |||||||||||||||||||||
| Dichte |
0,97 g·cm−3[2] | |||||||||||||||||||||
| Schmelzpunkt | ||||||||||||||||||||||
| Siedepunkt |
124 °C[2] | |||||||||||||||||||||
| Dampfdruck | ||||||||||||||||||||||
| pKS-Wert |
14,8 (25 °C)[3] | |||||||||||||||||||||
| Löslichkeit |
mischbar mit Wasser[2] | |||||||||||||||||||||
| Brechungsindex |
1,4024 (20 °C)[4] | |||||||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Zulassungsverfahren unter REACH |
besonders besorgniserregend: fortpflanzungsgefährdend (CMR)[6] | |||||||||||||||||||||
| MAK | ||||||||||||||||||||||
| Toxikologische Daten | ||||||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Brechungsindex: Na-D-Linie, 20 °C | ||||||||||||||||||||||
Gewinnung und Darstellung
Es bildet sich als Nebenprodukt in großen Mengen bei der Herstellung von Hydroxyethylmethylcellulose (HEMC), das aus alkalisierter Cellulose mit Ethylenoxid und Methylchlorid in einer „Eintopfreaktion“ hergestellt wird.
Eigenschaften
Physikalische Eigenschaften
Ethylenglycolmonomethylether ist eine entzündliche, luftempfindliche farblose Flüssigkeit mit angenehmem Geruch. Der Siedepunkt liegt bei Normaldruck bei 124 °C.[2] Die Dampfdruckfunktion ergibt sich nach Antoine entsprechend log10(P) = A−(B/(T+C)) (P in bar, T in K) mit A = 5,06386, B = 1853,556 und C = −30,838 im Temperaturbereich von 329 bis 396 K.[8] Die Verbindung ist mit Wasser in jedem Verhältnis mischbar.[2] Es bildet mit 84,7 % Wasser ein konstant bei 99,9 °C siedendes Azeotrop. Mit 75 % Toluol erhält man ein konstant bei 105,9 °C siedendes Azeotrop.[9]
Chemische Eigenschaften
Glycolmonoalkylether verhalten sich inert gegenüber Leichtmetallen wie Aluminium oder Magnesium. Am Siedepunkt ist jedoch eine langsame oberflächliche Korrosion zu beobachten.[10]
Sicherheitstechnische Kenngrößen
Ethylenglycolmonomethylether bildet entzündliche Dampf-Luft-Gemische. Die Verbindung hat einen Flammpunkt bei 39 °C.[2][11] Der Explosionsbereich liegt zwischen 2,5 Vol.‑% (80 g/m3) als untere Explosionsgrenze (UEG) und 20 Vol.‑% (630 g/m3) als obere Explosionsgrenze (OEG).[2][11] Der untere Explosionspunkt beträgt 35 °C.[2] Die Grenzspaltweite wurde mit 0,81 mm bestimmt.[2][11] Es resultiert damit eine Zuordnung in die Explosionsgruppe IIB. Die Zündtemperatur beträgt 285 °C.[11][2] Der Stoff fällt somit in die Temperaturklasse T3.
Verwendung
Bis in die 1980er wurde Ethylenglycolmonomethylether als Lösemittel für Lacke und Farben, als Lösemittel bei der Leiterplattenherstellung und für die Färbung von Leder verwendet. Es war in industriellen Lackreinigern und Reinigungsmitteln für Oberflächen enthalten und diente zur Herstellung von ofentrocknenden Industrielacken.[2] Es wurde industriell durch andere ähnliche Lösemittel ersetzt,[12] z. B. durch Methoxypropanol.
Sicherheitshinweise
Methylglycol hat vor allem eine toxische Wirkung auf das Keimepithel des Hodens und die embryonalen und fetalen Gewebe in der Gebärmutter. Methylglycol hat somit eine teratogene Wirkung.
Nach dem Bekanntwerden der fruchtschädigenden Wirkung dieses Stoffes hat ein Substitutionsprozess stattgefunden, der dazu geführt hat, dass dieses Lösungsmittel für Lacke in Konsumprodukten nicht mehr und in Industrielacken nur noch in geringen Mengen verwendet wird.
Einzelnachweise
- Eintrag zu METHOXYETHANOL in der CosIng-Datenbank der EU-Kommission, abgerufen am 16. April 2020.
- Eintrag zu Ethylenglykolmonomethylether in der GESTIS-Stoffdatenbank des IFA, abgerufen am 20. Januar 2022. (JavaScript erforderlich)
- David R. Lide (Hrsg.): CRC Handbook of Chemistry and Physics. 90. Auflage. (Internet-Version: 2010), CRC Press/Taylor and Francis, Boca Raton, FL, Dissociation Constants of Organic Acids and Bases, S. 8-43.
- David R. Lide (Hrsg.): CRC Handbook of Chemistry and Physics. 90. Auflage. (Internet-Version: 2010), CRC Press/Taylor and Francis, Boca Raton, FL, Physical Constants of Organic Compounds, S. 3-330.
- Eintrag zu 2-methoxyethanol im Classification and Labelling Inventory der Europäischen Chemikalienagentur (ECHA), abgerufen am 1. Februar 2016. Hersteller bzw. Inverkehrbringer können die harmonisierte Einstufung und Kennzeichnung erweitern.
- Eintrag in der SVHC-Liste der Europäischen Chemikalienagentur, abgerufen am 18. Oktober 2015.
- Schweizerische Unfallversicherungsanstalt (Suva): Grenzwerte – Aktuelle MAK- und BAT-Werte (Suche nach 109-86-4 bzw. Methylglycol), abgerufen am 2. November 2015.
- J. Pick, V. Fried, E. Hala, O. Vilim: Der Dampfdruck des Äthylenglykolmonomethyläthers und des Äthylenglykolmonoäthylathers. In: Collect. Czech. Chem. Commun. 21, 1956, S. 260–261, doi:10.1135/cccc19560260.
- Datenbank für Azeotrope, Zusammensetzung in mol%
- C. Yoshimura, T. Ogura In: Keikinzoku. 32, 1982, S. 443–450. Es ist hierbei unklar, ob Luftsauerstoff ausgeschlossen worden war. Wasserzusatz unterdrückte die Aluminiumkorrosion, beschleunigte die Magnesiumkorrosion. (Journal of Japan Institute of Light Metals).
- E. Brandes, W. Möller: Sicherheitstechnische Kenngrößen. Band 1: Brennbare Flüssigkeiten und Gase. Wirtschaftsverlag NW – Verlag für neue Wissenschaft GmbH, Bremerhaven 2003.
- BASF – Lösemittelübersicht.


