Lithiumoxid
Lithiumoxid ist eine chemische Verbindung, die aus Lithium und Sauerstoff aufgebaut ist. Es wird zur Herstellung von Lithiumniobat sowie als Zusatzstoff in Keramiken und Gläsern benutzt.
| Kristallstruktur | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
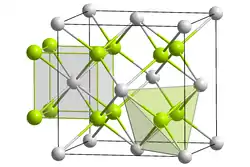 | |||||||||||||||||||
| _ Li+ _ O2− | |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Lithiumoxid | ||||||||||||||||||
| Andere Namen |
Dilithiumoxid, Lithia[1] | ||||||||||||||||||
| Verhältnisformel | Li2O | ||||||||||||||||||
| Kurzbeschreibung |
weißer, geruchloser Feststoff[2] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 29,88 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
fest | ||||||||||||||||||
| Dichte |
2,01 g·cm−3[2] | ||||||||||||||||||
| Schmelzpunkt | |||||||||||||||||||
| Löslichkeit | |||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||||||||||||
Gewinnung und Darstellung
Lithiumoxid kann durch Verbrennung von Lithium oder durch thermische Zersetzung von Lithiumperoxid oder Lithiumhydroxid hergestellt werden.[5][6]
Eigenschaften
Lithiumoxid ist ein weißer, geruchloser Feststoff. Er hat eine Kristallstruktur vom Anti-Flussspat-Typ (a = 4,611 Å).[6] Die Standardbildungsenthalpie von Lithiumoxid beträgt ΔHf0 = −599,1 kJ/mol.[7]
Verwendung
Lithiumoxid dient als Ausgangsstoff zur Herstellung von Lithiumniobat.[8] Des Weiteren kann es als Zusatzstoff zur Herstellung von Keramiken und Gläsern eingesetzt werden.[9] Auch in Fusionsreaktoren kann es eingesetzt werden.[10]
Einzelnachweise
- https://www.chemicalbook.com/ChemicalProductProperty_DE_CB7164125.htm
- Datenblatt Lithiumoxid bei AlfaAesar, abgerufen am 15. Dezember 2010 (PDF) (JavaScript erforderlich).
- Datenblatt Lithium oxide bei Sigma-Aldrich, abgerufen am 8. April 2011 (PDF).
- George K. Schweitzer, Lester L. Pesterfield: The Aqueous Chemistry of the Elements. Oxford University Press, 2010, ISBN 978-0-19-974219-6, S. 100 (eingeschränkte Vorschau in der Google-Buchsuche).
- A. F. Holleman, E. Wiberg, N. Wiberg: Lehrbuch der Anorganischen Chemie. 101. Auflage. Walter de Gruyter, Berlin 1995, ISBN 3-11-012641-9, S. 1152.
- Georg Brauer (Hrsg.), unter Mitarbeit von Marianne Baudler u. a.: Handbuch der Präparativen Anorganischen Chemie. 3., umgearbeitete Auflage. Band II, Ferdinand Enke, Stuttgart 1978, ISBN 3-432-87813-3, S. 951.
- A. F. Holleman, E. Wiberg, N. Wiberg: Lehrbuch der Anorganischen Chemie. 101. Auflage. Walter de Gruyter, Berlin 1995, ISBN 3-11-012641-9, S. 1176.
- Doktorarbeit Ulrich Grusemann.
- Vorlesungsskript (PDF; 35 kB).
- Risely Technical Service Report: The use of lithium oxide as the breeder in fusion reactors. Juli 1989, S. 30.
