Kupferron
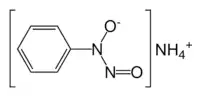
Kupferron ist das Ammoniumsalz von N-Nitroso-N-phenylhydroxylamin, das als Reagenz für die Komplexierung von Metallionen verwendet wird. Das Anion bindet dabei als zweizähniger Ligand über die beiden Sauerstoffatome die Metallionen in einem Fünfring. Die Verbindung wurde 1909 von Oskar Baudisch in die quantitative Analytik von Kupfer- und Eisenionen eingeführt.[4]
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Kupferron | ||||||||||||||||||
| Andere Namen |
| ||||||||||||||||||
| Summenformel | C6H9N3O2 | ||||||||||||||||||
| Kurzbeschreibung |
hellgelber, kristalliner Feststoff[1] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 155,15 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
fest | ||||||||||||||||||
| Schmelzpunkt | |||||||||||||||||||
| Löslichkeit |
schwer in Wasser (< 1 g·l−1 bei 18,5 °C)[2] | ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||||||||||||
Gewinnung und Darstellung
Kupferron wird in einer mehrstufigen Reaktion aus Phenylhydroxylamin hergestellt. Dieses wird zunächst mit Ammoniak in das Ammoniumsalz überführt und dann mit Amylnitrit umgesetzt:[5]
Verwendung
Kupferron wird zur Fällung von Metallionen wie Kupfer, Eisen, Titan, Vanadium, Thorium, Cer, Cobalt, Aluminium, Zink oder Zinn verwendet. Die sich bildenden Metallkupferronate sind schwer löslich in Wasser, aber leicht löslich in organischen Lösungsmitteln. Es wird daher zur Abtrennung von unerwünschten Elementen vor der quantitativen Bestimmung genutzt.[6][7]
Literatur
- C. S. Marvel: Cupferron In: Organic Syntheses. 4, 1925, S. 19, doi:10.15227/orgsyn.004.0019; Coll. Vol. 1, 1941, S. 1 (PDF).
- D. van der Helm, Lynne L. Merritt jr., Robert Degeilh, Caroline H. MacGillavry: The crystal structure of iron cupferron Fe(O2N2C6H5)3. In: Acta Cryst. 18, 1965, S. 355–362; doi:10.1107/S0365110X65000816.
Einzelnachweise
- Datenblatt Cupferron bei Sigma-Aldrich, abgerufen am 22. März 2015 (PDF).
- Eintrag zu Cupferron bei ChemicalBook, abgerufen am 22. März 2015.
- Eintrag zu Kupferron in der GESTIS-Stoffdatenbank des IFA, abgerufen am 8. Januar 2021. (JavaScript erforderlich)
- K. Schröder: Die Verwendung des Cupferrons in der quantitativen Analyse. In: Zeitschrift für Analytische Chemie. Band 61, Nr. 1–2, Januar 1922, S. 60–66, doi:10.1007/bf02425240.
- K. H. Slotta, K. R. Jacobi: Herstellung organischer Reagenzien im analytischen Laboratorium. II. „Kupferron“ (Ammoniumsalz des Nitrosophenylhydroxylamins). In: Zeitschrift für Analytische Chemie. Band 80, Nr. 3–4, März 1930, S. 97–103, doi:10.1007/BF01365065.
- Eintrag zu Cupferron in den Report on Carcinogens, Thirteenth Edition.
- Othmar G. Koch, Gertrud A. Koch-Dedic: Handbuch der Spurenanalyse: Die Anreicherung und Bestimmung von Spurenelementen unter Anwendung chemischer, physikalischer und mikrobiologischer Verfahren. Springer, 1964, ISBN 978-3-642-65423-7, S. 255 ff.

