Kupfer(I)-bromid
Kupfer(I)-bromid ist ein Kupfersalz des Bromwasserstoffs mit der Verhältnisformel CuBr. Kupfer besitzt hierbei die Oxidationsstufe +1.
| Kristallstruktur | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
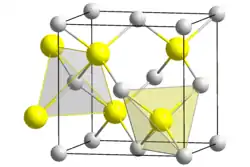 | ||||||||||||||||
| _ Cu+ _ Br− | ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | Kupfer(I)-bromid | |||||||||||||||
| Verhältnisformel | CuBr | |||||||||||||||
| Kurzbeschreibung |
rein weiße Kristalle[1] | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 143,45 g·mol−1 | |||||||||||||||
| Aggregatzustand |
fest | |||||||||||||||
| Dichte | ||||||||||||||||
| Schmelzpunkt | ||||||||||||||||
| Siedepunkt | ||||||||||||||||
| Löslichkeit |
schwerlöslich in Wasser[1] | |||||||||||||||
| Brechungsindex |
2,117[4] | |||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Brechungsindex: Na-D-Linie, 20 °C | ||||||||||||||||
Darstellung
Kupfer(I)-bromid kann durch die Reaktion elementaren Kupfers mit Bromwasserstoffsäure hergestellt werden. Dazu wird elementaren Kupfer mit einer etherischen Lösung von HBr umgesetzt und das entstehende HCuBr2 mit Waser zersetzt[6]
Eine weitere Synthesemöglichkeit besteht in der Reduktion von Kupfer(II)-bromid. Als Reduktionsmittel können beispielsweise Sulfitverbindungen dienen.
Diese Reduktion kann auch beim Kochen des Kupfer(II)-bromids in saurer Lösung mit einem Überschuss an Kupfer erfolgen.[3]
Ebenfalls möglich ist die Synthese durch Reaktion von Kupfersulfat-Pentahydrat mit Kaliumbromid und Schwefeldioxid.[1]
Eigenschaften
Das eigentliche Salz ist farblos. Seine grünliche Farbe erhält es aus Verunreinigungen von Kupfer(II)-Ionen. Kupfer(I)-bromid ist unlöslich in den meisten Lösungsmitteln. Es ist schwerlöslich in Wasser, aber löslich in Halogenwasserstoffsäuren, Salpetersäure und wässrigem Ammoniak. Kupfer(I)-bromid tritt in drei Modifikationen auf. Unterhalb von 391 °C liegt es als γ-CuBr mit einer Kristallstruktur vom Zinkblende-Typ und der Raumgruppe F43m (Raumgruppen-Nr. 216) (a = 5,691 Å) vor. β-CuBr mit einer Kristallstruktur vom Wurtzit-Typ liegt zwischen 391 °C und 470 °C vor. α-CuBr mit einer kubischen Kristallstruktur oberhalb 470 °C.[1]
 Kupfer(I)-bromid
Kupfer(I)-bromid-bromide-sample.jpg.webp) Kupfer(I)-bromid (oxidiert)
Kupfer(I)-bromid (oxidiert)
Verwendung
Ein Einsatzgebiet von Kupfer(I)-bromid ist die Sandmeyer-Reaktion. Hier wird es als Katalysator zur Synthese von Arylbromiden aus Arylaminen über die entsprechenden Diazoniumsalze eingesetzt.[3] Bei thermischer Anregung erzeugt gasförmiges Kupfer(I)-bromid blaues Licht, das eine höhere Farbsättigung aufweist als das durch Kupfer(I)-chlorid emittierte Licht.[7] Kupfer(I)-bromid ist daher ein geeigneter Emitter für pyrotechnische Leuchtsätze.
Literatur
- Wiberg, E.; Wiberg, N.; Holleman, A.F.: Anorganische Chemie, 103. Auflage, 2017 Walter de Gruyter GmbH & Co. KG, Berlin/Boston, ISBN 978-3-11-026932-1, S. 1696.
Einzelnachweise
- Georg Brauer (Hrsg.), unter Mitarbeit von Marianne Baudler u. a.: Handbuch der Präparativen Anorganischen Chemie. 3., umgearbeitete Auflage. Band II, Ferdinand Enke, Stuttgart 1978, ISBN 3-432-87813-3, S. 974.
- Datenblatt Kupfer(I)-bromid bei AlfaAesar, abgerufen am 3. Februar 2010 (PDF) (JavaScript erforderlich)..
- Yoffe, D.; Frim, R.; Ukeles, S.D.; Dagani, M.J.; Barda, H.J.; Benya, T.J.; Sanders, D.C.: Bromine Compounds. In: Ullmanns Enzyklopädie der Technischen Chemie, Wiley-VCH Verlag GmbH & Co. KGaA, Weinheim 2013; doi:10.1002/14356007.a04_405.pub2.
- David R. Lide (Hrsg.): CRC Handbook of Chemistry and Physics. 90. Auflage. (Internet-Version: 2010), CRC Press/Taylor and Francis, Boca Raton, FL, Index of Refraction of Inorganic Crystals, S. 10-246.
- Datenblatt Copper(I) bromide bei Sigma-Aldrich, abgerufen am 5. Januar 2022 (PDF).
- Hollemann Wieberg: Lehrbuch der Anorganischen Chemie. 91.-100. Auflage. Walter de Gruyter, Berlin New York 1985, ISBN 3-11-007511-3, S. 1003.
- E.-C. Koch: Spectral Investigation and Color Properties of Copper(I) Halides CuX (X=F, Cl, Br, I) in Pyrotechnic Combustion Flames, Propellants, Explos. Pyrotech. 2015, 40, 799–802. doi:10.1002/prep.201500231.


