Germanium(II)-bromid
Germanium(II)-bromid ist eine anorganische chemische Verbindung des Germaniums aus der Gruppe der Bromide.
| Kristallstruktur | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
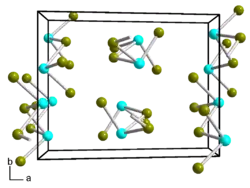 | ||||||||||||||||
| _ Ge2+ _ Br− | ||||||||||||||||
| Kristallsystem |
monoklin | |||||||||||||||
| Raumgruppe |
P21/c (Nr. 14) | |||||||||||||||
| Gitterparameter |
a = 11,68 Å, b = 9,12 Å, c = 7,02 Å, β = 101,9° | |||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | Germanium(II)-bromid | |||||||||||||||
| Andere Namen |
Germaniumdibromid | |||||||||||||||
| Verhältnisformel | GeBr2 | |||||||||||||||
| Kurzbeschreibung |
weißer bis blassgelber Feststoff[1] | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 232,45 g·mol−1 | |||||||||||||||
| Aggregatzustand |
fest[2] | |||||||||||||||
| Schmelzpunkt | ||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||
Gewinnung und Darstellung
Germanium(II)-bromid kann durch Reaktion von Germanium(IV)-bromid mit Germanium oder Zink[3] gewonnen werden.[1]
Ebenfalls möglich ist die Darstellung durch thermische Dissoziation von Tribromgerman im Vakuum oder Einengen einer Lösung von Germanium(II)-oxid in 46-prozentiger Bromwasserstoffsäure. Es kann auch als Rückstand der Destillation einer Lösung von Tribromgerman in Bromwasserstoffsäure oder auch als Rückstand der Destillation einer etherischen Lösung des aus Germanium(II)-oxid mit 40 % Bromwasserstoff in Ether erhältlichen GeHBr3-(C2H5)2O erhalten werden.[1] Zuerst wurde Germanium(II)-bromid durch Umsetzung von Germanium mit Bromwasserstoff und anschließender Reduktion des entstehenden Gemisches aus GeBr4 und GeHBr3 mit metallischem Zink hergestellt.[4]
Eigenschaften
Germanium(II)-bromid ist ein polymerer farbloser bis blassgelber Feststoff, der in Ethanol und Aceton löslich ist. Bei 180–220 °C erfolgt an Luft Oxidation. Er disproportioniert beim Erhitzen in unpolaren Lösungsmitteln zu Germanium(IV)-bromid und Subbromiden, beim trockenen Erhitzen bilden sich Germanium(IV)-bromid und Germanium.[1][4] Mit Wasser hydrolysiert er zu Germanium(II)-hydroxid.[3] Germanium(II)-bromid kristallisiert in einer monoklinen Struktur, Raumgruppe P21/c (Raumgruppen-Nr. 14), mit den Gitterparametern a = 11,68 Å, b = 9,12 Å, c = 7,02 Å und β = 101,9°.[5] In der Kristallstruktur ist jedes Germaniumatom an drei Bromatome gebunden, von denen zwei an weitere Germaniumatome binden, so dass sich eine Kettenstruktur ergibt.
Einzelnachweise
- Georg Brauer (Hrsg.), unter Mitarbeit von Marianne Baudler u. a.: Handbuch der Präparativen Anorganischen Chemie. 3., umgearbeitete Auflage. Band I, Ferdinand Enke, Stuttgart 1975, ISBN 3-432-02328-6, S. 724.
- Datenblatt Germanium(II) bromide, 97% bei Sigma-Aldrich, abgerufen am 9. Mai 2017 (PDF).
- A. F. Holleman, E. Wiberg, N. Wiberg: Lehrbuch der Anorganischen Chemie. 101. Auflage. Walter de Gruyter, Berlin 1995, ISBN 3-11-012641-9, S. 959.
- L. M. Dennis: Germanium. Zusammenfassung der Untersuchungen im Department of Chemistry, Cornell University, 1921-1927. In: Zeitschrift fÜr anorganische und allgemeine Chemie. Band 174, Nr. 1, 2. August 1928, S. 97, doi:10.1002/zaac.19281740114.
- Roland C. Rouse, Donald R. Peacor, Bruce R. Maxim: The crystal structure of germanium dibromide*. In: Zeitschrift für Kristallographie - Crystalline Materials. Band 145, Nr. 3-4, 1. Januar 1977, ISSN 2194-4946, doi:10.1524/zkri.1977.145.3-4.161.
