Flibanserin
Flibanserin ist ein Arzneistoff, der ursprünglich zur Behandlung von Depressionen entwickelt wurde, sich in diesem Bereich aber als unwirksam erwies, und nun zur Behandlung der hypoaktiven Sexualfunktionsstörung (HSDD) bei Frauen neu zugelassen wurde – die Wirksamkeit ist jedoch auch hier nicht bestätigt, was bereits zu vielen Kontroversen um das Thema Flibanserin (Addyi) und dessen angeblicher Wirkung geführt hat.
| Strukturformel | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
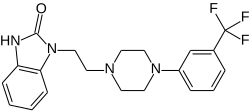 | ||||||||||||||||||||||
| Allgemeines | ||||||||||||||||||||||
| Freiname | Flibanserin | |||||||||||||||||||||
| Andere Namen |
| |||||||||||||||||||||
| Summenformel | C20H21F3N4O | |||||||||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Eigenschaften | ||||||||||||||||||||||
| Molare Masse | 390,40 g·mol−1 | |||||||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||||||||
Pharmakologische Eigenschaften
Wirkungsmechanismus (Pharmakodynamik)
Auf molekularer Ebene vermittelt Flibanserin seine pharmakologischen Effekte über Serotonin- und Dopamin-Rezeptoren. Flibanserin ist ein Agonist am Serotonin-Rezeptor 5-HT1A und ein Antagonist an 5-HT2A. Am Dopamin-Rezeptor D4 verhält sich Flibanserin als ein schwacher Partialagonist. Über diese Mechanismen beeinflusst Flibanserin die Freisetzung von Neurotransmittern im Gehirn, die an der Steuerung von Sexualfunktionen beteiligt sind. So hemmt es einerseits die Freisetzung des sexualitätshemmenden Serotonins und steigert andererseits die Freisetzung der sexualitätssteigernden Neurotransmitter Dopamin und Noradrenalin.[2]
Pharmakokinetik
Aus oralen Darreichungsformen wird Flibanserin zu über 90 % in Form des aktiven Arzneistoffs oder seiner Stoffwechselprodukte (Metabolite) in den systemischen Kreislauf aufgenommen. Sein Verteilungsvolumen beträgt etwa 180 Liter. Flibanserin wird über das Cytochrom-P450-Enzymsystem verstoffwechselt, wobei das Isoenzym CYP3A4 die wichtigste Rolle spielt. Eine Verstoffwechslung ist ferner auch über CYP2D6 möglich. Die Hauptprodukte der Verstoffwechslung sind die pharmakologisch inaktiven Metabolite Flibanserin-6-sulfat und Flibanserin-6,21-disulfat. Flibanserin und seine Metabolite werden zu nahezu gleichen Teilen über die Galle und den Urin ausgeschieden. Die terminale Plasmahalbwertzeit von Flibanserin beträgt etwa 10 Stunden und unter Einbeziehung seiner Metabolite etwa 66 Stunden.[3]
Analytik
Die zuverlässige qualitative und quantitative Bestimmung von Flibanserin in unterschiedlichen Untersuchungsmaterialien gelingt nach adäquater Probenvorbereitung durch Kopplung der HPLC mit der Massenspektrometrie.[4]
Klinische Angaben
Wechselwirkungen mit anderen Arzneistoffen
Da Flibanserin über das Cytochrom-P450-Enzymsystem verstoffwechselt wird, besteht das Risiko einer möglichen Wechselwirkung mit Hemmstoffen und Induktoren dieses Enzymsystems. So führt die gleichzeitige Einnahme des CYP3A4-Hemmers Ketoconazol zu einem deutlichen Anstieg des Flibanserinspiegels im Blut und einer verschlechterten Verträglichkeit. Eine Zunahme der Flibanserin-Nebenwirkungen konnte auch bei gleichzeitiger Anwendung von Serotonin-Wiederaufnahmehemmern, Triptanen, der Antibabypille und Alkohol beobachtet werden.[3]
Unerwünschte Wirkungen (Nebenwirkungen)
In klinischen Studien traten häufig (>10 %) Schwindel, Müdigkeit und Übelkeit auf. Gelegentlich (1 bis 10 %) konnten Schlaflosigkeit, Angstzustände, Mundtrockenheit, Abdominalschmerzen, Verstopfungen, nächtliches Harnlassen, Palpitation und Stress als Nebenwirkungen beobachtet werden. Das Risiko einer Synkope kann unter Flibanserin erhöht sein. Ebenso kann das Unfall- und Verletzungsrisiko nach Einnahme von Flibanserin wegen seiner sedierenden Nebenwirkungen erhöht sein.[3]
Klinische Entwicklung und Zulassung
Flibanserin wurde zunächst von Boehringer Ingelheim entwickelt und in insgesamt sieben klinischen Studien der Phase III getestet. In den zwei wichtigsten Studien konnte zwar eine statistische Überlegenheit gegenüber Placebo bezüglich der sexuellen Befriedigung gezeigt werden, jedoch konnte keine Verbesserung des Sexualverlangens nachgewiesen werden.[3]
Der Beraterausschuss der US-amerikanischen Arzneimittelzulassungsbehörde Food and Drug Administration (FDA) sah die Wirksamkeit durch die Studiendaten nicht ausreichend belegt und kritisierte gleichzeitig die vergleichsweise schlechte Verträglichkeit. Der Ausschuss empfahl somit, Flibanserin nicht für die Behandlung hypoaktiver Sexualfunktionsstörungen zuzulassen, und forderte weitere Wirksamkeits- und Sicherheitsbelege an.[5] Im Oktober 2010 gab Boehringer bekannt, die Entwicklung von Flibanserin vorerst einzustellen.[6] Das US-amerikanische Unternehmen Sprout Pharmaceuticals übernahm daraufhin die Weiterentwicklung des Präparates, das im August 2015 durch die FDA für den US-amerikanischen Markt zugelassen wurde.[7][8] Unmittelbar nach der Zulassung wurde Sprout Pharmaceuticals vom kanadischen Pharmaunternehmen Valeant übernommen.[9]
In Europa besteht keine Arzneimittelzulassung.
Mediale Rezeption
In den Medien wurde in Zusammenhang mit Flibanserin häufig von „Viagra für Frauen“ oder englisch „Female Viagra“ gesprochen. Dieser Vergleich ist jedoch in Bezug auf Indikation und Wirkung nicht zutreffend.
Handelspräparate
Addyi (USA)
Einzelnachweise
- Für diesen Stoff liegt noch keine harmonisierte Einstufung vor. Wiedergegeben ist eine von einer Selbsteinstufung durch Inverkehrbringer abgeleitete Kennzeichnung von 1,3-Dihydro-1-(2-(4-(3-(trifluoromethyl)phenyl)-1-piperazinyl)ethyl)-2H-benzimidazol-2-on im Classification and Labelling Inventory der Europäischen Chemikalienagentur (ECHA), abgerufen am 27. März 2020.
- F. Borsini, K. Evans, K. Jason, F. Rohde, B. Alexander, S. Pollentier: Pharmacology of flibanserin. In: CNS Drug Rev. Band 8, Nr. 2, 2002, S. 117–142, PMID 12177684.
- Division of Reproductive and Urologic Products Office of New Drugs Center for Drug Evaluation and Research, Food and Drug Administration: Background Document for Meeting of Advisory Committee for Reproductive Health Drugs (June 18, 2010). NDA 22-526. Flibanserin. (Proposed trade name: Girosa). Boehringer Ingelheim. (PDF; 3,9 MB) 20. Mai 2010, abgerufen am 3. Juli 2010.
- M. Poplawska, A. Blazewicz, P. Zolek, Z. Fijalek: Determination of flibanserin and tadalafil in supplements for women sexual desire enhancement using high-performance liquid chromatography with tandem mass spectrometer, diode array detector and charged aerosol detector. In: J Pharm Biomed Anal. 94, Jun 2014, S. 45–53. PMID 24531007
- D. Biermann: Flibanserin fällt bei FDA durch. In: Pharmazeutische Zeitung. Nr. 26, 2010 (pharmazeutische-zeitung.de).
- Pharmakonzern stoppt Lustpille für die Frau. In: Spiegel online. 8. Oktober 2010.
- FDA approves first treatment for sexual desire disorder. Pressemitteilung der FDA, 18. August 2015.
- Sprout Pharmaceuticals Receives FDA Approval of ADDYI™ (Flibanserin 100 MG) (Memento des Originals vom 20. August 2015 im Internet Archive) Info: Der Archivlink wurde automatisch eingesetzt und noch nicht geprüft. Bitte prüfe Original- und Archivlink gemäß Anleitung und entferne dann diesen Hinweis., PM Sprout Pharmaceuticals vom 18. August 2015, abgerufen am 19. August 2015.
- Übernahme von Sprout Pharmaceuticals : Valeant schluckt Hersteller der Lustpille. (Memento vom 20. August 2015 im Internet Archive) auf: tagesschau.de, 20. August 2015.