Fenpropimorph
Fenpropimorph ist eine racemische chemische Verbindung aus der Gruppe der Morpholine.
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
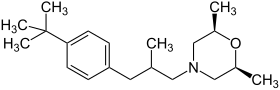 | |||||||||||||||||||
| Strukturformel ohne vollständige Stereochemie | |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Fenpropimorph | ||||||||||||||||||
| Andere Namen |
| ||||||||||||||||||
| Summenformel | C20H33NO | ||||||||||||||||||
| Kurzbeschreibung |
farb- und geruchlose Flüssigkeit[1] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 303,49 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
flüssig[1] | ||||||||||||||||||
| Dichte |
0,931 g·cm−3[1] | ||||||||||||||||||
| Schmelzpunkt | |||||||||||||||||||
| Siedepunkt |
120 °C (bei 0,067 mbar)[1] | ||||||||||||||||||
| Dampfdruck |
bei Raumtemperatur vernachlässigbar[1] | ||||||||||||||||||
| Löslichkeit | |||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Toxikologische Daten | |||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||||||||||||
Gewinnung und Darstellung
Für die Darstellung von Fenpropimorph wurden in der Literatur verschiedene Wege beschrieben:
Es kann durch Reaktion von Diisopropanolamin mit Schwefelsäure und der Reaktion des entstehenden 2,6-Dimethylmorpholin mit Ameisensäure und 3-para-tert-Butylphenyl-2-methylpropanal gewonnen werden.[4]
Fenpropimorph kann auch in ionischen Flüssigkeiten wie 1-Butyl-1-methyl-pyrrolidinium-bis[(trifluormethyl)sulfonyl]amid ([bmpyrr][NTf2]) synthetisiert werden. Dabei wird entweder von 4-tert-Butylbenzyliodid ausgegangen, das mittels Heck-Reaktion in Lilial überführt und anschließend mit 2,6-Dimethylmorpholin reduktiv zum Fenpropimorph aminiert wird. Alternativ kann auch von 4-tert-Butylbenzaldehyd ausgegangen werden, der mittels Aldol-Kondensation, Hydrierung und ebenfalls reduktiver Aminierung ins Produkt überführt werden kann.[5][6]
Eine siebenstufige stereoselektive Synthese des (S)-Enantiomers ist ebenfalls literaturbekannt.[5]
Eigenschaften
Fenpropimorph ist eine brennbare, wenig flüchtige, farb- und geruchlose Flüssigkeit, die praktisch unlöslich in Wasser ist.[1] Es ist stabil gegenüber Photolyse und Hydrolyse bei pH-Werten von 5, 7 und 9.[2]
Verwendung
Fenpropimorph wird als Fungizid verwendet.[1] Es wird als Holzschutzmittel präventiv gegen holzverfärbende und holzzerstörende Pilze eingesetzt. Es hemmt am Zellwandaufbau beteiligte Enzyme und verhindert die Sterol-Biosynthese.[7] Es dient weiterhin der Bekämpfung von Echtem Mehltau bei Weizen, Gerste und Roggen, Gelb- und Braunrost bei Weizen, sowie Rhynchosporium-Blattfleckenkrankheit bei Wintergerste.[8] Die Verbindung wurde 1983 auf den Markt gebracht.[9]
Zulassung
In den Staaten der Europäischen Union war der Wirkstoff Fenpropimorph seit Mai 2009 für Anwendungen als Fungizid bei Pflanzenschutzmitteln zulässig.[10] Inzwischen sind Pflanzenschutzmittel mit diesem Wirkstoff in der EU nicht mehr zugelassen. In der Schweiz dagegen besteht eine Zulassung.[11]
Sicherheitshinweise
Fenpropimorph ist als reproduktionstoxisch eingestuft und kann möglicherweise das Kind im Mutterleib schädigen.[1]
Einzelnachweise
- Eintrag zu Fenpropimorph in der GESTIS-Stoffdatenbank des IFA, abgerufen am 20. Januar 2022. (JavaScript erforderlich)
- FAO: Fenpropimorph (PDF; 426 kB).
- Eintrag zu cis-4-[3-(p-tert-butylphenyl)-2-methylpropyl]-2,6-dimethylmorpholine im Classification and Labelling Inventory der Europäischen Chemikalienagentur (ECHA), abgerufen am 1. August 2016. Hersteller bzw. Inverkehrbringer können die harmonisierte Einstufung und Kennzeichnung erweitern.
- Thomas A. Unger: Pesticide synthesis handbook. 1996, ISBN 978-0-8155-1401-5, S. 476 (eingeschränkte Vorschau in der Google-Buchsuche).
- Clemens Lamberth: Bioactive Heterocyclic Compound Classes. John Wiley & Sons, 2012, ISBN 978-3-527-66443-6, S. 59. (eingeschränkte Vorschau in der Google-Buchsuche).
- Stewart A. Forsyth, H. Q. Nimal Gunaratne u. a.: One-Pot Multistep Synthetic Strategies for the Production of Fenpropimorph Using an Ionic Liquid Solvent. In: Organic Process Research & Development. 10, 2006, S. 94, doi:10.1021/op050172m.
- BAUA: Fenpropimorph (Memento vom 23. Juni 2013 im Internet Archive)
- Müfit Bahadir, Harun Parlar, Michael Spiteller: Springer Umweltlexikon. Springer DE, 2000, ISBN 3-642-56998-6, S. 427 (eingeschränkte Vorschau in der Google-Buchsuche).
- Horst Börner, Klaus Schlüter: Pflanzenkrankheiten Und Pflanzenschutz. Springer DE, 2009, ISBN 3-540-49068-X, S. 496 (eingeschränkte Vorschau in der Google-Buchsuche).
- Richtlinie 2008/107/EG der Kommission vom 25. November 2008 zur Änderung der Richtlinie 91/414/EWG des Rates zwecks Aufnahme der Wirkstoffe Abamectin, Epoxiconazol, Fenpropimorph, Fenpyroximat und Tralkoxydim (PDF)
- Generaldirektion Gesundheit und Lebensmittelsicherheit der Europäischen Kommission: Eintrag zu Fenpropimorph in der EU-Pestiziddatenbank; Eintrag in den nationalen Pflanzenschutzmittelverzeichnissen der Schweiz, Österreichs und Deutschlands, abgerufen am 6. Dezember 2019.


