Elektrochemische Impedanzspektroskopie
Die elektrochemische Impedanzspektroskopie (oft mit EIS abgekürzt) bestimmt die Impedanz, d. h. den Wechselstromwiderstand, elektrochemischer Systeme als Funktion der Frequenz einer Wechselspannung bzw. des Wechselstroms. Elektrochemische Systeme sind z. B. galvanische Zellen oder Elektrolysezellen und enthalten einen Elektronenleiter (Elektrode), und einen Ionenleiter (Elektrolyt). Mit der Impedanzspektroskopie können wertvolle Informationen über das untersuchte System und die in ihm ablaufenden Vorgänge erhalten werden, z. B. auch über den Widerstand eines Elektrolyten.
Anwendungsgebiete
In fast allen Bereichen der Elektrochemie kann die Impedanzspektroskopie zur Untersuchung und Beurteilung von Material- oder Systemeigenschaften verwendet werden. Anwendungsgebiete können daher sein:
- Energiespeicher:
- Batterien, z. B. Bestimmung des Innenwiderstands. Weitere Ziele sind die Bestimmung des Ladezustandes oder des Alterungszustandes der Batterie.
- Brennstoffzellen
- Doppelschicht-Kondensatoren, z. B. Bestimmung der Kapazität
- Biologische und biomedizinische Systeme
- Elektrochemie von Halbleitern, z. B. in photoelektrochemische Zellen wie der Grätzel-Zelle. Hier muss man mit einem bedeutenden Beitrag des Elektronenleiters zur Gesamtimpedanz rechnen.
- Untersuchungen zur Korrosion, zum Korrosionsschutz und zur Passivierung
- Oberflächentechnik
- Kinetik
- Zur Untersuchung des Sedimentationsverhaltens von Partikeln in Flüssigkeiten[1]
- Feststellung der Zusammensetzung von Stoffgemischen (z. B. Milch)[2]
- Ermittlung von Eigenschaften von Stoffgemischen (z. B. Materialfeuchte, Aushärtungsgrad von Klebstoffen oder Baumaterialien)[2]
Messmethoden
Meist erfolgt die Impedanzspektroskopie, indem eine Wechselspannung aufgeprägt wird, d. h., das Potential der Arbeitselektrode wird sinusförmig moduliert und der Strom und seine Phase werden gemessen. Dabei gibt es mehrere Möglichkeiten für das mittlere Potential: Entweder wird beim Ruhepotential, d. h. beim Gleichgewichtspotential bei geöffnetem Stromkreis, gearbeitet, oder bei einem festgelegten mittleren Potential, das durch einen Potentiostaten auf einem abgesehen von der Spannungsmodulation konstanten Wert („potentiostatische Impedanzspektroskopie“) gehalten wird. Beim „potentiodynamischen Verfahren“ wird die Impedanz während eines zyklischen Voltammogramms aufgenommen.[3] Alternativ dazu kann die Impedanzspektroskopie auch mit Hilfe eines aufgeprägten Wechselstromes durchgeführt werden; dann wird das Potential und seine Phase gemessen.
Der Begriff der Impedanz und die komplexe Wechselstromrechnung gehen davon aus, dass zwischen den Amplituden von Spannung und Strom ein linearer Zusammenhang besteht. Das ist in elektrochemischen Systemen nur näherungsweise für kleine Amplituden, z. B. 1 bis 10 mV, der Fall.[4] Deutlich größere Amplituden dürfen daher nicht zur Messung verwendet werden.
Darstellung, Auswertung und Interpretation der Messergebnisse
Die Grundlagen der Darstellung, Auswertung und Interpretation der Messergebnisse sind dieselben wie bei anderen impedanzspektroskopischen Verfahren und werden hier beschrieben.
Als Beispiel soll eine wässrige Lösung aus Eisen(III)- und Eisen(II)-Ionen untersucht werden. In diese Lösung taucht eine Arbeits- und Gegenelektrode. Legt man an die Elektroden eine Wechselspannung an, so laufen mehrere Vorgänge ab, die mit einer Ersatzschaltung beschrieben werden können:
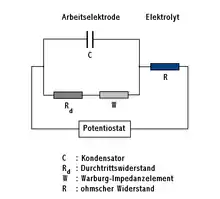
- In einer Doppelschicht an den Elektroden reichern sich die Ionen an bzw. ab. Diese Schicht wird durch einen Plattenkondensator mit der Kapazität C beschrieben.
- Die Wechselspannung verursacht an den Elektroden reversible Redoxreaktionen. Eisen(III)-Ionen werden durch Elektronenaufnahme zu Eisen(II)-Ionen reduziert und Eisen(II)-Ionen durch Elektronenabgabe oxidiert. Die Elektronenaufnahme bzw. Elektronenabgabe an den Elektroden erfordert eine Aktivierungsenergie und wird durch einen Durchtrittswiderstand Rd beschrieben.
- Aus der Lösung werden Ionen an die Elektroden transportiert bzw. von den Elektroden wegtransportiert. Hierbei spielt der Widerstand der Lösung eine Rolle, der durch einen ohmschen Widerstand R beschrieben wird. Dieser ist unabhängig vom Zustand der Elektrode.
- Aufgrund der Wechselspannung ändern sich an den Elektroden die Konzentrationen der Ionen, die reduziert bzw. oxidiert werden. Liegt die positive Sinushalbwelle an der Arbeitselektrode, so erfolgt die Oxidation. Elektronen werden von der Elektrode aufgenommen. Liegt die negative Halbwelle an, so erfolgt die Reduktion. Elektronen werden von der Elektrode abgegeben. Die Konzentrationsschwankungen der Eisen(III)- und Eisen(II)-Ionen bedingen eine gedämpfte Welle, die sich teilweise in der Lösung ausbreitet. Diese resultierende Impedanz kann mit dem Modell der Warburg-Impedanz beschrieben werden.
Die vier Impedanzelemente gelten für die Arbeitselektrode, aber zugleich auch für die Gegenelektrode, da dort die gleichen Vorgänge ablaufen.
Im nächsten Schritt der Auswertung wird für jedes Impedanzelement das frequenzabhängige Verhalten aus angenommenen Ausgangswerten berechnet und mit den gemessenen Daten verglichen. Bei guter Übereinstimmung wird ein physikalisch-chemisches Modell entwickelt, das das elektrochemische System detailliert unter Einbeziehung von Druck und Temperatur beschreibt. Man kann zum Vergleich auch eine Gleichspannung anlegen, um noch weitere Informationen zu erhalten.
Theorie
Harmonische Wechselströme, wie sie in der Impedanzspektroskopie verwendet werden, lassen sich durch eine Sinusfunktion beschreiben:
Hierbei ist die Spannung, die Amplitude der Spannung, der Strom, die Amplitude des Stroms, der Phasenwinkel der Spannung, der Phasenwinkel des Stroms und die Kreisfrequenz, die sich als Funktion der Frequenz schreiben lässt: . Die Phasenverschiebung kann durch die Differenz der beiden Phasenwinkel bestimmt werden: . In der Wechselstromlehre ist es sinnvoll, die mathematischen Zusammenhänge im komplexen Zahlenraum zu beschreiben.
Dabei ist die komplexe Spannung und der komplexe Strom. Wechselstromwiderstände werden Impedanz genannt. Das Ohmsche Gesetz gilt analog zur Gleichstromlehre: . Mit den komplexen Ausdrücken für die Spannung und den Strom ergibt sich:
Dabei ist der Scheinwiderstand , der den Betrag der komplexen Impedanz ausdrückt. Nach der Eulerschen Formel kann die Impedanz auch als differenzierter Real- und Imaginärteil dargestellt werden:
Hierbei ist der Realteil und der Imaginärteil des komplexen Wechselstromwiderstandes. Die reziproke Impedanz beschreibt den komplexen Leitwert, auch Admittanz genannt.[5] Im Nyquist-Diagramm werden die beiden Teile der Impedanz gegeneinander aufgetragen.
Weblinks
- Electrochemical Impedance Spectroscopy Theory: A Primer. Gamry Instruments, 28. Dezember 2007, archiviert vom Original am 1. Februar 2009; abgerufen am 22. August 2011.
- Apparative Methoden in der Physikalischen Chemie - Impedanzspektroskopie (PDF-Datei; 244 kB)
Einzelnachweise
- Nikolaus Doppelhammer, Nick Pellens, Christine E.A. Kirschhock, Bernhard Jakoby, Erwin K. Reichel: Using Moving Electrode Impedance Spectroscopy to Monitor Particle Sedimentation. In: IEEE Sensors Journal. 2020, ISSN 1530-437X, S. 1–1, doi:10.1109/JSEN.2020.3004510 (ieee.org [abgerufen am 14. Juli 2020]).
- Ilmsens GmbH: FAQ. Abgerufen am 15. Oktober 2021 (amerikanisches Englisch).
- Genady Ragoisha: Potentiodynamic Electrochemical Impedance Spectroscopy. In: ABC Chemistry. 2004, abgerufen am 15. August 2015.
- Basics of EIS: Electrochemical Research-Impedance. Linearity of Electrochemistry Systems. In: gamry.com > Resources > Application Notes > Electrochemical Impedance Spectroscopy. Gamry Instruments, 17. April 2018, abgerufen am 17. September 2019 (englisch).
- K. Funke: Apparative Methoden in der Physikalischen Chemie: Impedanzspektroskopie. 2002, abgerufen am 28. Februar 2020.