Dioxetane
Dioxetane sind heterocyclische organische chemische Verbindungen, die aus einem Vierring bestehen, der neben zwei Kohlenstoff- auch zwei Sauerstoffatome besitzt. Das 1,2-Dioxetan ist damit ein organisches Peroxid, wohingegen 1,3-Dioxetan ein cyclisches Acetal ist.
 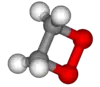 |
| 1,2-Dioxetan |
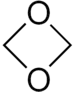 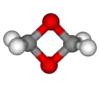 |
| 1,3-Dioxetan |
Geschichte und biologische Bedeutung
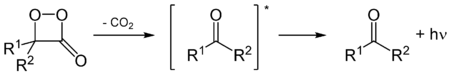
Einige natürlich vorkommende 1,2-Dioxetane bzw. deren α-Keto-Derivate (Dioxetanone, α-Peroxylactone) sind die Ursache der Biolumineszenz. In den 1960er Jahren kamen Biochemiker zum Schluss, dass diese Verbindungen in Leuchtkäfern (auch Glühwürmchen, Lampyridae, englisch fireflies) und anderen Lebewesen, die Biolumineszenz zeigten, aufgrund ihrer Instabilität ein „fließendes“ Vorkommen besäßen. Dann wurde 1968 das erste Beispiel eines stabilen Dioxetans an der University of Alberta in Edmonton gefunden. Dieses 3,3,4-Trimethyl-1,2-dioxetan löst sich mit gelber Farbe in Benzol. Nach Erhitzen der Lösung auf 333 Kelvin (60 °C) zersetzte sich die Substanz langsam und nicht – wie erwartet – explosionsartig zu Aceton und Acetaldehyd unter Aussendung von bleich-blauem Licht.[1]
Das zweite Beispiel eines Dioxetans, das symmetrische 3,3,4,4-Tetramethyl-1,2-dioxetan, wurde kurz darauf dargestellt. Die gelben Kristalle der Substanz sublimierten sogar bei der Aufbewahrung im Kühlschrank. Die Lösung in Benzol emittierte ebenfalls unter Zersetzung langsam blaues Licht. Durch geeignete Substitution mit unter UV-Licht fluoreszierenden Verbindungen konnte die Farbe des ausgesandten Lichts verändert werden. Da das 3,3,4,4-Tetramethyl-1,2-dioxetan zum Studienobjekt vieler Wissenschaftler zur Aufklärung der Mechanismen der Biolumineszenz wurde, war diese bald eine der weltweit am besten untersuchten symmetrischen Verbindungen.[2]
Darstellung
Die Biosynthese von Dioxetanen und Dioxetanonen erfolgt aus einem Luciferin, das meist ein Derivat eines stickstoffhaltigen Polycyclus ist, der Imidazol als Strukturelement enthält. Die Organismen setzen dieses Luciferin mit molekularem Sauerstoff, unter Anwesenheit von Ca2+-Ionen über spezielle, artspezifische Luciferasen zum lichtemittierenden Endstoff um.[3] Im Labormaßstab lassen sich Dioxetane aus cis-2-Butenderivaten wie 2,3-Dimethyl-2-buten durch Umsetzung mit Sauerstoff oder mit Wasserstoffperoxid und Brom und darauffolgender Cyclisierung des entstandenen Hydroperoxids mit einer Base darstellen.
Verwendung
Lumineszierende Schmuckgegenstände wie Armreife, Halsbänder und Ringe enthalten künstliche Derivate der Dioxetane, die zusätzlich eine Carbonylgruppe enthalten; diese Dioxetanone – wie 1,2-Dioxetandion – zersetzen sich unter Abspaltung von Kohlenstoffdioxid und Lichtemission. Andere Dioxetane werden in der klinischen Analytik zum Nachweis von niedrigsten Konzentrationen von Körperflüssigkeiten (wie Blut) eingesetzt.[4] Dioxetane können in entsprechend aufgebauten Nachweissystemen zusammen mit Luciferasen auch zum hochspezifischen und für minimale Mengen geeigneten qualitativen und quantitativen Nachweis von ATP (Nachweisgrenze 10−11 Mol), NADH und Sauerstoff eingesetzt werden.[5]
Siehe auch
Einzelnachweise
- Karl R. Kopecky, Cedric Mumford: Luminescence in the thermal decomposition of 3,3,4-trimethyl-1,2-dioxetane. In: Canadian Journal of Chemistry. 47 (4), 1969, S. 709, doi:10.1139/v69-114.
- Karl R. Kopecky, John E. Filby, Cedric Mumford, Peter A. Lockwood, Jan-Yih Ding: Preparation and Thermolysis of some 1,2-dioxetanes. In: Canadian Journal of Chemistry. 53 (8), 1975, S. 1103, doi:10.1139/v75-154.
- T. Lindel: Heterocyclenchemie (Memento des Originals vom 5. März 2016 im Internet Archive) Info: Der Archivlink wurde automatisch eingesetzt und noch nicht geprüft. Bitte prüfe Original- und Archivlink gemäß Anleitung und entferne dann diesen Hinweis. (PDF; 4,8 MB), TU Braunschweig
- US-Patent No. 5,330,900 to Tropix Inc.
- Wissenschaft-Online-Lexika: Eintrag zu Luciferasen im Lexikon der Chemie, abgerufen 2. April 2008.