Diiodmethan
Diiodmethan (CH2I2), in der Literatur ist häufiger die Bezeichnung Methyleniodid bzw. die veraltete Version Methylenjodid anzutreffen, ist ein zweifach iodiertes Derivat des Methans und somit ein halogenierter Kohlenwasserstoff. In der Natur ist diese Verbindung bspw. in Seewasser in Konzentrationen von einigen pmol/mol zu finden.[6]
| Strukturformel | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
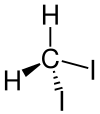 | ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | Diiodmethan | |||||||||||||||
| Andere Namen |
Methyleniodid | |||||||||||||||
| Summenformel | CH2I2 | |||||||||||||||
| Kurzbeschreibung |
hellbraune Flüssigkeit mit charakteristischem Geruch[1] | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 267,84 g·mol−1 | |||||||||||||||
| Aggregatzustand |
flüssig | |||||||||||||||
| Dichte |
3,325 g·cm−3[2] | |||||||||||||||
| Schmelzpunkt | ||||||||||||||||
| Siedepunkt | ||||||||||||||||
| Löslichkeit |
schlecht in Wasser (0,8 g·l−1 bei 25 °C)[1] | |||||||||||||||
| Brechungsindex |
1,7425 (20 °C)[2] | |||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Toxikologische Daten | ||||||||||||||||
| Thermodynamische Eigenschaften | ||||||||||||||||
| ΔHf0 |
68,5 ± 0,8 kJ·mol−1[5] | |||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Brechungsindex: Na-D-Linie, 20 °C | ||||||||||||||||
Gewinnung und Darstellung
Diiodmethan kann ähnlich wie Dibrommethan durch Reaktion von Iodoform mit Natriumarsenit und Natriumhydroxid gewonnen werden.[7]
Es kann auch durch Halogenaustausch mit Aluminiumiodid aus Dichlormethan hergestellt werden.
Eigenschaften
In frischem Zustand ist Diiodmethan eine farblose Flüssigkeit, die sich im Laufe der Zeit durch Zersetzungsreaktionen am Tageslicht bräunlich verfärben kann. Sowohl die Dichte als auch der Brechungsindex von Diiodmethan sind mit 3,325 g·cm−3[2] bzw. 1,7425 (20 °C und 589,3 nm)[2] außergewöhnlich hoch. Die Oberflächenspannung beträgt 0,0508 N·m−1.[8]
Verwendung
In der organischen Synthese kann CH2I2 zur Darstellung von Carbenen verwendet werden, zum Beispiel in der Simmons-Smith-Reaktion.[9] Außerdem findet es als Iodquelle bei sandmeyerartigen Reaktionen Verwendung, zum Beispiel wenn in Systemen gearbeitet wird, in denen anorganische Iodide nicht löslich sind.[10]
In der Mineralogie wird die Schwerflüssigkeit mithilfe der Immersionsmethode häufig zur Bestimmung des Brechungsindex von Mineralien, sowie zur Abtrennung und Dichtebestimmung unbekannter Schwermineralien verwendet. Wegen seiner unbestimmten Toxizität sollte Diiodmethan hierfür nicht mehr verwendet werden, zumal es in vielen Fällen sehr einfach durch ungefährlichere Schwerflüssigkeiten ersetzt werden kann.
Bei der Kontaktwinkelmessung wird Diiodmethan als Referenzflüssigkeit zur Bestimmung der Oberflächenenergie von Festkörpern verwendet, da es für eine rein bzw. vorwiegend unpolare Flüssigkeit eine relativ hohe Oberflächenspannung aufweist und daher gut messbare Kontaktwinkel ausbildet.
Einzelnachweise
- Eintrag zu Methyleniodid in der GESTIS-Stoffdatenbank des IFA, abgerufen am 8. Januar 2018. (JavaScript erforderlich)
- CRC Handbook of Tables for Organic Compound Identification, Third Edition, 1984, ISBN 0-8493-0303-6.
- Datenblatt Diiodmethan (PDF) bei Merck, abgerufen am 5. Juli 2007.
- Datenblatt Diiodomethane bei Sigma-Aldrich, abgerufen am 25. März 2011 (PDF).
- A. S. Carson, P. G. Laye, J. B. Pedley, Alison M. Welsby: The enthalpies of formation of iodomethane, diiodomethane, triiodomethane, and tetraiodomethane by rotating combustion calorimetry. In: The Journal of Chemical Thermodynamics, 1993, 25 (2), S. 261–269; doi:10.1006/jcht.1993.1025.
- Vogt, Rainer et al.: Iodine chemistry and its role in halogen activation and ozone loss in the marine boundary layer: A model study. In: Journal of Atmospheric Chemistry 32.3 (1999): 375-395.
- Roger Adams and C. S. Marvel: Methylene Iodide In: Organic Syntheses. 1, 1921, S. 57, doi:10.15227/orgsyn.001.0057; Coll. Vol. 1, 1941, S. 358 (PDF).
- Krüss: Liquids, abgerufen am 8. Oktober 2009.
- H. E. Simmons, T. L. Cairns, S. A. Vladuchick, C. M. Hoiness: Review of its use in the cyclopropanation of olefins. In: Org. React., 1973, 20, S. 1–131.
- V. Nair, S. Richardson: Modification of Nucleic Acid Bases via Radical Intermediates: Synthesis of Dihalogenated Purine Nucleosides. In: Synthesis, 1982, S. 670–672; doi:10.1055/s-1982-29896.
