cis-Abienol
cis-Abienol ist eine chemische Verbindung und gehört zu der Gruppe der Labdane, wobei das Labdan-Grundgerüst durch Doppelbindungen an den Stellen C-12 und C-14 und durch eine Hydroxygruppe an der Stelle C-8 modifiziert ist. Es handelt sich folglich um ein Diterpen-Alkohol (Terpenoid).[4] Das Isomer trans-Abienol, welches eine (E)-Stereochemie an C-12 aufweist, ist nur von geringer Bedeutung.
| Strukturformel | |||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
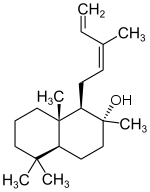 | |||||||||||||
| Allgemeines | |||||||||||||
| Name | Cis-Abienol | ||||||||||||
| Andere Namen |
| ||||||||||||
| Summenformel | C20H34O | ||||||||||||
| Kurzbeschreibung |
weißer bis blassgelblicher, wachsartiger Feststoff[1] | ||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||
| |||||||||||||
| Eigenschaften | |||||||||||||
| Molare Masse | 290,49 g·mol−1 | ||||||||||||
| Aggregatzustand |
fest[1] | ||||||||||||
| Schmelzpunkt | |||||||||||||
| Löslichkeit |
wenig in Chloroform und Ethylacetat[1] | ||||||||||||
| Sicherheitshinweise | |||||||||||||
| |||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||||||
Vorkommen und Gewinnung

Abienol ist ein Naturstoff und kommt in verschiedensten Pflanzen vor, unter anderem als Hauptbestandteil des Aromastoffes Oleoresin in der Balsam-Tanne (Abies balsamea),[5] in der Banks-Kiefer (Pinus banksiana),[6] in der Schwarz-Fichte (Picea mariana)[6] oder im Virginischen Tabak (Nicotiana tabacum), aus welchem er auch durch Extraktion gewonnen werden kann.[7] Er kommt hauptsächlich auf der Blattoberfläche vor.[8]
Verwendung
Abienol dient im Tabak als Inhibitor der Verwelkungskrankheit (englisch Wilt disease).[9] Des Weiteren ist er eine Ausgangsverbindung für die Produktion von Duft- und Aromastoffen.[10] Aus diesem Grund wird Abienol häufig in der Parfümindustrie als Ausgangsprodukt verwendet. Im Labor findet es maßgeblich Anwendung in der Synthese von Diolen.[1] Der Geruch wird als hölzern, bernsteinartig und balsamisch beschrieben.[6]
Einzelnachweise
- Eintrag zu (+)-cis-Abienol bei Toronto Research Chemicals, abgerufen am 8. April 2018 (PDF).
- Datenblatt (+)-cis-Abienol, SC-479393, bei Santa Cruz Biotechnology Inc., abgerufen am 9. April 2018 (PDF).
- Dieser Stoff wurde in Bezug auf seine Gefährlichkeit entweder noch nicht eingestuft oder eine verlässliche und zitierfähige Quelle hierzu wurde noch nicht gefunden.
- Eintrag zu cis-Abienol in Chemical Entities of Biological Interest (ChEBI), abgerufen am 9. April 2018.
- P. Zerbe et al.: Bifunctional cis-abienol synthase from Abies balsamea discovered by transcriptome sequencing and its implications for diterpenoid fragrance production. In: The Journal of Biological Chemistry. Band 287, 2012, S. 12121–12131, doi:10.1074/jbc.M111.317669.
- Eintrag zu cis-Abienol. The Goodscent Company, abgerufen am 9. April 2018.
- Eintrag zu Abienol in der MeSH der NIH US National Library of Medicine, abgerufen am 9. April 2018.
- V. Vontimitta et al.: Analysis of a Nicotiana tabacum L. genomic region controlling two leaf surface chemistry traits. In: Journal of Agricultural and Food Chemistry. Band 58, 2010, S. 294–300, doi:10.1021/jf903256h.
- S. Seo et al.: Identification of natural diterpenes that inhibit bacterial wilt disease in tobacco, tomato and Arabidopsis. In: Plant & Cell Physiology. Band 53, 2012, S. 1432–1444, doi:10.1093/pcp/pcs085.
- T. Hieda et al.: Microbial transformation of cis-abienol. In: Agricultural and Biological Chemistry. Band 46, 1982, S. 2249–2255, doi:10.1080/00021369.1982.10865428.