Cinacalcet
Cinacalcet (Handelsname in der EU Mimpara®; Hersteller Amgen) ist ein Arzneistoff zur Behandlung des primären und sekundären Hyperparathyreoidismus – einer Erkrankung der Nebenschilddrüse.
| Strukturformel | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
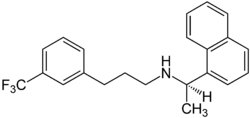 | ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Freiname | Cinacalcet | |||||||||||||||
| Andere Namen |
(R)-N-[1-(1-Naphthyl)ethyl]-3-[3-(trifluormethyl)phenyl]propan-1-amin | |||||||||||||||
| Summenformel |
| |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Arzneistoffangaben | ||||||||||||||||
| ATC-Code |
H05BX01 | |||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | ||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||
Wirkmechanismus
Cinacalcet ist ein allosterischer Modulator des calciumsensitiven Rezeptors und führt zu einer Konformationsänderung seiner Tertiärstruktur. Dies bewirkt eine Erhöhung der Empfindlichkeit des Rezeptors für Calcium und zu einer verminderten Freisetzung des Knochenstoffwechselhormons Parathormon. Die Wirkung von Cinacalcet auf den calciumsensitiven Rezeptor der Nebenschilddrüse ist dabei etwa 100-mal stärker als die Wirkung auf calciumsensitive Rezeptoren anderer Gewebe, z. B. der C-Zellen der Schilddrüse. Dies erklärt möglicherweise, warum bereits geringe Dosen von Cinacalcet die Produktion von Parathormon in der Nebenschilddrüse hemmen, ohne gravierende Nebenwirkungen in anderen Organen und Geweben hervorzurufen, die ebenfalls calciumsensitive Rezeptoren exprimieren.
Stereoisomerie
Cinacalcet enthält ein stereogenes Zentrum. Als Arzneistoff wird das reine (R)-Enantiomer eingesetzt.[2] Die fluorhaltige, chirale organische chemische Verbindung kommt aus der Gruppe der Naphthalin-Derivate.
Zulassung
Cinacalcet ist EU-weit seit 2004 unter dem Handelsnamen Mimpara® auf dem Markt, der Hersteller ist Amgen. In den USA lautet der Handelsname Sensipar®.
Die Zulassung erstreckt sich auf die Behandlung
- des sekundären Hyperparathyreoidismus bei Patienten mit dialysepflichtigem Nierenversagen in Verbindung mit Phosphatbindern und Vitamin D, seit September 2017 auch bei Kindern ab drei Jahren zugelassen,[3]
- der Hyperkalzämie beim Nebenschilddrüsenkarzinom sowie
- der Hyperkalzämie bei primärem Hyperparathyreoidismus, bei der eine operative Entfernung der Nebenschilddrüsen angezeigt wäre, im konkreten Fall aber nicht möglich ist.
Tierexperimentelle Daten
Bei Tieren mit chronischer Niereninsuffizienz führt Cinacalcet
- zu einem Abfall der Synthese und Freisetzung von Parathormon in der Nebenschilddrüse,
- zu einer Hochregulierung des Calcium sensitiven Rezeptors und des Vitamin-D-Rezeptors,
- zu einer verminderten Proliferation der Nebenschilddrüsen-Zellen,
- zu einem verminderten Fortschreiten einer Nebenschilddrüsen-Vergrößerung (Hyperplasie),
- zu einer vermehrten programmierten Zelltod (Apoptose) von Nebenschilddrüsen-Zellen,
- zu einem verminderten Fortschreiten der durch erhöhte Parathormonspiegel hervorgerufenen Knochenveränderungen (Osteitis fibrosa) sowie
- zu einem verminderten Fortschreiten von Kalkablagerungen in den Arterien.
Studien am Menschen
Bei Patienten mit primärem Hyperparathyreoidismus oder bei chronischen Hämodialysepatienten führt die Einnahme von Cinacalcet innerhalb von 2–4 Stunden zu einem raschen Abfall des Parathormons. Bei Dialysepatienten, nicht aber bei Patienten mit primärem Hyperparathyreoidismus, kommt es innerhalb von 4–8 Stunden zu einem Abfall des Serum-Calciums.
Die Langzeit-Anwendung von Cinacalcet führt bei primärem Hyperparathyreoidismus zu einem langsamen Abfall der zuvor erhöhten Calcium-Spiegel und zu einem Anstieg der Phosphat-Spiegel, die Parathormon-Spiegel ändern sich nur geringfügig.
Bei Dialysepatienten führt die Langzeit-Anwendung von Cinacalcet zu einem zunehmenden Absinken von Parathormon, Calcium- und Phosphat-Spiegeln. Der sekundäre Hyperparathyreoidismus kann so über Jahre unter Kontrolle gehalten werden.
Bei Patienten mit chronischer Niereninsuffizienz im Stadium 3 und 4 senkt Cinacalcet erhöhte Parathormonspiegel. Das Serum-Calcium wird gesenkt, das Serum-Phosphat steigt an. Im Urin steigt die Calcium-Ausscheidung, die Phosphat-Ausscheidung sinkt.[4]
Nach Nierentransplantation führt ein fortbestehender Hyperparathyreoidismus zu Hyperkalzämie und Hypophosphatämie aufgrund einer gesteigerten Ausscheidung von Phosphat über die Nieren. Cinacalcet führt in dieser Situation zu einer Normalisierung von Phosphat-Ausscheidung und Serum-Phosphat.[5]
Derzeit abgeschlossene Untersuchungen beim Menschen beschränken sich jedoch auf die Wirkung von Cinacalcet auf sogenannte Surrogatparameter, wie Parathormon, Calcium und Phosphat.
Studien, die die Auswirkungen einer Therapie mit Cinacalcet auf klinisch relevante Endpunkte untersuchen, werden derzeit erst durchgeführt. Eine Studie untersucht bei Dialysepatienten den Effekt von Cinacalcet auf die Verkalkung der Aortenklappe. Eine zweite Studie untersucht die Auswirkungen einer Behandlung von Dialysepatienten mit Cinacalcet auf Mortalität und kardiovaskuläre Endpunkte wie Herzinfarkt, Schlaganfall u. ä.[6] Bislang ist nicht geklärt, ob der Einsatz von Cinacalcet bei Patienten mit chronischer Nierenkrankheit, die noch keine Dialysebehandlung benötigen, sinnvoll ist.
Nebenwirkungen
Häufigste Nebenwirkungen von Cinacalcet sind Übelkeit und Erbrechen. Eine langsame Steigerung der Dosis kann dazu beitragen, die Nebenwirkungen zu reduzieren.
Eine Studie über die Sicherheit bei der Anwendung bei pädiatrischen Patienten ist im Februar 2013 nach dem Tod eines 14-jährigen Patienten vorsichtshalber abgebrochen worden, auch wenn nicht klar war, ob das Medikament zum Tod geführt hat. Mögliche Nebenwirkungen könnten eine Hypokalzämie mit darauf folgenden Krampfanfällen bis hin zum Stimmritzenkrampf oder Herzrhythmusstörungen durch Verlängerung der QT-Zeit sein,[7] weswegen die Kontrolle hinsichtlich des Auftretens einer Hypokalzämie besonders wichtig ist.[8] Unabhängig davon erfolgte im September 2017 eine EU-Zulassung auch bei Kindern ab drei Jahren für den sekundären Hyperparathyreoidismus.[3]
Einzelnachweise
- Für diesen Stoff liegt noch keine harmonisierte Einstufung vor. Wiedergegeben ist eine von einer Selbsteinstufung durch Inverkehrbringer abgeleitete Kennzeichnung von N-[(1R)-1-(naphthalen-1-yl)ethyl]-3-[3-(trifluoromethyl)phenyl]propan-1-amine hydrochloride (1:1) im Classification and Labelling Inventory der Europäischen Chemikalienagentur (ECHA), abgerufen am 28. Dezember 2019.
- ROTE LISTE® 2008, Verlag Rote Liste® Service GmbH, Frankfurt am Main, Seite 52, ISBN 978-3-939192-20-6.
- European Commission Approves Expanded Use Of Mimpara® (Cinacalcet) For The Treatment Of Secondary Hyperparathyroidism In Children With End-Stage Renal Disease On Dialysis, PM Amgen vom 31. August 2017, abgerufen am 6. September 2017.
- M. Chonchol, F. Locatelli, H. E. Abboud, C. Charytan, A. L. de Francisco, S. Jolly, M. Kaplan, S. D. Roger, S. Sarkar, M. B. Albizem, T. C. Mix, Y. Kubo, G. A. Block: A randomized, double-blind, placebo-controlled study to assess the efficacy and safety of cinacalcet HCl in participants with CKD not receiving dialysis. In: American journal of kidney diseases. Band 53, Nummer 2, Februar 2009, S. 197–207, doi:10.1053/j.ajkd.2008.09.021, PMID 19110359.
- Andreas L Serra, Claudia Wuhrmann, Rudolf P Wüthrich: Phosphatemic effect of cinacalcet in kidney transplant recipients with persistent hyperparathyroidism. In: American Journal of Kidney Diseases. 52, Nr. 6, Dezember 2008, S. 1151–1157. doi:10.1053/j.ajkd.2008.08.012. PMID 18950915.
- Tilman B Drüeke, Eberhard Ritz: Treatment of secondary hyperparathyroidism in CKD patients with cinacalcet and/or vitamin D derivatives. In: Clinical Journal of the American Society of Nephrology. 4, Nr. 1, Januar 2009, S. 234–241. doi:10.2215/CJN.04520908. PMID 19056615.
- FDA Drug Safety Communication: FDA suspends pediatric clinical trials of Sensipar (cinacalcet hydrochloride) after report of death
- Rote Hand Brief von Amgen im März 2013 zu Mimpara Janssen. (PDF; 333 kB) Abgerufen am 24. Februar 2016.