Chlorameisensäureester
Die Chlorameisensäureester (auch Chlorformiate oder genauer Chlorkohlensäureester) stellen eine Stoffgruppe organisch-chemischer Verbindungen dar. Formal gesehen sind sie die Ester der instabilen Chlorkohlensäure, die umgangssprachlich fast immer Chlorameisensäure genannt wird. Bei den Chlorameisensäureester handelt es sich also so gesehen auch um das Monochlorid und zugleich den Monoalkylester der Kohlensäure.[1]
| Chlorameisensäureester |
|---|
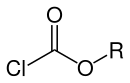 |
| Allgemeine Struktur der Chlorameisensäureester. Der Rest R stellt dabei einen aliphatischen, cyclischen oder aromatischen Rest dar. |
Geschichte
Chlorameisensäureester wurden erstmals 1833 von Jean-Baptiste Dumas beschrieben und erlangten ab 1950 als Zwischenprodukte in der organischen Synthese steigende Bedeutung.[2]
Herstellung
Am günstigsten werden Chlorameisensäureester durch Umsetzung von Phosgen, dem Dichlorid der Kohlensäure, mit wasserfreien Alkoholen unter Abspaltung von Chlorwasserstoff hergestellt:
In der Regel wird in technischen Prozessen für die Umsetzung von aliphatischen Alkoholen kein Katalysator und keine Base zum Abfangen des gebildeten Chlorwasserstoffs benötigt. Die Umsetzung von Phenolen mit Phosgen benötigen dagegen höhere Temperaturen (>100 °C) und säurebindende Mittel oder spezielle Katalysatoren (z. B. Dimethylpropylenharnstoff).[3]
Reaktionen
Chlorameisensäureester sind sehr reaktive chemische Verbindungen und reagieren mit der Reaktivität von Carbonsäurechloriden mit allen Nukleophilen.
- Chlorameisensäureester reagieren mit Wasser zu Chlorwasserstoff, Kohlendioxid und dem entsprechenden Alkohol:
- Chlorameisensäureester reagieren mit Alkoholen zu Carbonaten (Kohlensäurediester) und mit Thiolen (Mercaptanen) zu Thiocarbonaten:
- Chlorameisensäureester reagieren mit primären oder sekundären Aminen zu Carbamaten:
Einzelnachweise
- Eintrag zu Chlorformiate. In: Römpp Online. Georg Thieme Verlag, abgerufen am 12. Dezember 2021..
- Siegfried Böhm, Maren Beth-Hübner: Chloroformic Esters. In: Ullmann’s Encyclopedia of Industrial Chemistry. Wiley‐VCH Verlag GmbH & Co. KGaA., 15. April 2006, doi:10.1002/14356007.a06_559.pub2.
- Livius Cotarca, Heiner Eckert: Phosgenations – A Handbook. Wiley-VHC, Weinheim 2004, ISBN 3-527-29823-1, S. 47 (eingeschränkte Vorschau in der Google-Buchsuche).