CCR5
CCR5 oder C-C-Motiv-Chemokin-Rezeptor 5 ist – neben CD195 und weiteren Synonymen[1] – die Bezeichnung für ein Rezeptorprotein aus der Familie der Chemokinrezeptoren, das vom Gen CCR5 codiert wird, welches beim Menschen auf Chromosom 3 (Genlocus 3p21.31) liegt, und in Zellen des Immunsystems wie T-Zellen und Makrophagen exprimiert wird.[2]
| C-C-Chemokinrezeptor Typ5 | ||
|---|---|---|
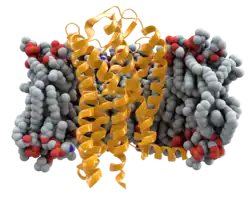 | ||
|
Vorhandene Strukturdaten: 1ND8, 1NE0, 1OPN, 1OPT, 1OPW, 2L87, 2MZX, 2RLL, 2RRS, 4MBS | ||
| Eigenschaften des menschlichen Proteins | ||
| Masse/Länge Primärstruktur | 352 Aminosäuren | |
| Sekundär- bis Quartärstruktur | Transmembranprotein | |
| Bezeichner | ||
| Gen-Namen | CCR5 ; CC-CKR-5; CCCKR5; CCR-5; CD195; CKR-5; CKR5; CMKBR5; IDDM22 | |
| Externe IDs | ||
| Orthologe | ||
| Mensch | Hausmaus | |
| Entrez | 1234 | 12774 |
| Ensembl | ENSG00000160791 | ENSMUSG00000079227 |
| UniProt | P51681 | P51682 |
| Refseq (mRNA) | NM_000579 | NM_009917 |
| Refseq (Protein) | NP_000570 | NP_034047 |
| Genlocus | Chr 3: 46.37 – 46.38 Mb | Chr 9: 124.12 – 124.15 Mb |
| PubMed-Suche | 1234 | 12774 |
Eine besondere Bedeutung hat CCR5 dadurch, dass ein HI-Virus 1 diesen als Corezeptor gebraucht (nach Bindung an CD4), um sich an eine Zelle so anzuheften, dass sie infiziert werden kann.
Rezeptor
Der Chemokinrezeptor CCR5 ist als Transmembranprotein auf der Oberfläche verschiedener Leukozyten zu finden, beispielsweise bei Makrophagen, CD4+-Zellen, CD8+-Zellen und NKT-Zellen. CCR5 wird durch unterschiedliche Liganden wie CCL3 (MIP-1α), CCL4 (MIP-1β), CCL5 (RANTES) und CCL8 (MCP-2) aktiviert,[3] ermöglicht eine chemotaktische Zellbewegung und ist damit in Entzündungsreaktionen involviert.
Pathologische Bedeutung
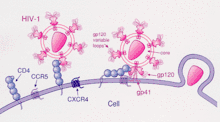
Der Rezeptor CCR5 stellt einen Co-Rezeptor für die HIV-Infektion dar und macht das Andocken von HI-Viren an Makrophagen wie auch verschiedene T-Lymphozyten möglich, das Eindringen in die Zellen und somit deren Infektion. Daher ist die Entwicklung von Arzneistoffen, welche die Anbindung von HIV an CCR5 hemmen, von großem Interesse und führte beispielsweise zum ersten zugelassenen Entry-Inhibitor Maraviroc.
Darüber hinaus wird CCR5 eine Beteiligung an Autoimmunerkrankungen wie multipler Sklerose, rheumatoider Arthritis und Diabetes mellitus vom Typ I zugeschrieben.
Genmutation
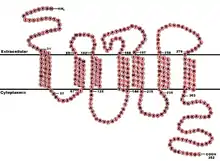
Eine Mutation des Gens CCR5 mit der Bezeichnung CCR5Δ32 (CCR5-Delta32), bei der ein 32-Basenpaar-Segment deletiert ist, führt zu einem Frameshift mit einem vorzeitigen Stopcodon. Das daraus resultierende verkürzte Protein – dem die drei C-terminalen Transmembrandomänen fehlen – bleibt im Zytoplasma und erscheint nicht an der Zelloberfläche.
Bei einem homozygoten Träger der Genmutation hat dies eine Resistenz gegenüber den meisten HIV-Stämmen zur Folge. Ein solcher homozygoter Genotyp wäre im Hardy-Weinberg-Gleichgewicht bei etwa 1 % der heutigen Europäer zu erwarten, da die Allelfrequenz rund 10 % beträgt. Als Grund des häufigen Auftretens dieser Mutation wurde zunächst ein Selektionsdruck durch Seuchen in Nordeuropa vor etwa 700 Jahren angenommen. Jedoch legen neuere Untersuchungen ein wesentlich höheres Alter für das Auftreten der Mutation und ihre Verbreitung durch Selektionseffekte nahe. Eine Aussage über den Selektionsfaktor wird damit nahezu unmöglich.[4][5][6][7]
Die einzige bis jetzt dokumentierte Heilung einer HIV-Infektion gelang durch die Knochenmarktransplantation von einem homozygoten CCR5Δ32-Spender bei einem HIV-Infizierten. Der später als "The Berlin Patient" bekannt gewordene HIV-positive Mann benötigte aufgrund einer AML eine Knochenmarktransplantation.[8] Nach der Transplantation des homozygoten CCR5Δ32-Knochenmarkes ließ sich nach einiger Latenz kein Virus mehr im Körper des Patienten nachweisen und er war seither nicht mehr auf eine HAART angewiesen.[9]
Darüber hinaus wird in einer im Januar 2006 im Journal of Experimental Medicine veröffentlichten Studie die Vermutung aufgestellt, dass die Anfälligkeit für das West-Nil-Virus durch dieselbe Mutation massiv begünstigt wird. Die Vermutung wurde zwei Jahre später durch eine Metaanalyse der Daten des Westnil-Ausbruchs in den USA erhärtet.[10][11]
Genmanipulation
Der chinesische Wissenschaftler He Jiankui hat nach eigenen Angaben den CCR5-Rezeptor bei mehreren menschlichen Embryonen deaktiviert, um so die dann geborenen Kinder immun gegen HIV zu machen[12].
Einzelnachweise
- so auch CKR-5, CC-CKR-5, CMKBR5, IDDM22; siehe Eintrag in HGNC.
- siehe Eintrag CCR5 auf NCBI.
- Murphy PM, Baggiolini M, Charo IF, et al.: International union of pharmacology. XXII. Nomenclature for chemokine receptors. In: Pharmacological Reviews. 52, Nr. 1, März 2000, S. 145–76. PMID 10699158.
- Galvani AP, Slatkin M: Evaluating plague and smallpox as historical selective pressures for the CCR5-Delta 32 HIV-resistance allele. In: Proc. Natl. Acad. Sci. USA. 100, Nr. 25, Dezember 2003, S. 15276–9. doi:10.1073/pnas.2435085100. PMID 14645720. PMC 299980 (freier Volltext).
- Biloglav Z, Zgaga L, Smoljanović M, et al.: Historic, demographic, and genetic evidence for increased population frequencies of CCR5Delta32 mutation in Croatian Island isolates after lethal 15th century epidemics. In: Croat. Med. J.. 50, Nr. 1, Februar 2009, S. 34–42. PMID 19260142. PMC 2657566 (freier Volltext).
- Zawicki P, Witas HW: HIV-1 protecting CCR5-Delta32 allele in medieval Poland. In: Infect. Genet. Evol.. 8, Nr. 2, März 2008, S. 146–51. doi:10.1016/j.meegid.2007.11.003. PMID 18162443.
- Faure E, Royer-Carenzi M: Is the European spatial distribution of the HIV-1-resistant CCR5-Delta32 allele formed by a breakdown of the pathocenosis due to the historical Roman expansion?. In: Infect. Genet. Evol.. 8, Nr. 6, Dezember 2008, S. 864–74. doi:10.1016/j.meegid.2008.08.007. PMID 18790087.
- Kerstin Decker: AIDS-Heilung: Anatomie eines Wunders. Der Tagesspiegel, 6. Juni 2011, abgerufen am 8. März 2014.
- Hartmut Wewetzer: Rätselraten um den „Berliner Patienten“. Der Tagesspiegel, 13. Juni 2012, abgerufen am 8. März 2014.
- W. G. Glass, D. H. McDermott u. a.: CCR5 deficiency increases risk of symptomatic West Nile virus infection. In: The Journal of experimental medicine Band 203, Nummer 1, Januar 2006, S. 35–40. doi:10.1084/jem.20051970. PMID 16418398. PMC 211808 (freier Volltext).
- J. K. Lim, C. Y. Louie u. a.: Genetic deficiency of chemokine receptor CCR5 is a strong risk factor for symptomatic West Nile virus infection: a meta-analysis of 4 cohorts in the US epidemic. In: The Journal of Infectious Diseases Band 197, Nummer 2, Januar 2008, S. 262–265. doi:10.1086/524691. PMID 18179388.
- https://www.zeit.de/wissen/gesundheit/2018-11/emmanuelle-charpentier-crispr-babys-china-genschere-entsetzt Crispr-Entdeckerin kritisiert Genversuche an Babys, Zeit online