Biocytin
Biocytin oder Nε-(+)-Biotinyl-L-lysin ist eine chemische Verbindung, die zu den Carbonsäureamiden gehört. Mit dem Trivialnamen Biocytin wird ausschließlich die Verbindung aus dem Vitamin Biotin [(+)-Stereoisomer] und dem L-Enantiomer der Aminosäure Lysin bezeichnet. Dabei ist die Carboxygruppe des Biotins mit der ε-Aminogruppe des Lysins kondensiert. Als Zwischenprodukt des Biotinstoffwechsels tritt Biocytin im Blutserum und im Urin auf.
| Strukturformel | |||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
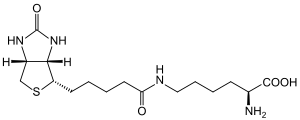 | |||||||||||||
| Allgemeines | |||||||||||||
| Name | Biocytin | ||||||||||||
| Andere Namen |
| ||||||||||||
| Summenformel | C16H28N4O4S | ||||||||||||
| Kurzbeschreibung |
beigefarbenes Pulver[1] | ||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||
| |||||||||||||
| Eigenschaften | |||||||||||||
| Molare Masse | 372,48 g·mol−1 | ||||||||||||
| Aggregatzustand |
fest | ||||||||||||
| Schmelzpunkt | |||||||||||||
| Sicherheitshinweise | |||||||||||||
| |||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||||||
Seit den späten 1980er Jahren wird Biocytin als so genannter neuronaler Tracer als Bestandteil von histologischen Färbemethoden für Nervenzellen genutzt.
Vorkommen und biologische Bedeutung
Biocytin ist der Biotin tragende Komplex in den folgenden Carboxylasen, die grundlegende Aufgaben im Kohlenhydrat-, Protein- und Fettstoffwechsel erfüllen:[2]
- Pyruvat-Carboxylase
- Methylcrotonoyl-CoA-Carboxylase
- Propionyl-CoA-Carboxylase
- Acetyl-CoA-Carboxylase
Beim Abbau dieser Carboxylasen durch Proteolyse bleibt Biocytin übrig. Die Spaltung des Biocytins in freies Biotin und Lysin wird von dem Enzym Biotinidase katalysiert. Da Tiere das Vitamin Biotin nicht selbst herstellen können, sind sie darauf angewiesen, Biotin mit der Nahrung aufzunehmen und schon im Körper vorhandenes Biotin viele Male zu recyceln. Deshalb stellt Biocytin eine wichtige Biotinquelle für den Organismus dar.
Welche Bedeutung Biocytin in dieser Hinsicht für den Menschen besitzt, wird durch die seltene Erbkrankheit Biotinidasemangel deutlich. Die Betroffenen können aufgrund eines Defekts der Biotinidase Biocytin nur unzureichend verwerten und entwickeln in der Folge Symptome eines Biotinmangels, was bis zum Tod führen kann.[3]
Eigenschaften
Biocytin in handelsüblicher Form ist ein beiges Pulver, das bei 245 °C schmilzt.[1] Wie Biotin wird auch Biocytin nichtkovalent von Avidin gebunden.
Das Enzym Biotinidase hydrolysiert die Amidbindung des Biocytins unter Bildung von Biotin und Lysin.
Verwendung
Biotinidase-Test
Da Biocytin das natürliche Substrat des Enzyms Biotinidase ist, kann es zur Messung der Biotinidase-Aktivität eingesetzt werden. Die Menge der pro Zeiteinheit entstehenden Reaktionsprodukte Biotin oder Lysin ist dabei ein Maß für die Aktivität des Enzyms.[4] Zur Bestimmung der Biotinidase-Aktivität in menschlichen Blutproben, insbesondere für die Diagnose der Stoffwechselstörung Biotinidasemangel, ist Biocytin jedoch nur bedingt geeignet. Die Medikation mit Biotin kann den Enzymdefekt verschleiern.[5]
Neuronaler Tracer
Beladung mit Biocytin ist eine von vielen Möglichkeiten, Neuronen einschließlich ihrer weit verästelten Ausläufer sichtbar zu machen.[6] Es besteht dabei die Möglichkeit, Biocytin ins lebende Gewebe zu applizieren, wo es sich innerhalb von Stunden über die Nervenzellen verteilt. Per Mikroinjektion können auch einzelne Neuronen mit Biocytin gefüllt werden. Nach diesem Schritt sind die Neuronen zwar markiert, aber noch nicht angefärbt, da Biocytin selbst kein Farbstoff ist. Die Färbung des anhaftenden Biocytins findet nach Wasch- und Fixierprozedur am Schnittpräparat statt. Dabei macht man sich zunutze, dass das Protein Avidin an Biotin und Biotin-Verbindungen wie Biocytin sehr stark bindet. Man kann beispielsweise einen Fluoreszenz-Farbstoff biotinylieren und dann an Avidin andocken lassen. Da Avidin mehrere Bindungsstellen für Biotinstrukturen besitzt, kann der Avidin-Fluorophor-Komplex nun seinerseits an das die Nervenzelle markierende Biocytin andocken – die Zelle fluoresziert. Eine weitere Möglichkeit besteht darin, einen Avidin-Peroxidase-Komplex an das Biocytin andocken zu lassen. Dieser ist allerdings auch noch nicht farbig. Eine Färbevariante besteht in einer Reaktion der Peroxidase mit Diaminobenzidin (DAB), Wasserstoffperoxid und zweiwertigen Nickel- und/oder Cobalt-Ionen.
Wie die beiden Beispiele zeigen, kann bei Verwendung von Biocytin zur Markierung von Neuronen die eigentliche Färbemethode sehr flexibel gehandhabt werden. So ist es möglich, für Lichtmikroskopie, Fluoreszenzmikroskopie und Elektronenmikroskopie geeignete Präparate herzustellen.[7]
Sicherheitshinweise
Laut Angaben eines Inverkehrbringers liegen zur Toxizität von Biocytin derzeit keine Daten vor, der Stoff ist aber noch nicht vollständig geprüft. Bezüglich der CLP-Verordnung ist dieser Stoff nicht als gefährlich eingestuft. Bei Arbeiten mit der reinen Substanz werden allgemein übliche Vorsichtsmaßnahmen empfohlen. Durch Selbsteinstufung des Herstellers befindet sich Biocytin in Wassergefährdungsklasse (WGK) 3.[1]
Einzelnachweise
- Datenblatt Biocytin bei Sigma-Aldrich, abgerufen am 22. Mai 2017 (PDF).
- J. M. Berg, J. L. Tymoczko, L. Stryer: Biochemie. 6. Auflage. Spektrum Akademischer Verlag, Elsevier GmbH, München 2007; S. 515–516, 551, 697–698, 711–713, 746, ISBN 978-3-8274-1800-5.
- E. R. Baumgartner, T. Suormala: Multiple carboxylase deficiency: inherited and acquired disorders of biotin metabolism. In: Int. J. Vitam. Nutr. Res. 67(5); 1997: S. 377–784; PMID 9350481.
- M. Koivusalo, C. Elorriaga, Y. Kaziro, S. Ochoa: Bacterial biotinidase. In: J. Biol. Chem. 238; March 1963: S. 1038–1042; PMID 14034272.
- K. Kumasaka, M. Muratsugu, T. Fukui, M. Kimura, Y. Takagi, N. Hashizume: A new quantitative analytical method of serum biotinidase activity using biocytin as a substrate and its clinical significance in Japan. In: Clin. Chim. Acta 306(1–2); April 2001: S. 71–77; PMID 11282096; doi:10.1016/S0009-8981(01)00395-3
- C. Köbbert, R. Apps, I. Bechmann, J. L. Lanciego, J. Mey, S. Thanos: Current concepts in neuroanatomical tracing. In: Prog. Neurobiol. 62(4); Nov 2000: S. 327–351, PMID 10856608;doi:10.1016/S0301-0082(00)00019-8
- A. J. McDonald: Neuroanatomical labeling with biocytin: a review. In: Neuroreport 3(10); Oct 1992: S. 821–827; PMID 1384763.