Arndt-Eistert-Homologisierung
Die Arndt-Eistert-Homologisierung oder auch Arndt-Eistert-Synthese ist eine Reaktion aus dem Bereich der Organischen Chemie. Dabei wird eine Carbonsäure in drei Stufen um eine Methylengruppe (–CH2–) verlängert (homologisiert). Die dritte Stufe bezeichnet man auch als Wolff-Umlagerung.
Die Reaktion ist nach ihren Entdeckern, den Chemikern Fritz Arndt (1885–1969) und Bernd Eistert (1902–1978), benannt.
Übersicht
In der ersten Stufe wird die Carbonsäure in das korrespondierende Säurechlorid umgewandelt. Danach erfolgt die Addition der Methylengruppe, welche durch das Diazomethan bereitgestellt wird. Es entsteht ein α-Diazo-methylketon. Die dritte Stufe, die Wolff-Umlagerung, führt mit z. B. Silberoxid als Katalysator und Wasser zur Bildung der homologen Carbonsäure. Durch den Austausch von Wasser durch andere Verbindungen können jedoch auch andere Derivate entstehen (siehe unten).

Praktisch wird die Reaktion mit einem zusätzlichen Äquivalent Diazomethan durchgeführt, da das sich abspaltende HCl-Molekül an das Diazoketon addieren und ein α-Halogen-Keton ergeben kann (Nierensteinreaktion). Das zusätzliche Äquivalent Diazomethan überführt HCl in Chlormethan, welches nicht mehr reaktiv genug ist.
Mechanismus
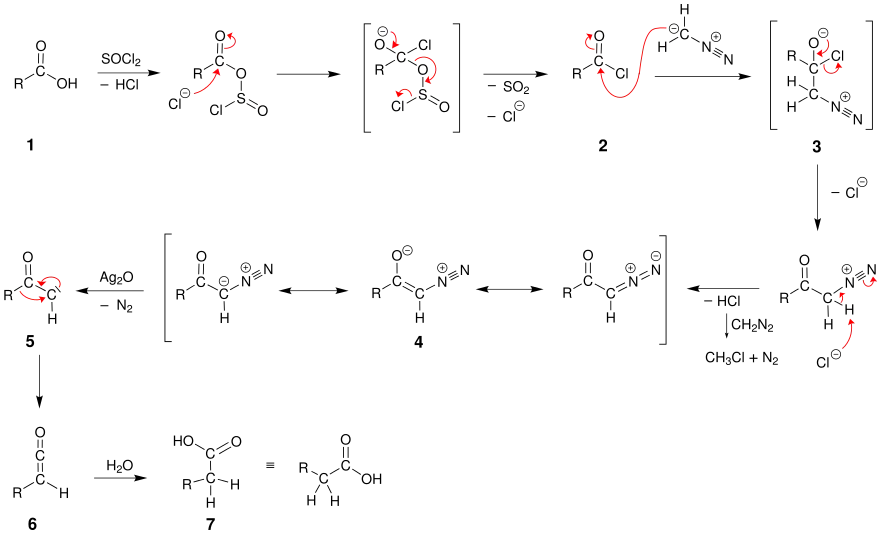
Aus der Carbonsäure 1 wird zunächst das Säurechlorid 2 gebildet. Danach erfolgt an dessen terminalem Kohlenstoffatom die nukleophile Addition der Methylengruppe des Diazomethans. Hierbei entsteht in einem Übergangszustand ein Diazoniumbetain 3, das unter Abspaltung von HCl in das mesomeriestabilisierte Diazoketon 4 übergeht (Addition-Eliminierungs-Mechanismus).
Diazoketone können bei erhöhter Temperatur mit Silber- und Kupfer-Katalysatoren unter Mitnahme der Bindungselektronen molekularen Stickstoff abspalten. Das Zwischenprodukt ist ein klassisches Carben 5. Im nächsten Schritt findet eine Wolff-Umlagerung statt, so dass sich das Keten 6 bildet. Dieses reagiert mit Wasser in einer nukleophilen Addition zur Carbonsäure 7.
Das Keten 6 kann auch mit anderen H-aciden, nucleophilen Verbindungen in einer nucleophilen Addition umgesetzt werden:[2]
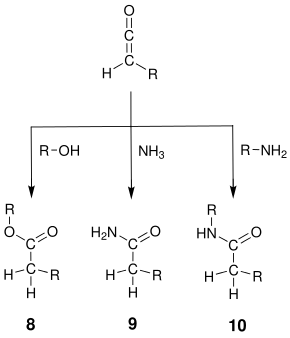
Verwendet man anstatt Wasser einen Alkohol, so erhält man den entsprechenden Ester 8. Durch Addition von Ammoniak oder Aminen können Amide 9 bzw. 10 gewonnen werden.
Siehe auch
Einzelnachweise
- L. Kürti, B. Czakó: Stratigic Applications of Named Reactions in Organic Synthesis. Elsevier Academic Press, Amsterdam 2005, ISBN 978-0-12-429785-2, S. 18.
- T. Laue, A. Plagens: Namen- und Schlagwort-Reaktionen. 5. Auflage. B. G. Teubner Verlag / GWV Fachverlage, Wiesbaden 2006, ISBN 978-3-8351-0091-6, S. 17.
Literatur
- Hans Beyer, Wolfgang Walter: Lehrbuch der Organischen Chemie. 23. überarb. und aktualisierte Auflage. S. Hirzel, Stuttgart/Leipzig 1998, ISBN 3-7776-0808-4.