4-Hydroxycumarine
4-Hydroxycumarine (Vitamin-K-Antagonisten, verkürzt auch Cumarine oder Cumarinderivate) werden in der Medizin vom 4-Hydroxycumarin abgeleitete Substanzen mit blutgerinnungshemmender Wirkung genannt.[1] Ihre Wirkung beruht auf einer Hemmung des für die Bildung von Blutgerinnungsfaktoren wichtigen Vitamin-K-Stoffwechsels. In der Medizin werden Cumarine als blutgerinnungshemmende Arzneistoffe eingesetzt (Antikoagulanzien). Darüber hinaus werden Cumarine auch als Rodentizide insbesondere zur Rattenbekämpfung genutzt.
Geschichte

Die wissenschaftliche Entwicklung der Cumarine begann mit der Entdeckung des Dicoumarol in Steinklee-haltigem Heu durch Karl Paul Link und Mitarbeiter im Jahr 1940.[2] Die Bildung von Dicoumarol in Heu und Silage aus den enthaltenen cumarinhaltigen Weidepflanzen kann bei einer fehlerhaften Herstellung oder Lagerung unter Pilzbefall erfolgen.[3] Die Verfütterung dicoumarolhaltiger Futtermittel kann bei Weidevieh infolge der Blutgerinnungshemmung zu inneren Verblutungen führen (Sweet Clover Disease). Basierend auf dieser Erkenntnis wurde diese neue Substanz 1941 erstmals klinisch als Antikoagulans erprobt.
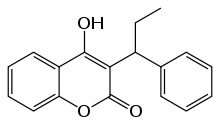
In den 1940er Jahren wurden Derivate des Dicoumarols insbesondere von der Arbeitsgruppe von Karl P. Link entwickelt. Während Link diese Substanzen für zu toxisch und daher nicht für vermarktbar hielt, glaubte sein Mitarbeiter Mark A. Stahmann an eine Nutzung und meldete mit Hilfe der Wisconsin Alumni Research Foundation (WARF) die nach ihr benannte Substanz Warfarin zum Patent an.[4] 1948 erfolgte die Markteinführung von Warfarin zunächst als Rodentizid. Nachdem 1951 ein Mitglied der US Navy erfolglos versucht hatte, sich mit Warfarin das Leben zu nehmen, und dank der Gabe von Vitamin K als Antidot gerettet werden konnte, wurde auch das therapeutische Potenzial des jetzt als sicher erachteten Warfarins untersucht.[5] 1954 wurde Warfarin zur medizinischen Verwendung zugelassen. Kurz zuvor wurden bereits die Cumarine Tromexan und Phenprocoumon als Antikoagulantien eingeführt. Bekanntheit erlangten die Antikoagulantien vom Dicoumarol-Typ im Jahr 1955, als der damalige Präsident der Vereinigten Staaten Dwight D. Eisenhower nach einem Herzinfarkt mit ihnen behandelt wurde.[4]
Chemie
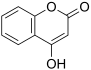
Die in der Medizin und in der Schädlingsbekämpfung verwendeten Cumarine leiten sich strukturell vom 4-Position-hydroxylierten Cumarin ab.
 |
_200.svg.png.webp) |
-2H-chromen-2-one_200.svg.png.webp) |
-2H-chromen-2-one_200.svg.png.webp) | |
| Cumarin | 4-Hydroxycumarin | Dicoumarol | Phenprocoumon (Antikoagulanz) | Warfarin (Antikoagulanz) |
 |
 |
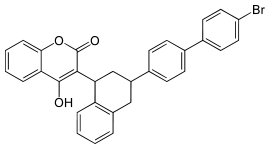 |
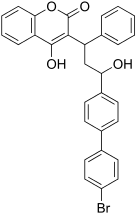 |
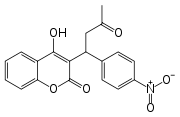
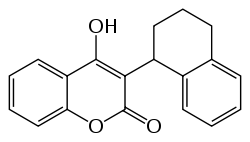
| Acenocoumarol (Antikoagulanz) | Coumatetralyl (Rodentizid) | Brodifacoum (Rodentizid) | Bromadiolon (Rodentizid) |
Wirkung
Bei der Anwendung als Medikament und als Rodentizid wird folgende Wirkung der Cumarine ausgenutzt:
Die Faktoren der plasmatischen Blutgerinnung müssen in der Leber modifiziert werden: Dabei wird die Aminosäure Glutamat am γ-C-Atom carboxyliert, damit die Faktoren mittels Calcium-Ionen an die Thrombozytenoberfläche binden und somit ihre maximale Wirkung entfalten können. Die Reaktion wird von der γ-Glutamylcarboxylase katalysiert und benötigt Vitamin K in seiner biologische aktiven Form – dem Vitamin-K-Hydrochinon – als Kosubstrat.
Das Vitamin-K-Hydrochinon geht als Vitamin-K-Epoxid aus der Reaktion hervor. Um für weitere Carboxylierungen zur Verfügung zu stehen, wird das Vitamin-K-Epoxid durch das Enzym Vitamin-K-Oxidoreduktase über das Zwischenprodukt Vitamin-K-Chinon zum Vitamin-K-Hydrochinon reduziert. Cumarine besitzen eine Strukturähnlichkeit zu Vitamin K und inhibieren beide Teilreaktionen kompetitiv. Cumarinderivate vermindern die Bildung der Gerinnungsfaktoren also dadurch, dass sie die Regeneration des Vitamin K in seine biologisch aktive Form hemmen. Die Wirkung tritt erst ein, nachdem die Gerinnungsfaktoren, die zum Zeitpunkt der Gabe des Cumarinderivats im Blut zirkulierten, teilweise verbraucht sind. Dies ist erst nach etwa sechs Stunden der Fall. Das Wirkmaximum wird nach 36–48 Stunden erreicht.
Therapieüberwachung
Die Wirkung wird bisher noch häufig anhand des Quick-Wertes kontrolliert. Da die Quick-Werte verschiedener Laboratorien/Reagentien voneinander abweichen, wird zur besseren Vergleichbarkeit vermehrt die INR (englisch international normalized ratio) angegeben. Zur Vermeidung von schwerwiegenden Nebenwirkungen ist neben der zuverlässigen Einnahme der Medikamente die regelmäßige Kontrolle dieses Wertes erforderlich. Dies kann bei chronisch Kranken mit Hilfe von tragbaren Testgeräten auch zu Hause im Rahmen des Gerinnungsselbstmanagements geschehen, was eine erhöhte Lebensqualität der Betroffenen bedeuten kann (dichtere Kontrollen, größere Mobilität).
Patienten, denen Phenprocoumon verabreicht wird, erhalten einen „Pass“ zum Mitführen, damit im Notfall die eingeschränkte Gerinnungssituation erkennbar ist, selbst wenn der Patient nicht ansprechbar sein sollte. In einem solchen Pass muss nach jeder Blutkontrolle der aktuelle Quick-Wert oder INR-Wert eingetragen werden; auch die aktuelle verordnete Dosierung sollte stets auf dem aktuellen Stand sein. Ebenso ist in diesem Pass ein Ziel-Quick oder Ziel-INR vermerkt, auf den der Patient eingestellt ist.
Indikation
Die Therapie mit Cumarinen ist bei Patienten notwendig, bei denen ein hohes Risiko für das Eintreten einer Thrombose besteht. Dies kann beispielsweise der Fall sein:
- nach Implantation künstlicher Herzklappen,
- nach einer bereits aufgetretenen Thrombose zur Rezidivprophylaxe,
- bei Vorhofflimmern,
- bei Herzerkrankungen mit erweiterter Herzkammer und schlechter Pumpfunktion,
- nach Implantation künstlicher Gefäßprothesen,
- nach einem Herzinfarkt.
Nebenwirkungen und Anwendungsbeschränkungen
Die Nebenwirkungen der Cumarine ergeben sich aus ihrer Hauptwirkung. Da unter Cumarin-Therapie die Blutgerinnung vermindert wird, treten vermehrt Blutungen auf. Dies kann sich beispielsweise äußern in:
- vermehrter Neigung zu blauen Flecken,
- vermehrtem Zahnfleischbluten,
- Blutungen im Magen-Darm-Trakt,
- Blutungen durch die Haut,
- Blut im Urin,
- Schlaganfällen durch Hirnblutung.
Bei Bestehen einer Schwangerschaft ist die Anwendung von Cumarinen wegen der fruchtschädigenden Wirkung kontraindiziert.
Rückenmarksnahe Regionalanästhesie-Verfahren (Spinalanästhesie bzw. Periduralanästhesie) sollten erst durchgeführt werden, wenn der INR als Maß für die Blutgerinnungszeit nach Absetzen der Cumaringabe unter 1,4 abgesunken ist.[6][7]
Wechselwirkungen
Cumarine zeigen eine starke Plasmaproteinbindung. Werden nun Substanzen eingenommen, die ihrerseits eine höhere Plasmaproteinbindungskapazität als Cumarine haben, so kommt es zu einer plötzlichen Freisetzung der gebundenen Cumarine mit deutlichem Wirkungsanstieg. Dies konnte früher insbesondere bei gleichzeitiger Gabe von Sulfonylharnstoffen der ersten Generation (z. B. Tolbutamid) und Warfarin oder Phenprocoumon beobachtet werden. Neuere Sulfonylharnstoffe zeigen diese Interaktion nicht mehr.
Cumarine werden überwiegend in der Leber über Cytochrom P450 3A4 und Cytochrom P450 2C9 abgebaut. Hemmstoffe dieser Enzymsysteme führen zu einem verlangsamten Abbau von Cumarinen und zu einer Anreicherung nach wiederholter Einnahme, verbunden mit einer erhöhten Blutungsgefahr. Dieses Risiko besteht nicht nur bei der gleichzeitigen Einnahme von Cumarinen mit CYP-3A4- oder CYP-2C9-hemmenden Arzneistoffen, sondern auch mit einigen Lebensmitteln. So warnte das Bundesinstitut für Arzneimittel und Medizinprodukte (BfArM) Patienten, die Cumarine einnehmen, vor möglichen Blutungskomplikationen wegen erhöhter Cumarinplasmaspiegeln aufgrund einer CYP-C29-Hemmung nach dem Konsum von Chinesischen Wolfsbeeren (Gemeiner Bocksdorn).[8]
Auch die Kombination mit Thrombozytenaggregationshemmern wie Acetylsalicylsäure verstärken die Blutungsgefahr. Des Weiteren steigt das Blutungsrisiko auch bei gleichzeitiger Anwendung von Cephalosporine, aber auch SNRI und SSRI. Beide zuletzt genannten auch über die Hemmwirkung auf die Thrombozytenaggregation durch Verarmung der Blutplättchen an Serotonin.[9]
Präparate
Bekannte Cumarine sind:
- Phenprocoumon (Produktnamen Marcumar, Falithrom)
- Warfarin (Produktnamen Coumadin, Marevan)
- Acenocumarol (Produktnamen Sintrom)
Antidot
Bei Vergiftungen mit Cumarinen muss unverzüglich hoch dosiertes Vitamin K als Antidot gegeben werden, um die fehlende Vitamin-K-Regeneration zu kompensieren. Auch hier besteht eine Verzögerung in der Wirkung, da die fehlenden Gerinnungsfaktoren erst nach und nach durch die Leber ersetzt werden können. Insbesondere bei Vergiftungen durch Brodifacoum, Difenacoum, Bromadiolon, Difethialon oder Flocoumafen (Rodentizide) ist eine Langzeittherapie mit Vitamin K erforderlich. Im Notfall können die fehlenden Gerinnungsfaktoren direkt ersetzt werden.
Einzelnachweise
- Pschyrembel: Klinisches Wörterbuch, Band 258. de Gruyter, 1998, ISBN 3-11-014824-2, S. 312.
- MA Stahmann, CF Hübner, KP Link: Studies on the hemorrhagic sweet clover disease; identification and synthesis of the hemorrhagic agent. In: J. Biol. Chem.. 138, Nr. 2, 1941, S. 513–527.
- A. Bye, H.K. King: The biosynthesis of 4-hydroxycoumarin and dicoumarol by Aspergillus fumigatus Fresenius. In: Biochemical Journal. 117, 1970, S. 237–245.
- Nicole Kresge, Robert D. Simoni, Robert L. Hill: Hemorrhagic Sweet Clover Disease, Dicumarol, and Warfarin: the Work of Karl Paul Link. In: J. Biol. Chem.. 280, 2005, S. e5.
- KP Link: The Discovery of Dicumarol and Its Sequels. In: Circulation. 19, 1959, S. 97–107. doi:10.1161/01.CIR.19.1.97.
- Wiebke Gogarten, Hugo Van Aken: Perioperative Thromboseprophylaxe - Thrombozytenaggregationshemmer - Bedeutung für die Anästhesie In: AINS – Anästhesiologie · Intensivmedizin · Notfallmedizin · Schmerztherapie, 47, 2012, S. 242–252; doi:10.1055/s-0032-1310414.
- S. A. Kozek-Langenecker, D. Fries, M. Gütl, N. Hofmann, P. Innerhofer, W. Kneifl, L. Neuner, P. Perger,T. Pernerstorfer, G. Pfanner, et al.: Lokoregionalanästhesien unter gerinnungshemmender Medikation. Empfehlungen der Arbeitsgruppe Perioperative Gerinnung (AGPG) der Österreichischen Gesellschaft für Anästhesiologie und Intensivmedizin (ÖGARI). In: Der Anästhesist, Volume 54, Number 5, 2005, S. 476–484, doi:10.1007/s00101-005-0827-0
- I Flügge: Mögliche Interaktion zwischen Vitamin-K-Antagonisten und der Goji-Beere – Risiko von INR-Erhöhung und schweren Blutungsereignissen Archiviert vom Original am 5. Dezember 2013. (PDF) In: Bulletin zur Arzneimittelsicherheit. Nr. 1, 2013. Abgerufen am 6. April 2013.
- P. Schweikert-Wehner: DOAK Update Interaktionen. In: Pharmazeutische Zeitung. Band 162, Nr. 38, 20. September 2017, S. 92.