1,3-Dioxolan
1,3-Dioxolan ist eine chemische Verbindung aus der Gruppe der Sauerstoffheterocyclen und ist isomer zu 1,2-Dioxolan. Man kann die Verbindung auch als cyclisches Acetal betrachten.
| Strukturformel | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
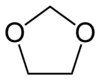 | ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | 1,3-Dioxolan | |||||||||||||||
| Andere Namen |
| |||||||||||||||
| Summenformel | C3H6O2 | |||||||||||||||
| Kurzbeschreibung |
leicht flüchtige, farblose Flüssigkeit[1] | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 74,08 g·mol−1 | |||||||||||||||
| Aggregatzustand |
flüssig[1] | |||||||||||||||
| Dichte |
1,06 g·cm−3[1] | |||||||||||||||
| Schmelzpunkt | ||||||||||||||||
| Siedepunkt |
74 °C[1] | |||||||||||||||
| Dampfdruck | ||||||||||||||||
| Löslichkeit |
mischbar mit Wasser[2][1], löslich in Ethanol, Diethylether, Aceton[2] | |||||||||||||||
| Brechungsindex |
1,401 (20 °C)[3] | |||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| MAK |
Schweiz: 20 ml·m−3 bzw. 62 mg·m−3[5] | |||||||||||||||
| Toxikologische Daten | ||||||||||||||||
| Thermodynamische Eigenschaften | ||||||||||||||||
| ΔHf0 |
−333,5 kJ/mol[6] | |||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Brechungsindex: Na-D-Linie, 20 °C | ||||||||||||||||
Gewinnung und Darstellung
1,3-Dioxolan kann durch Reaktion von Ethylenglycol mit Formaldehyd unter Säurekatalyse gewonnen werden:[7]
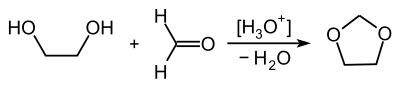
Alternativ kann auch Ethylenoxid mit Formaldehyd in Gegenwart von Zinntetrachlorid oder Tetraethylammoniumbromid als Katalysator umgesetzt werden.[8]
Eigenschaften
Physikalische Eigenschaften
1,3-Dioxolan ist eine leicht flüchtige, farblose Flüssigkeit, die bei Normaldruck bei 74 °C siedet.[1] Die Dampfdruckfunktion ergibt sich nach Antoine entsprechend log10(P) = A−(B/(T+C)) (P in bar, T in K) mit A = 4,11859, B = 1237,377 und C = −48.73 im Temperaturbereich von 281 K bis 355 K.[9] Bei −97 °C wird der Schmelzpunkt mit einer Schmelzwärme von 6,57 kJ·mol−1 beobachtet.[10][11] In fester Phase treten zwei polymorphe Kristallformen auf. Die Kristallform II wandelt sich bei −131 °C mit einer Umwandlungswärme von 2,68 kJ·mol−1 in die Kristallform I um.[11] Die Verbindung ist die mit Wasser, Diethylether, Aceton und Tetrahydrofuran in jedem Verhältnis mischbar.[2][8]
Chemische Eigenschaften
Die Verbindung neigt zur Bildung von Peroxiden.[2] In Gegenwart von Säuren erfolgt eine Hydrolyse zu Ethylenglycol und Formaldehyd. Im basischen Medium ist die Verbindung stabiler. Beim Erhitzen auf 470 °C bis 500 °C erfolgt eine Pyrolyse zu Ameisensäure und Ethylen.[8]
Sicherheitstechnische Kenngrößen
1,3-Dioxolan bildet leicht entzündliche Dampf-Luft-Gemische. Die Verbindung hat einen Flammpunkt von −5 °C.[1][12] Der Explosionsbereich liegt zwischen 2,3 Vol.‑% (70 g/m³) als untere Explosionsgrenze (UEG) und 30,5 Vol.‑% (935 g/m³) als obere Explosionsgrenze (OEG).[1][12] Die Sauerstoffgrenzkonzentration liegt bei 6,9 %.[13] Die Zündtemperatur beträgt 245 °C.[12][1] Der Stoff fällt somit in die Temperaturklasse T3.
Verwendung
1,3-Dioxolan wird als Comonomer zur Herstellung von modifizierten Polyoxymethylenen verwendet.[2] Es dient als Substitut für Dichlormethan in Abbeizmitteln.
Sicherheitshinweise/Toxikologie
1,3-Dioxolan wurde 2016 von der EU gemäß der Verordnung (EG) Nr. 1907/2006 (REACH) im Rahmen der Stoffbewertung in den fortlaufenden Aktionsplan der Gemeinschaft (CoRAP) aufgenommen. Hierbei werden die Auswirkungen des Stoffs auf die menschliche Gesundheit bzw. die Umwelt neu bewertet und ggf. Folgemaßnahmen eingeleitet. Ursächlich für die Aufnahme von 1,3-Dioxolan waren die Besorgnisse bezüglich Verbraucherverwendung, Exposition empfindlicher Bevölkerungsgruppen, hoher (aggregierter) Tonnage und weit verbreiteter Verwendung sowie der möglichen Gefahren durch mutagene und reproduktionstoxische Eigenschaften. Die Neubewertung läuft seit 2016 und wird von Deutschland durchgeführt.[14]
Einzelnachweise
- Eintrag zu 1,3-Dioxolan in der GESTIS-Stoffdatenbank des IFA, abgerufen am 20. Januar 2022. (JavaScript erforderlich)
- Eintrag zu 1,3-Dioxolan. In: Römpp Online. Georg Thieme Verlag, abgerufen am 1. Juni 2021.
- Datenblatt 1,3-Dioxolane, anhydrous, contains ~75 ppm BHT as inhibitor, 99.8% bei Sigma-Aldrich, abgerufen am 14. Februar 2013 (PDF).
- Eintrag zu 1,3-dioxolane im Classification and Labelling Inventory der Europäischen Chemikalienagentur (ECHA), abgerufen am 1. August 2016. Hersteller bzw. Inverkehrbringer können die harmonisierte Einstufung und Kennzeichnung erweitern.
- Schweizerische Unfallversicherungsanstalt (Suva): Grenzwerte – Aktuelle MAK- und BAT-Werte (Suche nach 646-06-0 bzw. 1,3-Dioxolan), abgerufen am 2. November 2015.
- David R. Lide (Hrsg.): CRC Handbook of Chemistry and Physics. 90. Auflage. (Internet-Version: 2010), CRC Press/Taylor and Francis, Boca Raton, FL, Standard Thermodynamic Properties of Chemical Substances, S. 5-24.
- von Karl-Heinz Lautenschläger, Werner Schröter, Andrea Wanninger: Taschenbuch der Chemie – Karl-Heinz Lautenschläger, Werner Schröter, Andrea Wanninger. Harri Deutsch Verlag, 2005, ISBN 978-3-8171-1760-4, S. 451 (eingeschränkte Vorschau in der Google-Buchsuche).
- Vishnu Ji Ram; Arun Sethi; Mahendra Nath; Ramendra Pratap: The Chemistry of Heterocycles – Nomenclature and Chemistry of Three-to-Five Membered Heterocycles, Elsevier 2017, ISBN 978-0-08-101033-4.
- Cherkaskaya, E.L.; Petrenkova, Z.E.; Tur, A.M.; Lubinova, V.I.: Phase Equilibrium of Liquid-Steam in System of Dioxolane-Water in Zh. Prikl. Khim. (Leningrad) 41 (1968) 2553–2554.
- E. S. Domalski, E. D. Hearing: Heat Capacities and Entropies of Organic Compounds in the Condensed Phase. Volume III. in : J. Phys. Chem. Ref. Data 25 (1996) 1–525, doi:10.1063/1.555985.
- Clegg, G.A.; Melia, T.P.: Thermodynamics of polymerization of heterocyclic compounds. Part V. The heat capacity, entropy, enthalpy and free energy of 1,3-dioxolan and poly-1,3-dioxolan in Polymer 10 (1969) 912–922.
- Chemsafe Datenbank für sicherheitstechnische Kenngrößen im Explosionsschutz, PTB Braunschweig/BAM Berlin, abgerufen am 1. Juni 2021.
- Abdelkhalik, A.; Askar, E.; Markus, D.; Stolz, T.; Brandes, E.; Zakel; S.: Explosion regions of 1,3-dioxolane/nitrous oxide and 1,3-dioxolane/air with different inert gases - Experimental data and numerical modelling in J. Loss Prev. Proc. Ind. 71 (2021) 104496, doi:10.1016/j.jlp.2021.104496.
- Community rolling action plan (CoRAP) der Europäischen Chemikalienagentur (ECHA): 1,3-dioxolane, abgerufen am 26. März 2019.


