1,1,2-Trichlorethan
1,1,2-Trichlorethan ist eine organische Verbindung aus der Gruppe der Organochlorverbindungen und aliphatische Chlorkohlenwasserstoffe. Es ist isomer zu 1,1,1-Trichlorethan.
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
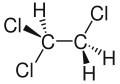 | |||||||||||||||||||
| Keile zur Verdeutlichung der Geometrie | |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | 1,1,2-Trichlorethan | ||||||||||||||||||
| Andere Namen |
| ||||||||||||||||||
| Summenformel | C2H3Cl3 | ||||||||||||||||||
| Kurzbeschreibung |
farblose flüchtige Flüssigkeit mit angenehmem Geruch[1] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 133,40 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
flüssig[1] | ||||||||||||||||||
| Dichte |
1,44 g·cm−3[1] | ||||||||||||||||||
| Schmelzpunkt | |||||||||||||||||||
| Siedepunkt |
113,65 °C[1] | ||||||||||||||||||
| Dampfdruck | |||||||||||||||||||
| Löslichkeit |
schlecht in Wasser (4,5 g·l−1 bei 20 °C)[1] | ||||||||||||||||||
| Brechungsindex |
1,471 (20 °C)[2] | ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| MAK | |||||||||||||||||||
| Thermodynamische Eigenschaften | |||||||||||||||||||
| ΔHf0 |
−190,8 kJ/mol[5] | ||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Brechungsindex: Na-D-Linie, 20 °C | |||||||||||||||||||
Gewinnung und Darstellung
Dargestellt werden kann 1,1,2-Trichlorethan durch Weiterchlorierung von 1,2-Dichlorethan.
Eigenschaften
1,1,2-Trichlorethan ist eine süßlich riechend Flüssigkeit, welche schlecht löslich in Wasser ist. Ihre Dämpfe sind viel schwerer (4,61-mal so schwer) als Luft.
Bei starker Erhitzung oder in hellem Licht zersetzt sich 1,1,2-Trichlorethan, wobei verschiedene Chlorverbindungen (z. B. Chlorwasserstoff, Phosgen) entstehen.
Verwendung
1,1,2-Trichlorethan kommt hauptsächlich als Zwischenprodukt bei der Herstellung von anderen Organochlorverbindungen wie Vinylidenchlorid (durch HCl Abspaltung[6]) vor. Als Lösungsmittel findet es nur beschränkte Anwendung zur Lösung von Chlorkautschuk.[7]
Sicherheitshinweise
1,1,2-Trichlorethan ist sehr toxisch für Herz, Leber und Niere.[8] Der Einsatz von 1,1,2-Trichlorethan in Produkten außerhalb von chemischen Anlagen bzw. bei Produkten, aus denen eine Freisetzung möglich ist, ist verboten.[9]
Siehe auch
Einzelnachweise
- Eintrag zu 1,1,2-Trichlorethan in der GESTIS-Stoffdatenbank des IFA, abgerufen am 8. Januar 2018. (JavaScript erforderlich)
- Datenblatt 1,1,2-Trichlorethan bei Sigma-Aldrich, abgerufen am 5. März 2011 (PDF).
- Eintrag zu 1,1,2-trichloroethane im Classification and Labelling Inventory der Europäischen Chemikalienagentur (ECHA), abgerufen am 1. Februar 2016. Hersteller bzw. Inverkehrbringer können die harmonisierte Einstufung und Kennzeichnung erweitern.
- Schweizerische Unfallversicherungsanstalt (Suva): Grenzwerte – Aktuelle MAK- und BAT-Werte (Suche nach 79-00-5 bzw. 1,1,2-Trichlorethan), abgerufen am 2. November 2015.
- David R. Lide (Hrsg.): CRC Handbook of Chemistry and Physics. 90. Auflage. (Internet-Version: 2010), CRC Press/Taylor and Francis, Boca Raton, FL, Standard Thermodynamic Properties of Chemical Substances, S. 5-22.
- Beschreibung wichtiger Alkene und ihrer Herstellung.
- Falbe Jürgen; Regitz Manfred: RÖMPP Lexikon Chemie, 10. Auflage, 1996-1999 Band 6: T - Z. Georg Thieme Verlag, 2014, ISBN 978-3-13-200071-1 (eingeschränkte Vorschau in der Google-Buchsuche).
- Informationen zu Erkrankungen durch Halogenkohlenwasserstoffe von der Universität Rostock (Memento vom 10. Februar 2012 im Internet Archive).
- Richtlinie 76/769/EWG für gefährlicher Stoffe (Memento vom 29. September 2007 im Internet Archive).

