Zementit
Zementit ist eine Verbindung von Eisen und Kohlenstoff der Zusammensetzung Fe3C (ein Eisencarbid mit Einlagerungsverbindungen) und tritt als metastabile Phase in Stahl und weißem Gusseisen auf. Er hat seinen Namen von „Zement“ (Zementstahl, früher „cämentierter Stahl“ = aufgekohlter Stahl)[5] und wird in Reinform gelegentlich auch als Nichtoxidkeramik betrachtet. Zementit ist eine intermediäre Phase,[6] eine sogenannte Häggs-Phase (Koordinationsphase).[7] Diese Phasen sind geometrisch bedingt, das Radienverhältnis bestimmt die Struktur.
| Kristallstruktur | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
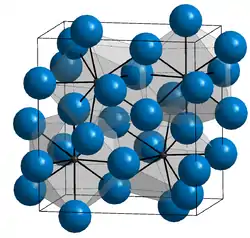 | ||||||||||||||||
| _ Fe _ C Es sind die zweifach überkappt-prismatischen Koordinationspolyeder von Fe um C gezeigt. | ||||||||||||||||
| Gitterparameter |
a= 0,4514 nm, b= 0,5080 nm, c= 0,6734 nm | |||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | Zementit | |||||||||||||||
| Andere Namen |
| |||||||||||||||
| Verhältnisformel | Fe3C | |||||||||||||||
| Kurzbeschreibung |
graue orthorhombische Kristalle[1] | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 179,55 g·mol−1 | |||||||||||||||
| Aggregatzustand |
fest | |||||||||||||||
| Dichte |
7,69 g·cm−3[2] | |||||||||||||||
| Schmelzpunkt |
1837 °C[1] | |||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Thermodynamische Eigenschaften | ||||||||||||||||
| ΔHf0 |
25,1 kJ/mol[4] | |||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||
Vorkommen
In der Mineralogie ist Zementit unter dem Namen Cohenit als meteoritisches Nickel-Eisen-Mineral in Verbindung mit Cobalt ([Fe, Ni, Co]3C) bekannt.
Gewinnung und Darstellung
Als Primärzementit (Fe3CI) wird Zementit bezeichnet, der durch eine Kristallisation aus der Schmelze hervorgegangen ist (Linie CD im Eisen-Kohlenstoff-Diagramm). Sekundärzementit (Fe3CII) entsteht durch Ausscheidung aus dem Austenit (Linie ES), Tertiärzementit (Fe3CIII) durch Ausscheidung aus dem Ferrit (Linie PQ). Besonders wichtig sind die eutektischen bzw. eutektoiden Phasengemische Ledeburit bei Gusseisen und Perlit bei Stahl. Primärzementit bildet aus der Schmelze zunächst grobe Nadeln. Sekundärzementit scheidet sich, aufgrund abnehmender Löslichkeit des Eisens für Kohlenstoff, als Korngrenzen- oder Schalenzementit um die Austenit- bzw. späteren Perlitkristalle ab. Metallografisch erscheint der Zementit im Perlit als Streifenzementit. Tertiärzementit lagert sich an den nächstliegenden vorhandenen Zementit an, aus reinem Ferrit scheidet er sich an den Korngrenzen aus. Daneben kann durch Weichglühen erreicht werden, dass der Zementit sich globular zusammenballt.[5][8]
Zementit entsteht auch durch thermisches Zersetzen von Berliner Blau (Eisenhexacyanidoferrat).
Eigenschaften
Bei langen Glühzeiten oder extrem langsamer Abkühlung zerfällt der metastabile Zementit in Eisen und Graphit. Die Kristallstruktur von Zementit ist relativ kompliziert. In einer orthorhombischen Elementarzelle befinden sich zwölf Eisen- und vier Kohlenstoffatome, wobei die Kohlenstoffatome relativ unregelmäßig (zweifach überkappt trigonal-prismatisch) von acht Eisenatomen umgeben sind. Zementit ist sehr hart (HV=800) und verschleißfest, aber spröde und daher schlecht plastisch verformbar. Er hat eine geringere Dichte als Eisen und ist unterhalb seiner Curietemperatur von 215 °C ferromagnetisch.
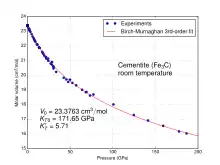
Da Kohlenstoff eine der möglichen leichten Komponenten in den Eisenlegierungen ist, die die Kerne von Planeten bilden, werden die Eigenschaften von Eisen-Kohlenstoff-Verbindungen auch unter extrem hohen Drücken und/oder Temperaturen experimentell untersucht. Die nebenstehende Grafik zeigt das Molvolumen als Funktion des Drucks bei Zimmertemperatur für Zementit als einer vereinfachten Modellsubstanz für Cohenit.

Die Zerspanbarkeit ist sehr schlecht. Praktisch lässt sich Zementit nicht zerspanen (Fräsen, Bohren etc.). Es kann in freier Form auftreten oder als Bestandteil von Perlit oder Bainit vorkommen und die Zerspanbarkeit dieser Gefüge beeinflussen. Wegen der großen Härte verursacht es einen hohen abrasiven Werkzeugverschleiß.[9][10] Siehe auch: Zerspanbarkeit von Stahl.
Verwendung
Eisencarbid kann als Katalysator bei chemischen Reaktionen (zum Beispiel der Spaltung von Wasser in Wasserstoff und Sauerstoff) eingesetzt werden.[11]
Siehe auch
Weblinks
Einzelnachweise
- Eintrag zu Eisencarbid. In: Römpp Online. Georg Thieme Verlag, abgerufen am 21. August 2013.
- Triiron carbide (WebElements)
- Dieser Stoff wurde in Bezug auf seine Gefährlichkeit entweder noch nicht eingestuft oder eine verlässliche und zitierfähige Quelle hierzu wurde noch nicht gefunden.
- David R. Lide (Hrsg.): CRC Handbook of Chemistry and Physics. 90. Auflage. (Internet-Version: 2010), CRC Press/Taylor and Francis, Boca Raton, FL, Standard Thermodynamic Properties of Chemical Substances, S. 5-19.
- Jürgen Gobrecht, Erhard Rumpler: Werkstofftechnik - Metalle. Oldenbourg, München 2006, ISBN 3-486-57903-7, S. 139ff.
- Hans-Jürgen Bargel, Günter Schulze: Werkstoffkunde. 12. Auflage. Springer-Verlag GmbH Deutschland, Berlin 2018, ISBN 978-3-662-48629-0, 1.5.4 Intermediäre Kristalle, S. 43.
- Physikalische Grundlagen der Materialkunde - Springer. doi:10.1007/978-3-540-71105-6.
- Ausbildungsformen des Zementit bei Stahl (metallograf)
- Herbert Schönherr: Spanende Fertigung, Oldenbourg, 2002, S. 60.
- Fritz Klocke, Wilfried König: Fertigungsverfahren Band 1: Drehen, Fräsen, Bohren, Springer, 8. Auflage, 2008, S. 274.
- Magnetische Blätter - Skelett eines Blattes ermöglicht filigrane Eisenkarbid-Strukturen für effiziente Katalysatoren (wissenschaft-aktuell)