Xenonhexafluorid
Xenonhexafluorid ist eine chemische Verbindung aus der Gruppe der Edelgasverbindungen. Es ist ein farbloser Feststoff.
| Strukturformel | |||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
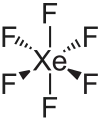 | |||||||||||||
| Allgemeines | |||||||||||||
| Name | Xenonhexafluorid | ||||||||||||
| Andere Namen |
Xenon(VI)-fluorid | ||||||||||||
| Summenformel | XeF6 | ||||||||||||
| Kurzbeschreibung |
farbloser Feststoff[1] | ||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||
| |||||||||||||
| Eigenschaften | |||||||||||||
| Molare Masse | 245,28 g·mol−1 | ||||||||||||
| Aggregatzustand |
fest | ||||||||||||
| Dichte |
3,56 g·cm−3[2] | ||||||||||||
| Schmelzpunkt | |||||||||||||
| Siedepunkt |
75,6 °C[3] | ||||||||||||
| Dampfdruck | |||||||||||||
| Sicherheitshinweise | |||||||||||||
| |||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||||||
Herstellung
Alle Xenonfluoride werden durch thermische oder photochemische Aktivierung von Xenon/Fluor-Gemischen hergestellt. Welches Produkt entsteht, hängt vom Stoffmengenverhältnis sowie den Reaktionsbedingungen ab (Druck, Temperatur). So kann Xenonhexafluorid durch langandauerndes Erhitzen von Xenon mit starken Fluor-Überschuss (1:20) bei 300 °C und einem Druck von 200 – 300 bar gewonnen werden[1].
Die Aufreinigung kann durch Zersetzung von Dinatriumfluoroxenat(VI) bei 120 °C erfolgen.
Eigenschaften
Physikalische Eigenschaften
Das Molekül ist in der Gasphase verzerrt oktaedrisch aufgebaut, wobei der Xenon-Fluor-Abstand im gasförmigen Zustand 189 pm beträgt.[3] Im festen Zustand besteht Xenon(VI)-fluorid aus - und -Ionen, welche zu tetrameren oder hexameren Ringen verbrücken. Bei tiefen Temperaturen bildet die Verbindung in nicht-ionisierenden Medien gelöst ebenfalls Tetramere aus. Die gelbgrüne Schmelze der Verbindung setzt sich neben den Tetrameren auch aus Monomeren zusammen und besitzt eine geringe Eigenleitfähigkeit.[5] Die eintretende Gelbfärbung während der Erhitzung ist reversibel, sodass der Festkörper nach dem Erkalten der Schmelze wieder farblos ist.[1]
Chemische Eigenschaften
Xenonhexafluorid ist von allen Xenonfluoriden die am stärksten oxidierende Verbindung und konnte bisher nicht weiter oxidiert werden. Es reagiert sowohl als Fluorid-Akzeptor als auch -Donator. Im Allgemeinen reagiert die Verbindung mit Metallfluoriden des Typ wie Antimonpentafluorid als Donator.
Mit Alkalimetallfluoriden reagiert Xenon(VI)-fluorid dagegen als Akzeptor zu sechswertigen Fluoroxenaten, von denen die Salze der höheren Homologe mit dem zweifach negativen Anion die höchste Stabilität besitzen.[5]
Xenonhexafluorid hydrolysiert schrittweise unter Bildung von Xenontrioxid.
Siehe auch
- Xenondifluorid XeF2
- Xenontetrafluorid XeF4
Einzelnachweise
- C. L. Chernick and J. G. Malm: Xenon hexafluoride. In: Henry F. Holtzclaw, Jr. (Hrsg.): Inorganic Syntheses. Band 8. McGraw-Hill Book Company, Inc., 1966, S. 258–260 (englisch).
- Datenblatt bei Webelements.
- Eintrag zu Xenon-Verbindungen. In: Römpp Online. Georg Thieme Verlag, abgerufen am 3. Januar 2018.
- Dieser Stoff wurde in Bezug auf seine Gefährlichkeit entweder noch nicht eingestuft oder eine verlässliche und zitierfähige Quelle hierzu wurde noch nicht gefunden.
- Arnold F. Hollemann, Nils E. Wiberg: Anorganische Chemie. Band 1. de Gruyter, Berlin 2017, ISBN 978-3-11-026932-1, S. 467–468.
- S. K. Jain, Shailesh K. Jain: Conceptual Chemistry Volume-I For Class XII. S. Chand Publishing, ISBN 81-219-1623-2, S. 7–127.