Wundheilung
Mit Wundheilung bezeichnet man den Verschluss einer Wunde durch Wiederherstellung des beschädigten Körpergewebes durch neugebildetes Bindegewebe in Verbindung mit Epithelisierung (Überwachsen mit Epithelzellen). Es handelt sich um einen natürlichen Prozess, der therapeutisch und mit Wundauflagen unterstützt werden kann. Eine Verletzung, bei der die Wundheilung sich verzögert oder nicht mehr voranschreitet, wird zu einer chronischen Wunde.
Der Artikel Wunde behandelt den Prozess der Wundheilung nach einer Wundsetzung.
| Schürfwunde an Hand | ||||
 |
 |
 |
 | |
| Tage nach Verletzung (etwa) | ||||
| 0 | 3 | 17 | 30 | |
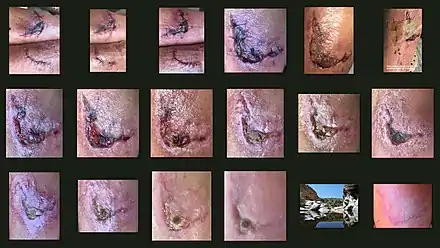
Verlauf
Der Begriff der Wundheilung beschreibt einen natürlichen biologischen Prozess und fasst die Vorgänge zusammen, die zur Zusammenführung von getrenntem und Wiederherstellung von zerstörtem Gewebe führen.[1] Diese Abläufe setzen bereits unmittelbar nach der Wundentstehung ein, wie mit enzymhistochemischen Verfahren nachgewiesen werden konnte. Die Blutplättchen treten an die geschädigte Stelle und versuchen sie zu verschließen. In seltenen Fällen entsteht über Exsudation (Flüssigkeitsabsonderung) eine Schorfbildung, was auch den oft mit der Wundheilung einhergehenden Juckreiz auslöst.
Dem Arzt obliegt es lediglich, durch Optimierung der Bedingungen Beschwerden (Wundschmerz) zu lindern, einer Komplikation oder Infektion vorzubeugen, eine Verzögerung zu verhindern und das kosmetische Resultat so optimal wie möglich zu gestalten. Eine echte Wundheilungsbeschleunigung gibt es noch nicht, allerdings ist das je nach Wundtyp trockene oder feuchte Wundmilieu von Vorteil. Das Ziel der Heilung ist eine völlige Wiederherstellung (restitutio ad integrum), funktionell wie kosmetisch, die aber in vollem Umfang selten zu erreichen ist. Da ein Wundstarrkrampf und eine Sepsis (Blutvergiftung) entstehen könnte, sind spezielle Vorsorge-Impfungen unerlässlich. Fehlen diese, sollten sie unmittelbar gesetzt werden. Eine aufgrund eines Unfalls entstandene Wunde sollte per Antisepsis (Desinfektion) von Keimen befreit werden, zudem sind Fremdkörper für die Heilung hinderlich. Große offene Wunden müssen entweder geklammert, genäht oder geklebt werden. Oft bleibt eine sichtbare Narbe zurück.
Beim frühestens acht Stunden nach der Erstaufbringung erforderlichen bzw. empfohlenen Verbandwechsel beobachten Ärzte bzw. Pflegepersonen den Heilungsfortschritt, reinigen die Wundumgebung und das Wundgebiet und schützen die Wunde durch eine erneute künstliche Abdeckung. Sind Wunden reizlos und physikalisch geschlossen, können sie durch die Sauerstoffzufuhr beschleunigt offen komplett ausheilen.
Phasen
Es werden mehrere Phasen der Wundheilung, die zeitlich überlappend nacheinander auftreten, unterschieden. Diese Einteilung ist nicht einheitlich und nicht unwidersprochen; sie basiert auf morphologischen Leitkriterien und ihre kennzeichnenden Effekte sind für das bloße Auge bei sekundär heilenden Wunden sichtbar. Die Abgrenzung der Phasen der Wundheilung voneinander unterscheidet sich je nach Quelle und ist willkürlich:[1]
- Latenzphase, wird manchmal nicht separat erwähnt und/oder mit der nachfolgenden Wundheilungsphase zusammengefasst
- Exsudative Phase, wird auch als Entzündungs-, Inflammations- oder Reinigungsphase bezeichnet
- Resorptive Phase, wird manchmal nicht separat aufgeführt, sondern mit der vorigen oder der nachfolgenden Wundheilungsphase zusammengefasst
- Proliferative Phase oder Granulationsphase
- Reparative Phase oder Epithelisierungs- bzw. Regenerationsphase
Eine Einteilung in drei Phasen kann ebenfalls erfolgen:
- Latenzphase (1. bis 3. Tag)
- Proliferationsphase (4. bis 7. Tag)
- Reparationsphase (ab dem 8. Tag)[2]
Latenzphase
Diese Phase ist nicht generell in jeder Gliederung der verschiedenen Wundheilungsphasen enthalten. Ausgangspunkt jeder Wundheilung ist eine Störung des Blutflusses durch Kapillarverletzungen. Die initiale Blutung leitet eine Blutgerinnung ein, das zerstörte Blutgefäß wird durch ein Gerinnsel (Blutpfropf) verschlossen. Nun beginnt die manchmal als separate Phase genannte Latenzphase (vom lat. Wort für „im Verborgenen“; auch Ruhephase genannt), da anscheinend keine makro- und mikroskopisch sichtbaren weiteren Reaktionen eintreten. Diese Phase wird in vielen Einteilungsschemata der „Exsudationsphase“ zugeordnet, da sie meist kurz und nur schlecht abzugrenzen ist.
Exsudationsphase
Die Bezeichnung stammt vom lat. Begriff Exsudat – austretende Flüssigkeit. Dieser Vorgang wird auch als Reinigungs-, Inflammations- oder Entzündungsphase bezeichnet. Durch die Zerstörung des Gewebes bei der Wundentstehung bluten die zerstörten Blutgefäße zunächst heftig. Dies trägt dazu bei, Fremdkörper aus der Wunde zu spülen. Kurze Zeit später verengen sich jedoch die verletzten Gefäße und der Blutfluss lässt nach. Dieser Vorgang wird als Vasokonstriktion bezeichnet und dauert etwa fünf bis zehn Minuten. Auf die Vasokonstriktion folgt wieder eine Ausweitung der Blutgefäße, die sogenannte Vasodilatation. Die zunehmende Durchblutung führt zu einer Rötung und Erhöhung der Hauttemperatur im Wundbereich. Gleichzeitig erhöht sich die Durchlässigkeit der Kapillarwände, damit finden vermehrt Blutzellen ihren Weg in den Wundbereich. Hinzu kommt Lymphe, die aus den beschädigten Lymphgefäßen austritt.[1] Die Zunahme der Flüssigkeit im Gewebe nahe der Wunde verursacht eine Schwellung, das sogenannte Wundödem. Durch den nun einsetzenden Austritt von Wundexsudat werden Rückstände der erfolgten Gewebszerstörung, wie Zelltrümmer, aber auch Fremdkörper, sowie Keime und Erreger aus der Wunde „herausgeschwemmt“. Diese Phase kann bis zu vier Tage andauern und sich um einige Tage mit der folgenden Wundheilungsphase überschneiden.[3] In der Exsudationsphase sind die Zellen und Hormone des Immunsystems wesentlich beteiligt und zwar nicht nur zur Abtötung eingedrungener Bakterien oder Viren, sondern auch zur Stimulation der Heilung selbst.
Resorptive Phase
Die Blutgerinnsel, welche die Gefäße verschließen, bestehen hauptsächlich aus Thrombozyten, die sich aufgrund ihrer Oberflächenstruktur miteinander verbinden und mit chemischen Signalen weitere Blutplättchen in den Wundbereich lotsen. Als Nächstes bildet sich ein Netz aus Fibrinfasern. Dieses bei der Gerinnselbildung initiierte Fibrinnetz ermöglicht ein Verkleben aneinanderliegender Wundränder. Klares Wundexsudat, welches im Wesentlichen aus Blutserum und Lymphe besteht, ist mit Entzündungszellen durchsetzt. Unter sauberen Verhältnissen sollte diese Phase nicht länger als ein bis drei Tage dauern. Im Verlauf dieser Phase nimmt die Zytokinese (Zellteilung) im Wundgebiet zu. Monozyten reifen in dem Wundgebiet zu Makrophagen, die Zelltrümmer und Pfropf abräumen. Fibroblasten, die sich aus eingewanderten, aber auch aus im Wundrand ortständigen Bindegewebszellen entwickeln und durch Zellteilung vermehren, vollbringen in der folgenden Phase die eigentliche Aufbauarbeit. Hierzu ist ein feuchtes Wundmilieu nötig und wird durch moderne Wundauflagen nachgebildet bzw. unterstützt.
Granulationsphase oder proliferative Phase
Von den Wundrändern aus bauen sich (induziert durch eine von Fibronektin und andere Proteasen bewirkte Fibroblastenvermehrung[4]) Kollagenfasern entlang dem früher gebildeten Fibrinnetz auf und bilden neues Bindegewebe. Darin lagern sich weitere Zellen ein. Es entsteht körniges Granulationsgewebe, das die Wunde von unten her füllt und sich allmählich zusammenzieht. Dadurch schließt sich die Wunde weiter. Durch Proliferation (lat. für ‚Bildung, Entstehung‘) von neuem Bindegewebe wird der Wunddefekt auf diese Weise zunehmend aufgefüllt. Synonym hierfür ist: Granulationsphase. Hierfür ist das sichtbare Granulationsgewebe namensgebend (lat. Granulum = ‚Körnchen‘; das Füllgewebe sieht grob gekörnt aus). Hand in Hand mit der zellreichen Auffüllung eines Wunddefektes geht der Abbau des Fibrinnetzes (Fibrinolyse) durch Plasmin einher. Zugleich nimmt durch einsprossende Haargefäße der Gefäßreichtum (lat. Vaskularisation) zu. Die Fibroblasten produzieren hexosaminhaltige saure Muco-Polysaccharide, als Mutterboden (extrazelluläre Grundsubstanz des Bindegewebes) und über intrazelluläre Vorstufen die schließlich extrazellulären kollagenen Bindegewebsfasern. Der zeitliche Ablauf ist sehr komplex und unterliegt dem Einfluss zahlreicher Wachstumsfaktoren (Zytokine). Das Granulationsgewebe kann sich nur zeitgemäß entwickeln, wenn keine allgemeine und örtliche Mangelernährung (keine Mangeldurchblutung) und keine Stoffwechselerkrankungen das Wachstum behindern. Bei sehr kleinen Wunden kann dieses Gewebe schon nach wenigen Stunden entstehen (nach Nadelstichverletzungen innerhalb weniger Minuten). Üblicherweise setzt die Granulationsphase zwischen dem zweiten und dem vierten Tag ein und reicht bis zum 14. Tag der Wundheilung. Sie läuft über viele Tage gleichzeitig mit der nachfolgenden Wundheilungsphase ab.[3] Etwa zwischen dem sechsten und zehnten Tag beginnt die Ausreifung der kollagenen Fasern.
Regenerationsphase, Reparationsphase oder reparative Phase
In der Regenerationsphase wird die Wunde an der Oberfläche durch Epithelisation (nach Epithel – Deckgewebe; → Epidermis) geschlossen. Der Durchmesser einer gut granulierenden Wunde schließt sich zu einem Drittel ausschließlich durch Schrumpfung, zu zwei Dritteln durch Neubildung (Zellteilung) von Oberflächenzellen und Zellwanderung auf der „Gleitbahn“ verflüssigten Fibrins vom Wundrand her zur Wundmitte. Die Voraussetzung für den komplikationslosen Ablauf der reparativen Phase ist ein ausreichend feucht-warmes Wundmilieu, das eine Einwanderung frischer Zellen begünstigt. Das Austrocknen des Wundgrundes kann Wundheilungsstörungen zur Folge haben.[1] Das Füllbindegewebe (Granulationsgewebe) bildet zunehmend Kollagenfasern aus, womit die Wiederherstellung aller Hautschichten nahezu abgeschlossen ist. Am Schluss bildet sich auf der Wundoberfläche durch die so genannte Epithelisation eine neue Hautschicht. Als Ergebnis aller Vorgänge entsteht eine Narbe. Sie überragt die gesunde Haut zuerst und sinkt mit der Zeit durch Straffung des Bindegewebes ein. Das Narbengewebe unterscheidet sich deutlich von der umgebenden Haut, da es keine Haar- oder Schweißdrüsen und auch keine Melanocyten (Pigmentzellen) enthält. Da keine elastischen Fasern gebildet werden, verfügt das ursprünglich gefäßreiche Narbengewebe („rote Narbe“) als kapillar- und zellarmes Bindegewebe („weiße Narbe“)[5] über keine Elastizität und ist unvermeidbar minderwertig, weswegen in der Therapieplanung eine minimale Narbe angestrebt wird.
Remodellierung
An die Wundheilung schließt sich eine längere Phase von Um- und Ausbauvorgängen an, in der sich die Gewebestruktur weiter verändert.[1] Diese Prozesse werden mit den Begriffen "Remodellierung" oder "Maturation" bezeichnet. Manche Einteilungen bevorzugen eine besondere Bezeichnung für die weitere funktionelle Anpassung des Narbengewebes (Reifung) an die örtlich verschiedenen Anforderungen. Andere halten diesen Prozess der Regeneration zugehörig. Die weitere Zunahme der Reißfestigkeit des Narbengewebes hängt von der Vernetzung, Verfestigung und Ausrichtung der Kollagenfasern ab. Der Wassergehalt des Gewebes nimmt ab, die anfänglich das Hautniveau gering überstehende Narbe schrumpft regelhaft unter Hautniveau. Auch nimmt der Gefäßreichtum des Narbengewebes ab. Die ursprünglich frisch rote Narbe wird weiß. Dieser Prozess dauert ein bis zwei Jahre.
Wundheilungsformen
Epitheliale Wundheilung findet bei oberflächlichen Wunden statt, bei denen lediglich die Epidermis betroffen ist – etwa bei Abschürfungen – und ist nach wenigen Tagen narbenfrei abgeschlossen. Die Epitheliale Wundheilung ist ein regenerativer Vorgang, während bei den beiden anderen Wundheilungsarten eine Reparation stattfindet.[1]
Primäre Wundheilung: Primär heilende (p. p. = sanatio per primam intentionem) Wunden sind als Wunden definiert, deren Ränder ohne Infektion bündig schließen, z. B. auch Operationswunden, die vernäht wurden.
Sekundäre Wundheilung: Sekundär heilende (p. s. = sanatio per secundam intentionem) Wunden sind solche, bei denen ein Gewebsdefekt vorliegt. Diese Wunden sind bakteriell infiziert (mit Bakterien besiedelt). Die Keimart kann durch einen Wundabstrich identifiziert und hierbei auch die Wirksamkeit von Antibiotika mittels Antibio- oder Resistogramm vorhergesagt werden.
Ihre Bedeutung hat diese Unterteilung bei der Beurteilung der OP-Verfahren. Unter vergleichbaren Bedingungen, d. h. gleiche Operation und gleichartiges Krankengut, ist die höhere Anzahl sekundär geheilter Wunden ein negatives Zeichen (Fragliche OP-Sterilität, pflegerische Wundversorgung usw.).
Komplikationen
Verschiedene Faktoren können den Heilungsverlauf (etwa als Wundheilungsstörung) bzw. die Narbenbildung negativ beeinflussen. Die Folge sind große, deformierende oder insuffiziente Narben oder chronische Wunden.
Störfaktoren allgemeiner Art
- Bei großen Wunden kommt es durch die vermehrte Exsudation zu einem ausgedehnten Granulationsgewebe und dadurch zu einem negativen Einfluss auf die Heilung (Heilung per secundam intentionem).
- Einseitige Wundlagerung kann Dekubitus oder Ulcus cruris hervorrufen, welches für die Heilung eher kontraproduktiv ist.
- Frühzeitige Belastung kann zur Wunddehiszenz oder zum Narbenbruch führen.
- Durch die kontraktilen Eigenschaften der Myofibroblasten kommt es zu einer Volumenreduktion der Narbe und damit eventuell zu Narbenkontrakturen.
- Infektionen der Wunde begünstigen die Entstehung von Granulationsgewebe und damit überschießender Narbenbildung.
Auch bei optimaler Versorgung kommt es manchmal zu überschießender Bindegewebsvermehrung (Keloid). Die Ursache dafür ist unbekannt.
Systemische Erkrankungen
Gewisse systemische Erkrankungen können zu Komplikationen führen.
- Fibroblasten sind von einem Sauerstoffpartialdruck von mindestens 15 mmHg abhängig. Demzufolge haben Erkrankungen, die eine verminderte Blut- und damit Sauerstoffzufuhr bedingen, eine negative Auswirkung auf die Heilung (v. a. arterielle Verschlusskrankheit, Arteriosklerose)
- Diabetes mellitus bedingt die schlechtere Wundheilung durch zwei Faktoren: der schlechteren Durchblutung aufgrund Gefäßveränderungen einerseits und einer verminderten körpereigenen Infektionsbekämpfung andererseits.
- Glukokortikoide hemmen die Wundheilung über die Phospholipase A2.
- Veränderungen des Blutbildes im Sinne einer Granulozytopenie bzw. angeborene Defekte der Chemotaxis oder der Phagozytose haben ebenfalls eine herabgesetzte Wundheilung zur Folge.
Chronische oder nicht heilende Wunden
In einigen Wunden verschiebt sich das Zusammenwirken abbauender (= kataboler) und aufbauender (= anaboler) Reaktionen zuungunsten der konstruktiven Vorgänge. Der gestörte Heilungsprozess stagniert dann meist in der ersten Phase der Wundheilung, der Entzündungsphase. Solche Wunden werden als Chronische Wunden bezeichnet. Die Definition dieses Begriffes ist international uneinheitlich.[6] So besteht beispielsweise Uneinigkeit, wie lange eine Wunde bestehen sollte, um als chronische Wunde bezeichnet werden zu können. Ebenfalls ist nicht einheitlich definiert, ob das Einsetzen oder die Anzeichen einer Abheilung diesen Status wieder aufhebt. Die Fachgesellschaft Initiative Chronische Wunden definiert einen Zeitraum von acht Wochen als Kennzeichen einer chronischen Wunde, betont aber gleichzeitig, dass bestimmte Wunden, wie das Ulcus cruris venosum, der Dekubitus oder das Diabetische Fußulcus vom Zeitpunkt der Entstehung als chronische Wunden anzusehen sind.[7]
Tissue Management
Im Fall von chronischen Wunden setzt sich die Entzündungsphase fort, wodurch die Regenerationsphase verzögert oder gar blockiert wird. Die Methoden der Regenerativen Medizin (Tissue Engineering) zielen darauf ab, auch in diesen Fällen einen Wundverschluss zu erzielen. Dazu werden entweder körpereigene Zellen oder die von Fremdspendern für die Herstellung von Hautäquivalenten verwendet. So werden z. B. die Keratinozyten, Zellen der Epidermis, in einem drei- bis vierwöchigen Prozess vermehrt und im Anschluss direkt oder mittels eines Trägers auf die Wunde verbracht. Die sich anschließende Heilung ist in ihrer Dauer abhängig von den Rahmenbedingungen.[8]
Sonstige Komplikationen
Gewebe, das durch Bestrahlung – beispielsweise durch eine Strahlentherapie – geschädigt wurde, weist eine geringere Heilungsfähigkeit auf.[9]
Aktive Maßnahmen
Als eine aktive Maßnahme zur Förderung der Wundheilung wird die Adulte-Stammzell-Therapie untersucht.[10] [11][12]
Mit Hilfe eines modernen Wundmanagements heilen Wunden schneller.[13]
Für Calciumcarbonat wird eine Förderung der Wundheilung in der Zahnheilkunde angegeben.[14]
Literatur
- Kerstin Protz: "Moderne Wundversorgung. Praxiswissen, Standards und Dokumentation", Elsevier Verlag, 8. überarbeitete Auflage, München 2016, ISBN 978-3-437-27885-3
- Anette Vasel-Biergans, Wiltrud Probst: Wundversorgung für die Pflege. Ein Praxisbuch. 2. überarbeitete Auflage. Wissenschaftliche Verlagsgesellschaft Stuttgart, Stuttgart 2011, ISBN 978-3-8047-2798-4
- GMS Krankenhaushygiene Interdisziplinär. Zeitschrift der Deutschen Gesellschaft für Krankenhaushygiene (DGKH). Band 1 (2006): Die infizierte Problemwunde. [mit 33 Beiträgen]. Die infizierte Problemwunde
- P. Kujath, A. Michelsen: Wunden – von der Physiologie zum Verband. In: Deutsches Ärzteblatt, 2008, 105(13), S. 239–248.
- Klaus-Jürgen Bauknecht, Joachim Boese-Landgraf: Wunde, Wundheilung, Wundheilungsstörung, Wundbehandlung, Tetanusprophylaxe. In: Rudolf Häring, Hans Zilch (Hrsg.): Lehrbuch Chirurgie mit Repetitorium. (Berlin 1986) 2., durchgesehene Auflage. Walter de Gruyter, Berlin / New York 1988, ISBN 3-11-011280-9, S. 7–17, hier: S. 10–12 (Wundheilung).
- Klinikverbund Südwest (Hrsg.): Handbuch Versorgung von Problemwunden. November 2006 (klinikverbund-suedwest.de [PDF]).
Weblinks
Einzelnachweise
- S. Piotek, J. Toutenhahn: Physiologie der Wundheilung. In H. Lippert: Wundatlas. Georg Thieme Verlag, Stuttgart 2006, ISBN 3-13-140832-4, S. 28–33
- Klaus-Jürgen Bauknecht, Joachim Boese-Landgraf: Wunde, Wundheilung, Wundheilungsstörung, Wundbehandlung, Tetanusprophylaxe. In: Rudolf Häring, Hans Zilch (Hrsg.): Lehrbuch Chirurgie mit Repetitorium. (Berlin 1986) 2., durchgesehene Auflage. Walter de Gruyter, Berlin / New York 1988, ISBN 3-11-011280-9, S. 7–17, hier: S. 11 f. (Wundheilungsphasen).
- A. Vasel-Biergans, W. Probst: Wundversorgung für die Pflege. Ein Praxisbuch. Wiss. Verlagsges. Stuttgart, Stuttgart 2011, S. 16–22
- Klaus-Jürgen Bauknecht, Joachim Boese-Landgraf: Wunde, Wundheilung, Wundheilungsstörung, Wundbehandlung, Tetanusprophylaxe. 1988, S. 12.
- Klaus-Jürgen Bauknecht, Joachim Boese-Landgraf: Wunde, Wundheilung, Wundheilungsstörung, Wundbehandlung, Tetanusprophylaxe. 1988, S. 12.
- Joachim Dissemond: Blickdiagnose chronischer Wunden. Über die klinische Inspektion zur Diagnose, 3. Auflage, Viavital Verlag, Köln 2016, ISBN 978-3-934371-55-2, Seite 11
- Standards des ICW e. V. für die Diagnostik und Therapie chronischer Wunden. (PDF) In: Wundmanagement, Heft 2, Jahrgang 11, mhp-Verlag 2017, S. 81–86
- W. Vanscheidt, A. Ukat, V. Horak, H. Bruening, J. Hunyadi, R. Pavlicek, M. Emter, A. Hartmann, J. Bende, Th. Zwingers, T. Ermuth, R. Eberhardt: Treatment of recalcitrant venous leg ulcers with autologous keratinocytes in fibrin sealant: A multinational randomized controlled clinical trial. In: Wound Rep Reg, 15, 2007, S. 308–315.
- Frank Haubner, Elisabeth Ohmann, Fabian Pohl, Jürgen Strutz, Holger G. Gassner: Wound healing after radiation therapy: Review of the literature. In: Radiation Oncology. Band 7, 2012, S. 162, doi:10.1186/1748-717X-7-162 (englisch).
- Hoffnungsträger adulte Stammzellen. Max-Planck-Gesellschaft, 11. Februar 2008, abgerufen am 7. März 2019.
- Zellbasierte, regenerative Medizin. Bundesministerium für Bildung und Forschung, abgerufen am 10. April 2019.
- Stem cells from development to the clinic. Nature, 15. Juni 2018, abgerufen am 10. April 2019 (englisch).
- Wundheilung aktiv beschleunigen. (PDF) 20. Oktober 2011, abgerufen am 10. April 2019.
- Thomas Kindermann: Einfluss eines subgingival applizierten Calciumhydroxidpräparates auf die inflammatorische Reaktion bei Parodontitis und dessen regenerativ/reparatives Vermögen auf die parodontalen Gewebe. Hrsg.: Universität des Saarlandes. Februar 2013, S. 34 (uni-saarland.de).