Threit
Threit (1,2,3,4-Butantetrol) bezeichnet eine chemische Verbindung mit süßem Geschmack, die zur Gruppe der Zuckeralkohole (Alditole) gehört. Von Threit existieren zwei Enantiomere, (2R,3R)-Threit und (2S,3S)-Threit. Die Moleküle der beiden Threit-Formen verhalten sich zueinander wie Bild und Spiegelbild. Auch ein Gemisch dieser beiden Verbindungen wird mit Threit bezeichnet. Ein weiterer Zuckeralkohol mit derselben Summenformel wie das Threit ist das Erythrit.
| Strukturformel | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
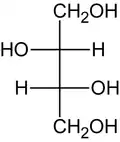 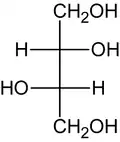 | ||||||||||||||||||||||
| (2R,3R)-Threit und (2S,3S)-Threit (Fischer-Projektion) | ||||||||||||||||||||||
| Allgemeines | ||||||||||||||||||||||
| Name | Threit | |||||||||||||||||||||
| Andere Namen |
| |||||||||||||||||||||
| Summenformel | C4H10O4 | |||||||||||||||||||||
| Kurzbeschreibung |
weißer Feststoff[1] | |||||||||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Eigenschaften | ||||||||||||||||||||||
| Molare Masse | 122,12 g·mol−1 | |||||||||||||||||||||
| Aggregatzustand |
fest[1] | |||||||||||||||||||||
| Schmelzpunkt | ||||||||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||||||||
Vorkommen
Threit kommt im Hallimasch und einigen Pflanzen vor.[2]
Herstellung
Threit kann aus dem Zucker Threose durch Reduktion der Aldehydgruppe zur Hydroxygruppe hergestellt werden. Im Labor ist dies mit Natriumborhydrid als Reduktionsmittel gut möglich. Weiterhin kann die Reduktion von Threose mit Wasserstoff erfolgen, wobei Nickel (Ni) als Katalysator dient (katalytische Hydrierung). Eine weitere Möglichkeit stellt die katalytische Hydrierung von Erythrulose dar, dabei entstehen beide Konfigurationen. Weiterhin kann Threit biotechnologisch aus Erythrit hergestellt werden. Diese Reaktion wird z. B. durch Bordetella avium katalysiert.
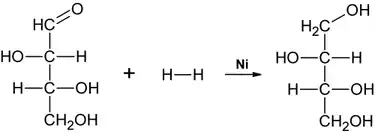
Molekülaufbau
Beide enantiomeren Formen sind optisch aktiv, da sie chiral gebaut sind. Threit verfügt mit dem zweiten und dritten Kohlenstoff-Atom über 2 Chiralitätszentren, die in den Fischer-Projektionen als Schnittpunkte der vertikalen und horizontalen Bindungen (Kreuze) dargestellt sind. Die beiden Enantiomere unterscheiden sich in der räumlichen Lage ihrer Hydroxygruppen an diesen C-Atomen. Die Bezeichnungen (2R,3R)-Threit und (2S,3S)-Threit basieren auf der Anordnung der Hydroxygruppen und folgen der Cahn-Ingold-Prelog-Konvention.
Erythrit hat dieselbe Summenformel und dieselbe Konstitution wie Threit, unterscheidet sich jedoch in der Konfiguration. In der Fischer-Projektion von Erythrit liegen die Hydroxygruppen am zweiten und dritten C-Atom auf der gleichen Seite.
Einzelnachweise
- Datenblatt DL-Threitol bei Sigma-Aldrich, abgerufen am 24. April 2011 (PDF).
- RÖMPP Lexikon Chemie, 10. Auflage, 1996-1999: Band 6: T - Z. Georg Thieme Verlag, 2014, ISBN 978-3-13-200071-1 (books.google.com).
