Thénards Blau
Das Pigment Thénards Blau (Dumonts Blau, Leithners Blau) ist ein nach dem französischen Chemiker Louis Jacques Thénard benanntes Cobaltaluminat mit der Formel CoAl2O4. Es handelt sich demnach um ein Oxidpigment. Die klassische Variante wird im Colour Index unter C.I. Pigment Blue 28 gelistet, eine grünlichere Variante mit der Formel Co(Al, Cr)2O4 unter C.I. Pigment Blue 36.[4]
| Kristallstruktur | |||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
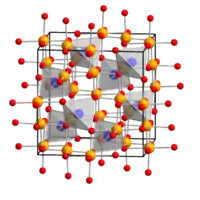 | |||||||||||||
| _ Al3+ _ Co2+ _ O2− | |||||||||||||
| Allgemeines | |||||||||||||
| Name | Thénards Blau | ||||||||||||
| Andere Namen | |||||||||||||
| Verhältnisformel | CoAl2O4 | ||||||||||||
| Kurzbeschreibung |
blaues Pulver[2] | ||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||
| |||||||||||||
| Eigenschaften | |||||||||||||
| Molare Masse | 176,894 g·mol−1 | ||||||||||||
| Aggregatzustand |
fest | ||||||||||||
| Dichte |
4,5 g·cm−3[2] | ||||||||||||
| Schmelzpunkt |
1955 °C[3] | ||||||||||||
| Sicherheitshinweise | |||||||||||||
| |||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||||||
Weitere Namen und Abgrenzung zu anderen Farben
Thénards Blau wird auch Kobaltblau oder Cobaltblau genannt. Selbst wenn man davon absieht, dass „kobaltblau“ auch eine reine Farbtonbezeichnung unabhängig vom Cobaltgehalt sein kann, sind diese Bezeichnungen nicht eindeutig, da auch die Farbe des Kobaltglases und das Pigment Smalte Kobaltblau genannt werden. In allen drei genannten Substanzen kommt die blaue Farbe durch Co2+-Ionen zustande, die von vier Sauerstoffatomen tetraedrisch umgeben sind. Allerdings sind Kobaltglas und das Kobaltglas-Pigment Smalte amorphe Gläser, die zumindest teilweise transparent sind und die in der Regel sehr wenig Aluminium enthalten. Thénards Blau ist dagegen intransparent und hat eine definierte kristalline Struktur – es ist ein Cobaltspinell – und hat einen sehr hohen Al2O3-Anteil.
Weitere Bezeichnungen für Thénards Blau sind Coelestinblau oder Coelinblau (aus Himmelsblau, von lateinisch coelestis „himmlisch“); allerdings sind auch diese Namen nicht eindeutig, da z. B. das Coelestinblau B (C17H18ClN3O4) ein Oxazinfarbstoff ist.
Handelsnamen für Thénards Blau sind z. B. 22-5091, Sicopal Blau 6310, Heucodur 552.
Geschichte
Kobaltblau wurde im Laufe der Geschichte mehrfach entdeckt: im Alten Ägypten, in China und durch Louis Jacques Thénard.[5] Der erste kobaltblaue Farbstoff, das Smalte, wurde bereits in der Antike in Persien zur Dekoration von Tonwaren genutzt. Cobaltaluminat wurde nach Analysen antiker Scherben im Alten Ägypten während der 18. bis 20. Dynastie (von 1550 bis 1070 v. Chr.) verwendet, danach geriet es wieder in Vergessenheit.[6] Für die Herstellung des Cobaltaluminats wurden wahrscheinlich kobalthaltige Alaune (in der Form von Magnesiumaluminiumsulfaten) von den westägyptischen Oasen Dachla (ad-Dakhla) und al-Charga (El-Kharga) als Rohmaterial verwendet.[7] Diese wurden vermutlich in Wasser gelöst und mit Natron als Hydroxide ausgefällt und dann oberhalb 900 °C geglüht. In China wurden ab der Zeit der Tang-Dynastie (618–906 n. Chr.) Cobaltpigmente in keramischen Glasuren genutzt.[5][8] Im 16. bis 18. Jahrhundert waren Blaufarbenwerke im westlichen Erzgebirge europäisches Zentrum der Verhüttung von Cobalterzen und der Herstellung des blauen Farbpigments Smalte, das ein Siliciumglas ist und damit ein amorpher Feststoff, der praktisch kein Aluminiumoxid enthält.
Als Pigment wurde das kristalline Cobalt-Aluminium-Mischoxid Thénards Blau in der Neuzeit erstmals in der Wiener Porzellanmanufaktur von dem Chemiker und Porzellanmaler Josef Leithner erhalten, weshalb es auch Leithners Blau genannt wird. Es finden sich unterschiedliche Angaben über den Zeitpunkt von Leithners Entdeckung: vor allem die Jahre 1775[9] und 1795[10] werden genannt. Da die Porzellanmanufaktur die Rezeptur seiner Farben geheim hielt, ist es plausibel, dass der Pariser Universitätsprofessor Louis Jacques Thénard das Pigment im Juni 1802[11][12] zumindest teilweise unabhängig von Leithner neu entdeckte – allerdings suchte er im Auftrag des Innenministers Jean-Antoine Chaptal in der Porzellanmanufaktur Sèvres gezielt nach einem Ersatz für das teure Ultramarin. Er hatte dabei mit dem Chemiker und Maler Léonor Mérimée zusammengearbeitet; er veröffentlichte seine Entdeckung 1803.[13] Er konnte seinen blauen Kobaltspinell durch Glühen von Aluminiumsulfat und Cobalt(II)-nitrat (Co(NO3)2) synthetisch erzeugen und veranlasste auch eine industrielle Erzeugung des tiefblauen Pigments – die Produktion in Frankreich begann 1807. Der Chemiker Gabriel Dumont verbesserte das Herstellungsverfahren; sein Neffe, ein Fabrikant, brachte die Farbe auf den Markt, wobei der Cobaltspinell unter dem Namen Dumonts Blau (Bleu Dumont) verkauft wurde.[14] Die Vermarktung von Thénards Blau trug dazu bei, dass die ältere Hüttengewinnung von Smalte im 19. Jahrhundert zurückgedrängt wurde.
Herstellung
Das Cobaltaluminiumoxid CoAl2O4 kann aus Cobaltoxiden und Aluminiumoxid erhalten werden. Dabei ist es bei ausreichenden Temperaturen nicht entscheidend, ob man von Cobalt(II)-oxid CoO, Cobalt(III)-oxid Co2O3 oder vom gemischten Oxid Co3O4 ausgeht, da die Co(III)-haltigen Oxide oberhalb 900 °C Sauerstoff abgeben und dabei Co2+ bilden. Als Flussmittel kann Kaliumchlorid verwendet werden. Bei niedrigeren Temperaturen ab 400 °C kann man aus einem Hydroxidgemisch zwar Cobalt-Aluminium-Oxide mit Spinellstruktur erhalten, diese sind aber dunkelgrün und enthalten auch Co3+.[15] Die für ein schönes Blau notwendigen Temperaturen von 1000 °C oder mehr sind mit einem einfachen Bunsenbrenner nur schwer zu erreichen, so dass man bevorzugt einen starken Teclubrenner nutzt; ideal ist vierstündiges Erhitzen auf 1000 °C im Glühofen. Geht man nicht von Oxiden aus, sondern von Aluminiumalkoholaten (z. B. von 2-Butanol) und Cobaltnitrat aus, so kann man mit einem Sol-Gel-Verfahren schon bei 700 °C den blauen Spinell erhalten.[16]
Chemie und Eigenschaften
Cobaltaluminat ist ein Cobalt-Aluminium-Spinell, mit folgender stöchiometrischen Zusammensetzung:
- CoO·Al2O3 (Cobalt(II)-oxid und Aluminiumoxid).
CoAl2O4 ist ein normaler Spinell: die Co2+-Cobaltionen besetzen ein Achtel der Tetraederlücken zwischen den kubisch dichtest gepackten O2−-Sauerstoffionen. Die Al3+-Aluminiumionen besetzen die Hälfte der Oktaederlücken. Die Entstehung von CoAl2O4 dient als Nachweisreaktion auf Aluminium in einer Schmelzprobe in der anorganischen analytischen Chemie.
Bei hohen Temperaturen (900 bis 1100 °C) hat CoAl2O4 eine elektrische Leitfähigkeit, die bei hohen Sauerstoffpartialdrücken durch Defektelektronen entsteht und bei niedrigen Drücken durch Ionenleitung.[17]
Farblehre
Farbcode: #0047AB
Farbcode: #0082CE
Kobaltblau als Farbe ist ein neutrales Blau von hoher Farbsättigung.
- HSV 215°, 100 %, 67 %
- RGB255 (0, 71, 171) dezimal bzw. 0047AB hexadezimal
- CMYK100 (100, 58, 0, 33)
Verwendung
- Pigmentpulver
 Cobaltblau C.I. PB 28
Cobaltblau C.I. PB 28 Cobaltblau grünlich C.I. PB 36
Cobaltblau grünlich C.I. PB 36
Pigment
Das Besondere dieses Pigments ist eine extreme Farbtiefe. Die Chrominanz von etwa 85 %[18] liegt weit außerhalb des Farbraums, der bei der fototechnischen Farbreproduktion oder drucktechnisch erreichbar ist. Im Druck sind deshalb Sonderfarben nötig, da die Brillanz außerhalb des CMYK-Farbraumes des klassischen Vierfarbdrucks liegt. Im RGB-Farbraum von Bildschirmen liegt die Farbe außerhalb des Gamuts und kann nicht wiedergegeben werden. Das Pigment[18] zeigt als Pulver eine deutlich hellere Farbnuance als etwa Ausmischungen in Öl.
Ein charakteristisches Beispiel für die Verwendung dieses Pigments ist das Gemälde des französischen Impressionisten Pierre-Auguste Renoir "La Yole".[19][20]
Im Lackbereich findet Kobaltblau dort Anwendung, wo das Echtheitsniveau von Kupferphthalocyaninblau nicht ausreicht. Dies gilt etwa für die Bewitterungsstabilität von Fassadenfarben. Für andere Bereiche wird das billigere und zugleich farbstärkere Phthalocyaninblau eingesetzt.
Nachweisreaktion
Beim Glühen von Aluminiumsalzen mit Cobalt(II)-nitrat entsteht das blaue Pigment. Die Reaktion kann damit als Nachweisreaktion eingesetzt werden.
Giftigkeit
Cobaltoxide selbst werden als gesundheitsschädlich (H-Sätze H302 Gesundheitsschädlich bei Verschlucken und H410 Sehr giftig für Wasserorganismen mit langfristiger Wirkung) eingestuft. Im Pigment jedoch ist das Cobalt in Spinellmischphase fest eingebaut und kann aufgrund der stabilen Kristallstruktur nicht ausgebaut werden. Das konnte auch in dänischen Untersuchungen an Porzellanmalerinnen bestätigt werden. Hier wurden jedoch toxikologisch relevante Expositionen bei der Exposition gegenüber geringfügig löslichen Cobalt-Zink-Silikat-Farben beobachtet.[21]
Siehe auch
Literatur
- Kurt Wehlte: Werkstoffe und Techniken der Malerei. Otto Maier, Ravensburg 1967, ISBN 3-473-48359-1.
- Cobalt und seine Blaufarben. In: Neue Zürcher Zeitung. 214, 15. September 1993, S. 67.
- A. Roy: Cobalt blue. In: B. H. Berrie (Hrsg.): Artists’ Pigments. A Handbook of Their History and Characteristics. Band 4, National Gallery of Art, Washington 2007, ISBN 978-1-904982-23-4.
Einzelnachweise und Anmerkungen
- Eintrag zu CI 77346 in der CosIng-Datenbank der EU-Kommission, abgerufen am 12. Dezember 2021.
- BASF: Product Safety Data Sheet for SICOPAL® Blue K 6310, abgerufen am 27. Dezember 2019.
- Veronica D'Ippolito, Giovanni B. Andreozzi, Ferdinando Bosi, Ulf Halenius: Blue spinel crystals in the MgAl2O4-CoAl2O4 series: Part I. Flux growth and chemical characterization. In: Mineralogical Society of America (Hrsg.): American Mineralogist. Band 97, Nr. 11-12, November 2012, S. 1828–1833, doi:10.2138/am.2012.4138 (rruff.info [PDF; abgerufen am 3. Februar 2018]).
- Gunter Buxbaum, Gerhard Pfaff: Industrial Inorganic Pigments. Wiley-VCH.
- Robert B. Heimann, Marino Maggetti, Gabriele Heimann, Jasmin Maggetti: Ancient and Historical Ceramics: Materials, Technology, Art and Culinary Traditions. Schweizerbart’sche Verlagsbuchhandlung Nägele und Obermiller, Stuttgart 2014, ISBN 978-3-510-65290-7.
- Walter Noll: Chemie vor unserer Zeit: Antike Pigmente. In: Chemie in unserer Zeit. Band 14, Nr. 2. Verlag Chemie, John Wiley & Sons, Weinheim April 1980, S. 37–43, doi:10.1002/ciuz.19800140202.
- A. J. Shortland, M. S. Tite, I. Ewart: Ancient Exploitation and Use of Cobalt Alums from the Western Oases of Egypt*. In: Archaeometry. Band 48, Nr. 1, 1. Februar 2006, S. 153–168, doi:10.1111/j.1475-4754.2006.00248.x.
- M. S. Tite, A. J. Shortland: Production Technology for Copper- and Cobalt-Blue Vitreous Materials from the New Kingdom Site of Amarna—A Reappraisal*. In: Archaeometry. Band 45, Nr. 2, 1. Mai 2003, S. 285–312, doi:10.1111/1475-4754.00109.
- William Jervis Jones: Historisches Lexikon deutscher Farbbezeichnungen. Band 3: Frühneuhochdeutsch–Neuhochdeutsch; F–K. Akad.-Verlag, Berlin 2013, ISBN 978-3-05-005953-2.
- Leithner, Joseph. In: Biographisches Lexikon des Kaiserthums Oesterreich.
- Gérard Emptoz: Le binôme Gay-Lussac et Thenard: une longue amitié. In: Société des amis de la Bibliothèque de l’Ecole polytechnique SABIX (Hrsg.): Bulletin de la SABIX. Band 50, 2012, S. 31–44 (französisch, openedition.org).
- Sehr häufig wird für Thénards Entdeckung auch die Jahreszahl 1799 genannt, z. B. in der Biografie Louis-Jacques Thenard. auf britannica.com Wenn Chaptal Thénards Arbeiten beauftragt hat, nachdem er Innenminister geworden war, kann das frühestens 1801 geschehen sein.
- Louis Jacques Thénard: Sur les Couleurs, suives d’un procédé pour préparer une couleur bleue aussi belle que l'outremer. In: conseil des mines (Hrsg.): Journal des mines. Band 15, Nr. 1, 1804, S. 128–136 (annales.ensmp.fr [PDF]).
- Notice des products de l’industrie française précedée d’une historique des exposìtìons anterieures. 1834, S. 157 (eingeschränkte Vorschau in der Google-Buchsuche).
- Minori Taguchi, Takayuki Nakane, Kenjiro Hashi, Shinobu Ohki, Tadashi Shimizu: Reaction temperature variations on the crystallographic state of spinel cobalt aluminate. In: Dalton Transactions. Band 42, Nr. 19, 24. April 2013, doi:10.1039/c3dt32828g.
- U. Lavrenčič Štangar, B. Orel, M. Krajnc: Preparation and Spectroscopic Characterization of Blue CoAl2O4 Coatings. In: Journal of Sol-Gel Science and Technology. Band 26, Nr. 1-3, 1. Januar 2003, S. 771–775, doi:10.1023/a:1020770810027.
- Hermann Schmalzried: Ionen- und Elektronenfehlordnung in CoCr2O4 und CoAl2O4. In: Berichte der Bunsengesellschaft für physikalische Chemie. Band 67, Nr. 1, 1. Januar 1963, S. 93–96, doi:10.1002/bbpc.19630670117.
- Farbmuster Kobaltblau (Pigment): nach CIECAM ab plane. In: Bruce MacEvoy: Handprint. Watercolors. Die Abbildung bei seilnacht.com trifft den Farbton, erreicht jedoch nicht die Leuchtkraft des Pigments, abgerufen 16. Mai 2006.
- A. Roy: The Palettes of three Impressionist Paintings. In: National Gallery Technical Bulletin. Band 9, 1985, S. 12–20.
- Pierre-Auguste Renoir, ‘La Yole’ Colourlex.
- E. Prescott, B. Netterstrøm, J. Faber, L. Hegedüs, P. Suadicani, J. M. Christensen: Effect of occupational exposure to cobalt blue dyes on the thyroid volume and function of female plate painters. In: Scandinavian Journal of Work, Environment & Health. Band 18, Nr. 2, April 1992, S. 101–104, PMID 1604269.

